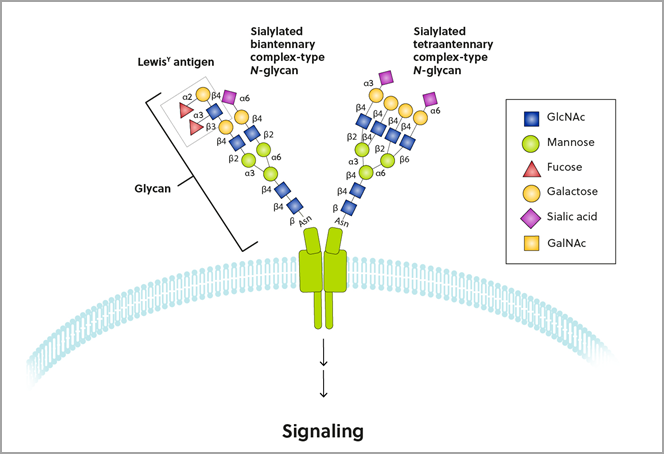
Les sucres sont essentiels aux processus physiologiques normaux de la cellule, mais ils jouent également un rôle majeur dans les processus pathologiques. Les bactéries et les virus sont même capables de les identifier pour infecter leurs hôtes. Même si ce sujet de recherche reste difficile à cerner, le domaine de la glycobiologie a suscité beaucoup d'intérêt ces dernières années de la part de chercheurs dans un certain nombre de disciplines. L'un de ces outils est la chimie bioorthogonale qui peut servir à imager les glycanes, structures glucidiques attachées aux protéines et aux peptides (Figure 1).
Récemment, le groupe de recherche de Carolyn Bertozzi a employé la chimie bioorthogonale pour découvrir un nouvelle biomolécule fascinante, le glycoARN, qui a ouvert une toute nouvelle voie de recherche dans le secteur de la chimie bioorthogonale depuis des années. Nous examinerons ici le monde de la chimie bioorthogonale et ses applications, notamment la manière dont elle a contribué à faire progresser le domaine de la glycobiologie et les possibilités qu'il ouvre.
Qu'est-ce que la chimie bioorthogonale ?
Le terme chimie bioorthogonale a été inventé par le groupe de recherche de Bertozzi, pionnier dans ce domaine depuis de nombreuses années. La chimie bioorthogonale est une série de réactions qui peuvent intervenir dans des environnements biologiques en entraînant un minimum d'effets sur les biomolécules ou de perturbations des processus biochimiques. Le processus de la chimie bioorthogonale répond aux critères stricts nécessaires à la création de réactions telles qu'elles se produiraient dans les systèmes biologiques :
- Ces réactions doivent se produire aux températures et au pH des environnements physiologiques.
- Elles doivent fournir des produits de manière sélective et à haut rendement sans être affectées par l'eau ou les nucléophiles endogènes, les électrophiles, les réducteurs ou les oxydants présents dans les environnements biologiques complexes.
- Elles doivent être rapides, même à faible concentration, en formant des produits de réaction stable.
- Elles doivent impliquer des groupes fonctionnels qui ne sont pas naturellement présents dans les systèmes biologiques.
À quoi sert la chimie bioorthogonale ?
CAS Collection de contenusTM nous a permis d'analyser les tendances de publication dans les applications de chimie bioorthogonale de 2010 à 2020 (Figure 2). Entre 2010 et 2020, l'imagerie a représenté l'usage le plus important de la chimie bioorthogonale, suivie de la mise au point et de l'administration de médicaments.
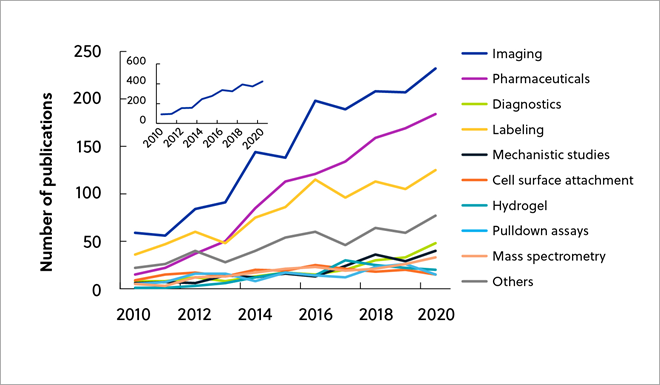
(*L'année 2010 a été choisie comme point de référence initial car c'est la première année au cours de laquelle le nombre de documents contenant le terme « chimie bioorthogonale » a augmenté de manière significative par rapport à l'année précédente. Environ 90 % du nombre total de documents contenant le terme « bioorthogonal » ou « bio-orthogonal » ont été publiés depuis 2010.)
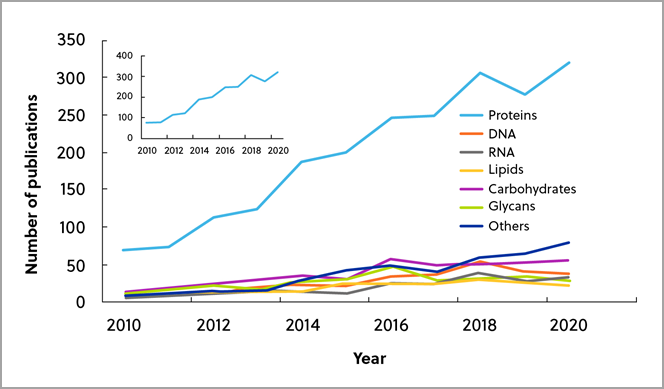
En outre, la chimie bioorthogonale des protéines représente le nombre le plus élevé de publications, probablement parce que ces méthodes sont les plus établies, les autres domaines progressant régulièrement eux aussi, y compris le secteur relativement nouveau des glycanes (Figure 3).
Imagerie des glycanes
La chimie bioorthogonale s'est avérée un outil essentiel pour comprendre les structures, la localisation et les fonctions biologiques des glycanes. Oligosaccharides fixés aux peptides, aux protéines et aux lipides fréquemment présents dans les parois cellulaires, les glycanes peuvent servir à visualiser les types de cellule de manière sélective. Les précurseurs métaboliques des glycanes comprennent de nombreuses fonctionnalités bioorthogonales, notamment des azotures, des alcynes terminaux et des alcynes contraints. Les glycanes peuvent être visualisés à l'aide du partenaire bioorthogonal approprié. Par exemple, les azotures sont visibles avec des esters contenant des phosphines ou des thioesters par réaction de ligature de Staudinger ou de Staudinger sans trace, les alcynes terminaux ou les alcynes contraints sont identifiés à l'aide de la réaction CuAAC ou SPAAC, respectivement.
La chimie bioorthogonale fait progresser la glycobiologie
Jusqu'à présent, l'ARN n'était pas une cible majeure de glycosylation ; toutefois, une découverte récente importante a été rendue possible par le marquage métabolique et la chimie bioorthogonale : la découverte du « glycoARN ». À l'aide d'une batterie d'approches chimiques et biochimiques, le Dr Ryan A. Flynn a dirigé un groupe de recherche de Bertozzi qui a découvert que les petits ARN non codants conservés portent des glycanes sialylés et que les glycoARN sont présents dans de multiples types de cellules et espèces de mammifères, à la fois dans les cultures cellulaires et in vivo.
La stratégie utilisée pour cette découverte a consisté à marquer métaboliquement les cellules ou les animaux avec des sucres précurseurs fonctionnalisés avec un groupe d'azotures cliquables. Les azidosucres permettent une réaction bioorthogonale avec une sonde de biotine pour l'enrichissement, l'identification et la visualisation après incorporation dans le glycane cellulaire. En utilisant un précurseur de l'acide sialique marqué par un azoture, la N-azido-acetyl-mannosamine péracétylée (Ac4ManNAz), on a constaté que les préparations d'ARN hautement purifiées présentaient une réactivité aux azotures. L'assemblage du glycoARN dépend de la machinerie de biosynthèse des N-glycanes canoniques et produit des structures enrichies en acide sialique et en fucose. Une analyse plus poussée des cellules vivantes a révélé que la majorité des glycoARN sont présents à la surface de la cellule, où ils interagissent avec des anticorps anti-ARNd et avec les membres de la famille des récepteurs Siglec. Des recherches plus approfondies s'imposent pour déterminer le rôle du glycoARN.
La chimie bioorthogonale a permis d'établir une interface directe entre la biologie de l'ARN et la glycobiologie, et de nombreuses autres découvertes restent à approfondir.
Quelles opportunités nous réserve l'avenir de la chimie bioorthogonale ?
Avec un large éventail d'applications en science et en médecine, la chimie bioorthogonale a été très fréquemment utilisée ces dernières années pour faire progresser la recherche. Outre le développement de la glycosylation grâce à la découverte des glycoARN, elle a démontré des applications prometteuses dans l'administration et le ciblage des médicaments, et son utilisation devrait encore prendre de l'ampleur à l'avenir. Entre autres exemples, on peut citer :
- Synthèse in situ d'agents pharmaceutiques : la chimie bioorthogonale pourrait être utile pour assembler des médicaments à partir de précurseurs plus petits. Les médicaments créés sur mesure pourraient ainsi être plus efficaces et moins toxiques ; la portée de l'intervention pharmacologique pourrait aussi être étendue.
- Marquage des glycanes : des nanoparticules lipidiques contenant des galactosamines marquées avec des azotures et utilisant des ligands de folate ont été générées. En raison de la présence accrue de récepteurs de folate dans les tissus tumoraux, une internalisation des LNP s'est produite, suivie d'une libération de la charge dans les cellules tumorales. Les membranes tumorales ont intégré la dibenzocyclooctyne activée par des azotures, déclenchant une réponse immunitaire lorsque les cellules tumorales étaient exposées à des sérums humains.
- Cliquer pour libérer : cette méthode utilise la chimie bioorthogonale pour contrôler le moment et l'emplacement de la libération du médicament, avec pour corollaire un traitement qui devrait présenter une toxicité sélective pour les cellules cibles.
Grâce à la poursuite du développement et à l'affinage des réactions, la chimie bioorthogonale deviendra un outil important pour l'approfondissement de la recherche.
Voir notre article dans Bioconjugate Chemistry et le rapport CAS Insights connexe pour plus de détails au sujet de la chimie bioorthogonale et de ses multiples applications.