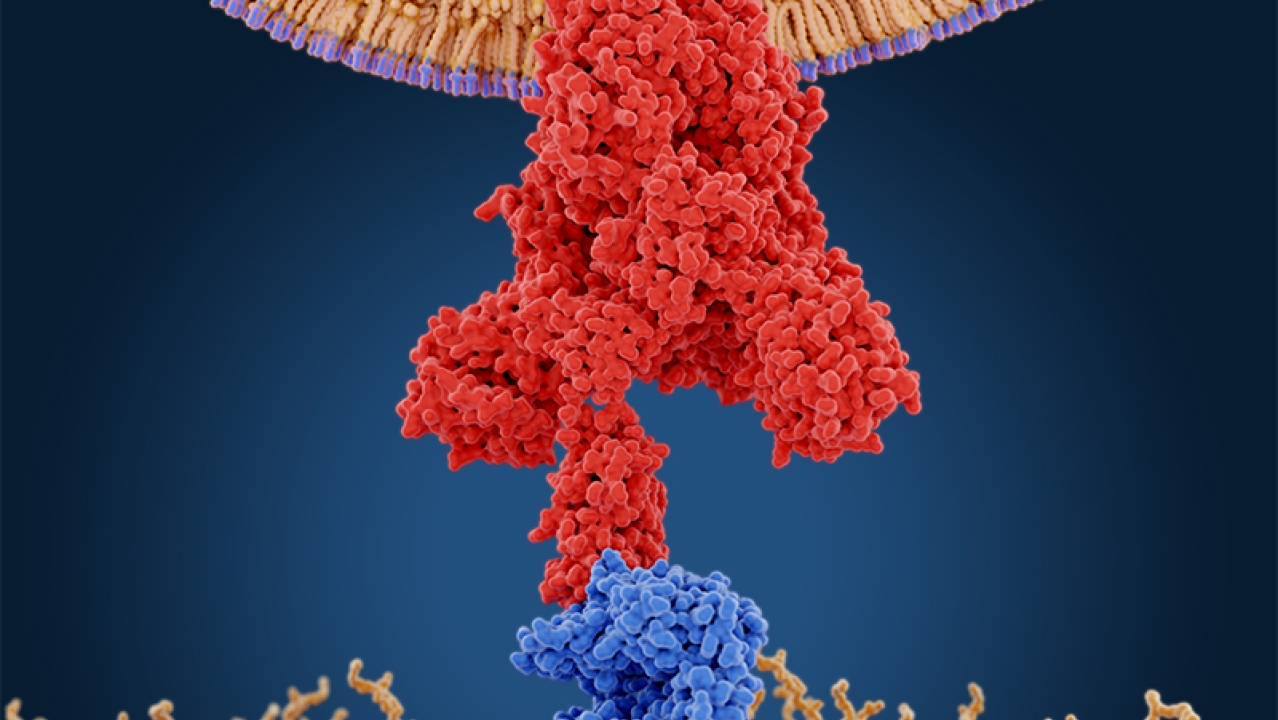
COVID-19 치료제 개발 연구에서 중요한 단계 중 하나가 바이러스가 인체 세포에 침투하는 방식을 명확하게 이해하는 것입니다. 이 인사이트는 그러한 침투 경로 차단을 목표로 하는 항바이러스 치료제 개발의 토대가 될 것입니다.
2002년 전염병 원인균으로 처음 발견된 SARS-CoV 바이러스와 현재 COVID-19를 발병시킨 관련 코로나바이러스, SARS-CoV-2에 대한 연구 결과, 두 바이러스 모두 바이러스막에서 돌출되는 스파이크(S) 단백질이 인체 세포 표면에서 최소 하나의 단백질, 안지오텐신 전환 효소 2(ACE2)에 결합된다는 공통점을 갖고 있다는 사실이 밝혀졌습니다. 결합 후에는 다른 단백질을 작은 조각으로 분해하는 인간 효소, 프로테아제가 스파이크 단백질을 절단하거나 S1 외절을 제거하고 S2 내절을 나타내도록 "준비"시킵니다. 스파이크 단백질 S2 내절로 인해 바이러스막과 인체 세포막이 융합되며 바이러스 유전 물질이 세포로 들어가 복제를 시작합니다. 최근 한 포스팅에서 ACE2의 역할을 강조하여 이 과정을 요약 정리했습니다. 이 포스팅에서는 바이러스가 인체 세포에 침투하는 데 프로테아제, 즉 인간 단백질 분해 효소가 어떤 역할을 하는지 자세히 살펴보며 그 과정을 공략하는 항바이러스 치료법에 대해서도 알아봅니다.
SARS-CoV-2 스파이크 단백질을 구성하는 두 요소
SARS-CoV-2 스파크 단백질은 머리 부분이 크고 줄기 부분이 길고 얇은 나사 모양처럼 생겼습니다(그림 1). 이 스파이크 단백질 3개가 서로 결합되어 더 큰 나사 모양의 삼량체가 됩니다. 줄기 부분은 바이러스막에 삽입되어 머리 부분이 바이러스에서 이탈하지 못하도록 고정시키는 역할을 합니다. 이 큰 머리 부분과 줄기의 일부를 스파이크 단백질의 S1 영역이라고 합니다. 줄기에서 바이러스막에 좀 더 가까운 나머지 부분을 S2 영역이라고 합니다.
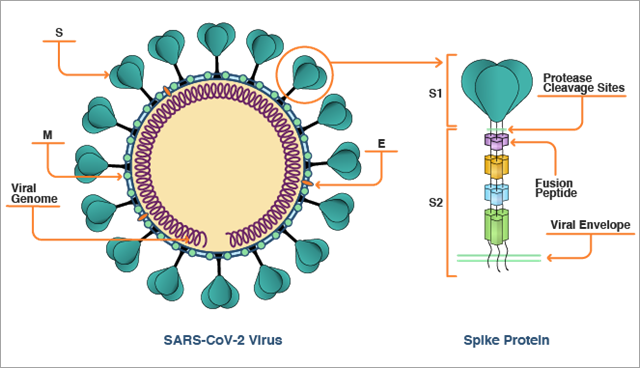
스파이크 단백질이 체내로 들어가 호흡계, 위장관, 혈관 또는 표면에 ACE2를 나타내는 다른 세포와 접촉하면 스파이크 단백질의 S1 영역이 세포 표면의 ACE2와 결합하고 바이러스를 인체 세포 외부에 고정시킵니다. 이것이 바로 바이러스 복제 프로세스의 첫 번째 단계입니다.
세포에 침투하는 SARS-CoV-2
세포에 결합된 바이러스는 두 가지 다른 침투 경로를 갖게 됩니다(그림 2). 사용하는 경로는 스파이크 단백질을 "준비"시키는 프로테아제(단백질 분해 효소)가 있는지 여부에 따라 다릅니다. 또한 프로테아제 존재 여부는 바이러스가 침입하는 인간 세포의 유형과 해당 세포의 특정 조건에 따라 결정됩니다. 스파이크 단백질을 쪼갤 수 있는 여러 프로테아제는 막관통 세린 프로테이나아제 2(TMPRSS2), Furin, 엘라스타아제, 트립신 등 여러 가지가 있습니다. TMPRSS2는 인간 폐 세포로 표현됩니다. 따라서 바이러스가 호흡기 세포에 침투하는 데 중요한 역할을 하는 것으로 알려져 있습니다.
이러한 프로테아제가 스파이크-ACE2 결합 인터페이스 가까운 곳에 존재하면 스파이크 단백질을 쪼개서 S2 영역, 구체적으로 스파이크 단백질의 융합 펩타이드 영역이 노출됩니다. 스파이크 단백질의 이 융합 펩타이드 영역은 소수성이 더 강한 또는 지질과 유사한 아미노산으로 만들어져 있으며 지질 함유 세포막에 삽입되어 바이러스막-세포막 융합을 유도하고 이어서 바이러스 유전체가 세포에 침투하게 됩니다(그림 2a). 이러한 분할은 스파이크-ACE2 결합 이후에 발생해야 합니다. 그 이전에 발생하면 바이러스의 세포 감염율이 낮아집니다.
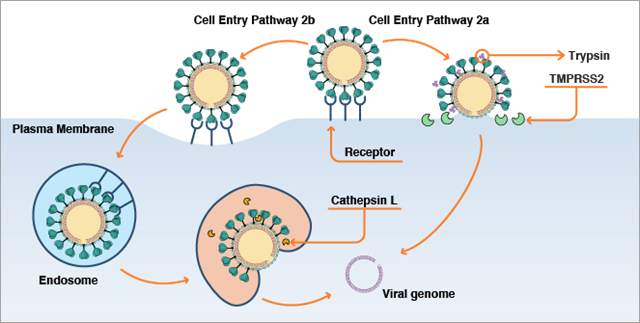
프로테아제가 스파이크-ACE2 결합 인터페이스 가까운 곳에 없으면 내포 작용이라는 다른 경로로 바이러스가 세포에 침투합니다(그림 2b). 이 프로세스에서는 세포막의 작은 영역을 집어 넣는 방식으로 세포 외부에서 ACE2 단백질에 결합된 코로나바이러스를 둘러싼 다음 다시 꺼내 외부 물질을 세포 안으로 가져오는 세포내 이입 소포를 형성합니다. 이 과정이 끝나면 세포내 이입 소포가 엔도솜이라는 세포 내 막벽 소낭과 융합됩니다. 엔도솜에는 카텝신 L과 같이 스파이크 단백질을 쪼개 융합 펩타이드 영역을 노출시키는 프로테아제가 있습니다. 이 융합 펩타이드는 바이러스 막과 엔도솜 막의 융합을 중재하며 이후 바이러스 유전체가 세포 안으로 들어가도록 유도합니다.
최근 연구 결과에서는 SARS-CoV-2가 세포에 침투할 수 있는 세 번째 방법의 가능성을 제안하고 있습니다. 바이러스가 복제 과정을 거쳐 세포 내부에 새 바이러스 입자를 만들 때 새로운 바이러스 구성 과정에서 퓨린이라는 단백질 분해 효소에 의해 일부 스파이크 단백질이 미리 쪼개지거나 먼저 준비를 마칠 수 있습니다. 이는 바이러스가 세포에서 분리되면 스파이크 단백질이 먼저 준비된 바이러스가 다른 세포와 융합되어 감염시킬 수 있음을 의미합니다. 앞에서 설명한 두 가지 "정상적인" 스파이크 단백질 분할 경로 중 하나에 대해 프로테아제의 양이 적은 경우도 마찬가지입니다.
반격 준비
COVID-19 퇴치를 위해 감염 주기에서 스파이크 ̶ ACE2 ̶막 융합 ̶ 엔도시토시스 부분을 표적으로 할 수 있는 약물에 대한 많은 연구가 진행되고 있습니다. 이전 포스팅에서는 재조합형 가용성 ACE2의 치료제 가능성을 강조했습니다. 이 경우 SARS-CoV-2가 세포 표면의 ACE2에 결합되려면 스파이크 단백질을 비활성화해야 합니다. 그러나 다른 많은 신약 후보도 함께 고려되고 있습니다.
나파모스타트와 MI-1851은 스파이크 단백질 분할에 관여하는 프로테아제, TMPRSS2와 퓨린을 각각 억제하므로 시험관에서 SARS-CoV-2 감염을 줄일 수 있습니다. 스파이크 단백질의 작은 부분과 유사한 매우 짧은 단백질, 펩타이드는 바이러스에서 준비된 스파이크 단백질을 "막는" 방식으로 바이러스 및 인간 세포막의 융합을 억제하는 것으로 알려져 있습니다. 막 융합 프로세스에서 형태를 바꿈으로써 바이러스 침입을 방해합니다. 마지막으로, SARS-CoV-2 감염을 차단하는 것으로 알려진 PIKfyve 억제제가 있습니다. PIKfyve는 특정 지질에 인산기를 추가하는 효소 역할을 하는 인간 지질 키나아제입니다. PIKfyve가 세포내 이입 경로의 바이러스 침투 경로에 있어 엔도좀 대사에 관여하므로 PIKfyve 억제제는 항바이러스성 활성을 갖습니다.
이들은 SARS-CoV-2 바이러스 침투 억제제로 연구되고 있는 여러 약물 후보 중 일부에 불과합니다. COVID-19 치료제 개발을 위해 많은 표적에 대한 연구를 진행하고 있습니다. 스파이크 단백질, ACE2, 스파이크 단백질을 쪼개는 프로테아제, 세포내 이입 경로의 구성 요소 모두 가능한 연구 대상이며 이들 각각의 표적과 관련된 항바이러스성 활성을 갖는 많은 물질이 있습니다. CAS는 이러한 잠재적 후보 물질을 더 빠르게 식별하려는 연구 노력을 돕기 위해, CAS REGISTRY®를 토대로 알려진 항바이러스 약물과 이러한 항바이러스성 약물과 구조적으로 유사한 관련 화합물에 대한 공개 데이터세트를 발표했습니다. 이 데이터세트를 비롯한 다른 CAS 공개 COVID-19 리소스를 다운로드하여 알아보십시오.



