COVID-19の治療法開発を急ぐうえで重要な手順は、ウイルスが人の細胞内に侵入する仕組みを科学者が正しく理解することです。 この知識は、その感染経路をブロックすることを標的とした抗ウイルス治療法の開発を支えます。
2002年に出現して大流行を引き起こした最初のSARS-CoVの研究と、現在COVID-19を引き起こしているコロナウイルスSARS-CoV-2の研究では、ウイルスの膜から隆起するスパイク(S)タンパク質がヒト細胞表面にある少なくとも1種類のタンパク質、アンジオテンシン変換酵素2(ACE2)と結合することが明らかになっています。 結合の後で他のタンパク質を分割、切断または刺激するヒトの酵素であるプロテアーゼは、スパイクタンパク質外側の切片(S1)を取り除き、内側の切片(S2)を露出させます。 スパイクタンパク質のS2切片はウイルス細胞膜とヒト細胞膜を結合させ、ウイルスの遺伝情報が細胞内に侵入して複製を開始します。 最近の記事では、ACE2の役割に焦点を当ててこのプロセスをまとめています。 この記事では、ウイルスが人体に侵入する際、それを助けるヒトプロテアーゼの役割を詳しく説明し、そしてその相互作用を標的とする抗ウイルス治療にも注目します。
SARS-CoV-2のスパイクタンパク質:2つの切片について
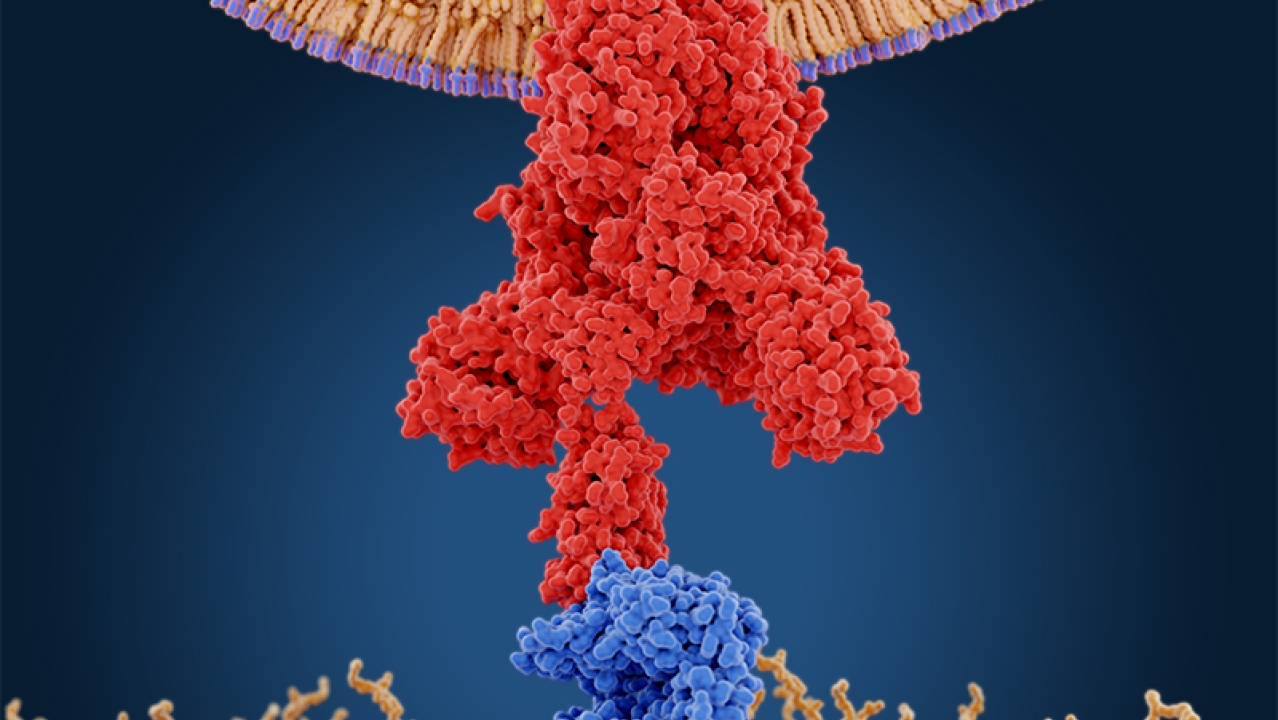
SARS-CoV-2のスパイクタンパク質は、頭が大きく細長い軸を持ったネジのような形をしています(図1)。 3つのスパイクタンパク質が結合して三量体を形成し、予測通り、さらに大きなネジのような形になります。 軸がウイルスの細胞膜に挿入され、頭の部分をウイルスの外部に向けています。 この大きな頭の部分と軸の一部が、スパイクタンパク質のS1領域です。 ウイルスの膜に近い軸の残り部分がS2領域となります。
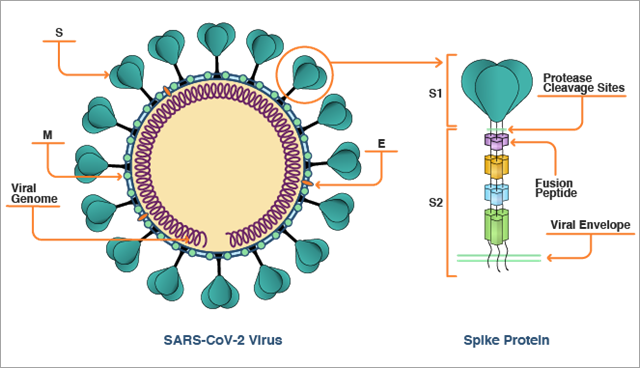
これが体内に侵入して呼吸器系、消化管、血管、その他の表面にACE2を発現する細胞と接触すると、スパイクタンパク質のS1領域が細胞表面のACE2に結合し、人細胞の外側にウイルスを繋ぎ止めます。 これがウイルス複製プロセスの最初の段階です。
何らかの方法でSARS-CoV-2が細胞に侵入
ウイルスが細胞と結合した後の侵入経路には2つの異なる可能性があります(図2)。 使用される経路は、スパイクタンパク質を「準備する」ヒトプロテアーゼが存在するかどうかによって変わります。 プロテアーゼの有無はウイルスが侵入する人細胞の種類およびその細胞の特定の状況によって異なります。 いくつかのヒトプロテアーゼはスパイクタンパク質を分割できます。これにはII型膜貫通型セリンプロテアーゼ(TMPRSS2)、フリン、エラスターゼ、トリプシンが含まれます。 TMPRSS2は人の肺細胞に発現します。 よって、呼吸器系の細胞へのウイルス侵入において重要な役割を果たしていると考えられています。
これらのプロテアーゼがスパイクとACE2の結合面付近に存在している場合、スパイクタンパク質が分割されてS2領域、具体的にはスパイクタンパク質の融合ペプチド領域が露出します。 このスパイクの融合ペプチド領域は、より疎水性が高い、脂質様のアミノ酸であるため、脂質を含む細胞膜に挿入され、ウイルス膜と細胞膜の融合と、その後のウイルス遺伝子の細胞への侵入を誘導します(図2a)。 この分割は、スパイクとACE2の結合後に発生する必要があります。 その前に生じた場合は、細胞へのウイルスの感染力は弱まります。
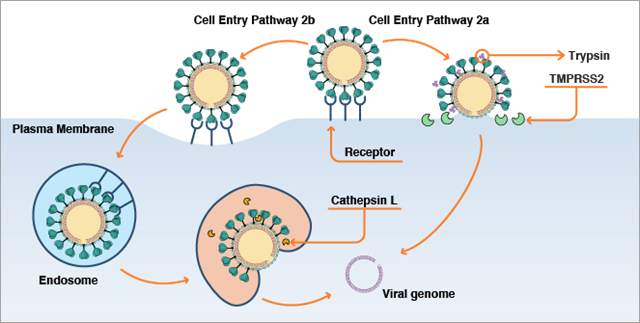
スパイクとACE2の結合面の近くにプロテアーゼが存在しない場合、ウイルスは食作用という別の経路で細胞に侵入します(図2b)。 このプロセスでは、細胞外のACE2タンパク質に結合したコロナウイルスは細胞膜の小さな領域の圧入により貪食され、細胞内小胞の形で外部の物質を細胞内に取り込みます。 これが生じると、細胞内小胞はエンドゾームという細胞内膜壁小胞に融合します。 エンドゾーム内にはカテプシンLというプロテアーゼが存在します。これがスパイクタンパク質を分割し、融合ペプチド領域を露出させます。 融合ペプチドはウイルス膜とエンドゾーム膜の融合を媒介し、その後のウイルス遺伝子の細胞への侵入を誘導します。
最近のエビデンスでは、SARS-CoV-2が細胞に侵入する第3の経路の存在が示唆されています。 ウイルスが複製して新しいウイルス粒子を細胞内に生じさせる際に、新しいウイルス構築プロセスで一部のスパイクタンパク質がフリンにより既に分割(刺激)されている可能性があります。 これは、上記2つの「通常の」スパイクタンパク質分割経路に存在しているプロテアーゼの量が他の細胞で低い場合であっても、ウイルスが細胞内に広がる時既に刺激されたスパイクタンパク質を持つウイルスが他の細胞に融合して感染する可能性があることを意味しています。
対処方法の計画
研究者は、COVID-19の感染を妨げるために、感染過程におけるスパイクとACE2、膜融合、食作用の部分を標的にした薬剤を開発すべく懸命に努力しています。 前回の記事では、潜在的な治療方法として組み換え可用性ACE2に焦点を当てました。 これはSARS-CoV-2が細胞表面のACE2に結合する前に、スパイクタンパク質を非活性化する作用があります。 しかし、その他の多くの候補薬も検討されています。
NafomastatとMI-1851はスパイクタンパク質の分割に関与するプロテアーゼであるTMPRSS2とフリンをそれぞれ阻害します。試験管ではSARS-CoV-2感染を減らす可能性を示しています。 スパイクタンパク質の小さな領域に類似している非常に短いタンパク質であるペプチドは、膜の融合プロセス中に形状が変化する際、ウイルスの刺激されたスパイクタンパク質を妨害することで、ウイルスと人の細胞膜との融合を阻害することが示されています。 これによりウイルスの侵入を防ぎます。 最後に、PIKfyve阻害剤はSARS-CoV-2感染の既知の遮断薬です。 PIKfyveはヒトの脂質キナーゼで、特定の脂質にリン酸基を加える酵素の一種です。 PIKfyveはウイルス侵入のエンドサイトーシス経路におけるエンドソームの代謝に関与しているため、PIKfyve阻害剤には抗ウイルス活性効果があることになります。
これらは、SARS-CoV-2ウイルスの侵入阻害薬として研究されている数多くの候補薬のうち数例にすぎません。 他にもCOVID-19の治療法として研究の対象となる多くの標的が存在しています。 スパイクタンパク質、ACE2、スパイクタンパク質を分割するプロテアーゼ、食作用経路の構成要素は、すべて研究対象となる可能性があります。そして、これらの標的それぞれに関連する抗ウイルス活性を持つ物質も数多く存在しています。 科学者がこれらの有望な候補薬を迅速に特定できるように、CASはCAS REGISTRY®から抽出したオープンセットのデータセットを公開しました。これには既知の抗ウイルス薬と既知の抗ウイルス薬と構造的に似ている関連化合物が記載されています。 詳細やダウンロード、およびその他のCASオープンアクセスのCOVID-19関連リソースはこちらからどうぞ。



