"Estamos no meio de uma revolução terapêutica", de acordo com os autores de um artigo de revisão recente, publicado na Frontiers in Bioengineering and Biotechnology. Os autores comentam sobre a rápida expansão das terapias de RNA na pesquisa moderna e no desenvolvimento clínico, impulsionada em parte pelo interesse nas vacinas de RNA contra a Covid-19 durante a pandemia de SARS-CoV-2, ainda em andamento.
Tradicionalmente, o desenvolvimento de medicamentos tem sido dominado pelos chamados medicamentos de pequenas moléculas (definidas como qualquer composto orgânico com baixo peso molecular), que ainda têm inúmeras aplicações na medicina. No entanto, os avanços da biotecnologia e da biologia molecular têm permitido aos pesquisadores projetar agentes macromoleculares que variam de anticorpos monoclonais e proteínas recombinantes a oligonucleotídeos e genes/fragmentos de genes como candidatos a medicamentos. Como consequência, ‘os produtos biológicos’ se estabeleceram como os principais elementos na caixa de ferramentas das terapias disponíveis hoje. No início de 2020, os produtos biológicos representavam sete dos 10 medicamentos mais vendidos no mundo.
Além disso, surgiu o design de medicamentos à base de ácido nucleico – e atualmente está em rápida expansão. Embora o desenvolvimento clínico de terapias de RNA tenha sido tradicionalmente dificultado por desafios como eficiência e imunogenicidade, o sucesso recente das vacinas de mRNA para a Covid-19 e a aprovação de diversos medicamentos baseados em RNA deram um impulso substancial ao campo de estudo. Usando o CAS Content Collection™ – a maior coleção de conhecimento científico publicado com curadoria humana – examinamos a aplicação de RNA na medicina moderna.
Leia o relatório do CAS Insights: "Medicamentos derivados de RNA: uma revisão das tendências e desenvolvimentos de pesquisa"
Vantagens e desafios das terapias de RNA
A mira nos alvos "não passíveis de tratamento"
Uma grande vantagem da terapia de RNA é que os medicamentos de RNA podem ser usados para atacar moléculas ‘não passíveis de tratamento’, que são difíceis ou impossíveis de atingir usando medicamentos à base de pequenas moléculas. Somente cerca de um quinto das proteínas pode ser alvo dos medicamentos usados normalmente, incluindo pequenas moléculas e anticorpos e não é possível ter RNAs não codificantes como alvo usando as pequenas moléculas tradicionais ou anticorpos monoclonais (que se ligam a regiões do local ativo dos receptores de proteínas ou enzimas, exigindo assim que ocorra a tradução).
Síntese facilitada
Os produtos de RNA podem ter grandes vantagens de fabricação sobre as proteínas em termos de simplicidade, custo-benefício e velocidade dos processos de fabricação, tornados particularmente relevantes no desenvolvimento recente de vacinas de RNA. As estratégias à base de ácido nucleico também podem contornar a necessidade de processos complexos de síntese como modificações pós-tradicionais ao utilizar a maquinaria celular da célula de mamífero.
Além disso, a sequência do RNA pode ser ajustada rapidamente, entregando moléculas personalizadas para diferentes alvos. Isso agiliza muito o processo de desenvolvimento, o que ficou bem claro com o rápido desenvolvimento das vacinas de RNA para a Covid-19.
Segurança e efeitos colaterais
Por entrarem no núcleo, os medicamentos de DNA despertam preocupações com a segurança devido à possível integração com o genoma do hospedeiro. Exceto os RNAs do sistema CRISPR-Cas, que editam o genoma, os RNAs não alteram o material genômico e não apresentam risco de integração genômica.
No entanto, as terapias de RNA podem ter problemas de especificidade que podem causar efeitos colaterais, e sua suscetibilidade à degradação pode gerar uma farmacodinâmica ruim, complicando seu uso. Alguns desses problemas podem ser mitigados ao se modificar quimicamente o RNA, um tópico sobre o qual as pesquisas têm se concentrado.
Entrega
As terapias de RNA tendem a ter um tamanho grande, em comparação com as terapias de pequenas moléculas, e têm uma carga elétrica elevada, tornando desafiador a entrega intracelular em suas formas nativas.
Tendências de pesquisa em terapias de RNA
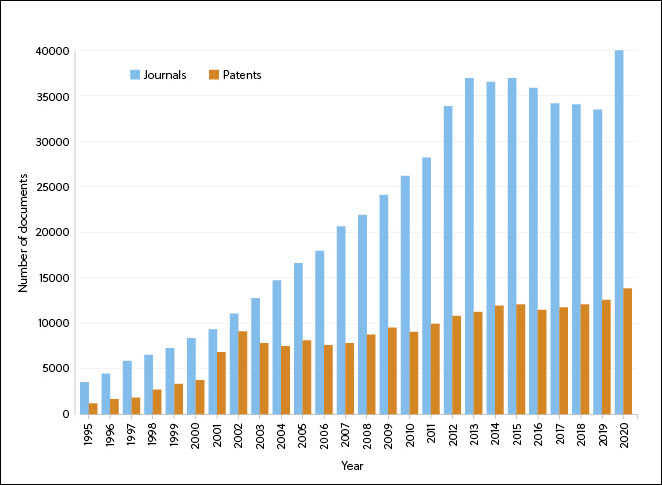
Desde 1995, tem havido um aumento constante no número de revistas científicas e patentes contendo informações sobre a terapia de RNA, atingindo seu pico em pacientes por volta de 2001 (possivelmente relacionado ao primeiro ensaio clínico humano usando células dendríticas transfectadas com mRNA codificando antígenos tumorais) e um aumento do número de revistas em 2020 (muito provavelmente resultando do interesse nas vacinas de mRNA para a Covid-19) (Figura 1).
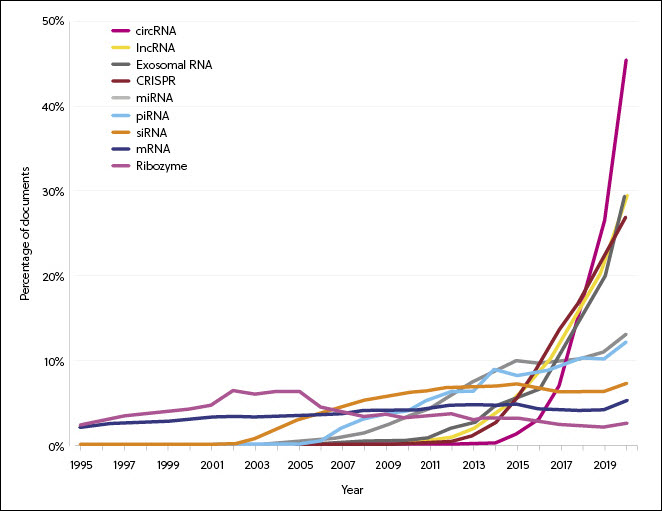
A pesquisa de RNA tornou-se gradualmente mais diversificada à medida que novos tipos de RNA são descobertos, particularmente nas áreas de siRNA, miRNA, lncRNA e CRISPR (Figura 2). As taxas de aumento nos volumes de publicação de circRNA, exossomo de RNA, lncRNA e CRISPR são significativamente mais rápidas do que o resto. Notavelmente, a tecnologia CRISPR foi responsável por 20% dos pedidos de patentes em geral, relacionados ao RNA em 2020. Isso coincide com um número acelerado de aprovações de terapias baseadas em CRISPR para iniciar os ensaios clínicos.
Interferir na funcionalidade de RNAs recém-descobertos é considerada uma ferramenta terapêutica promissora para superar as fraquezas das abordagens terapêuticas tradicionais (Tabela 1).
| Tipo de RNA | Funções terapêuticas |
| mRNA | O princípio básico da terapia de mRNA envolve a entrega de mRNA transcrito in vitro em uma célula alvo, onde o mRNA é traduzido para uma proteína funcional, ou seja, anticorpos, antígenos e citocinas. |
| siRNA | Por meio da degradação direcionada de mRNA, o siRNA faz a mediação do silenciamento de genes específicos de sequência para a patogênese de várias doenças associadas a um histórico genético conhecido. |
| miRNA | O miRNA pode conciliar a expressão de vários genes-alvo diferentes; simultaneamente ao mediar a degradação de mRNA alvo ou a repressão de tradução de mRNA. |
| IncRNA | Os lncRNAs são um grande grupo de genes de RNA estruturalmente complexos que podem interagir com DNA, RNA ou moléculas de proteína (histonas) para regular a transcrição de genes por meio de modificações epigenéticas (principalmente por meio de metilação e acetilação). |
| circRNA | Os circRNAs podem sequestrar proteínas ou translocar proteínas entre os compartimentos subcelulares. A desregulação de circRNAs tem sido implicada em uma variedade de doenças, especialmente câncer, doenças cardiovasculares e doenças neurológicas. De uma maneira específica de tecido ou célula, as abordagens de ganho de função e perda de função são normalmente realizadas usando a expressão circRNA. |
| piRNA | Os piRNAs podem se ligar às proteínas piwi para formar um complexo piRNA/piwi, influenciando assim o silenciamento de transposons, espermiogênese, rearranjo do genoma, regulação epigenética, regulação de proteínas e manutenção de células-tronco germinativas. |
| Ribozima | As enzimas de RNA – ribozimas – são moléculas de RNA catalíticas que reconhecem seu RNA alvo de uma maneira altamente específica de sequência para regular negativamente e reparar genes patogênicos. Elas podem ser usadas para tratar uma variedade de doenças que vão desde distúrbios metabólicos inatos até infecções virais e doenças adquiridas, como câncer. |
| exossoma de RNA | Os exossomos são um tipo de nanovesícula extracelular potencialmente utilizada para o diagnóstico ou a terapia de diversas indicações patológicas. Pesquisas em andamento investigam o potencial da detecção de RNA de exossomos no diagnóstico clínico. Para fins terapêuticos, a entrega de RNA pequeno baseada em exossomos é usada como uma ferramenta de silenciamento de genes pós-transcricional potente e específica por degradação catalítica ou parada de tradução de RNA direcionado. |
| CRISPR | O sistema CRISPR-Cas9 é uma das tecnologias de edição de genes específicos de sequência mais versáteis e eficientes que podem ser usadas para edição de genoma, investigação de função gênica e terapia de genes. Até o momento, o CRISPR-Cas9 tem sido amplamente utilizado em doenças genéticas, incluindo distrofia muscular de Duchenne, deficiência de α1-antitripsina, hemofilia, perda auditiva e doenças hematopoiéticas. |
Em que áreas terapêuticas estão concentradas as terapias de RNA?
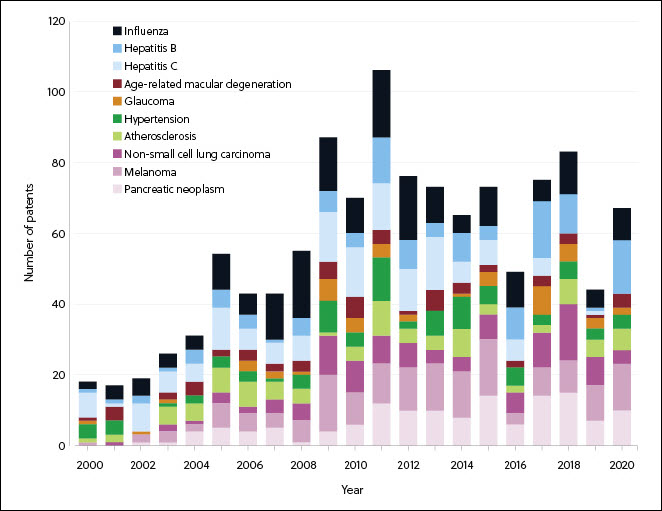
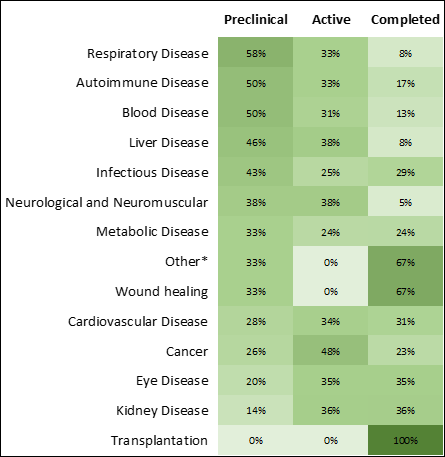
As doenças infecciosas e o câncer apresentam o maior crescimento e o maior número de terapias na fase de pesquisa (Figuras 3 e 4). A pandemia da Covid-19 intensificou as fases de pesquisa e o número de terapias aprovadas dos medicamentos de RNA para doenças infecciosas (Figura 4), levando ao mercado a primeira terapia de mRNA aprovada.
Resolvendo os desafios nas terapias de RNA
A modificação química do RNA pode ser usada para proteger o RNA da degradação e melhorar a especificidade do alvo, diminuindo o risco de efeitos colaterais devido a efeitos fora do alvo. Além da modificação química, os veículos de entrega constituídos por nanomateriais podem ser usados para proteger o RNA da degradação e auxiliar no transporte da terapia ao alvo desejado.
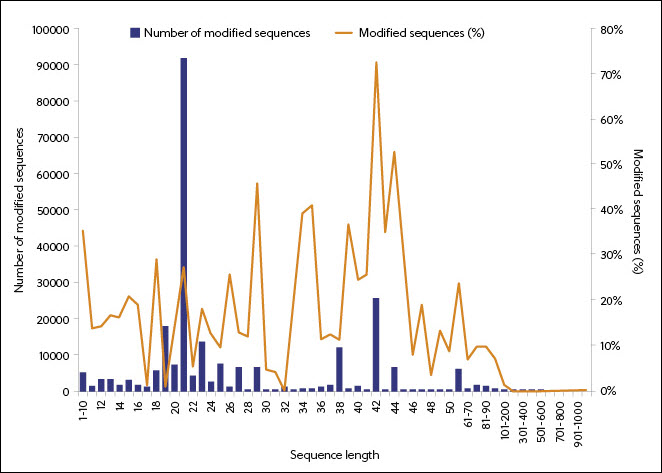
De acordo com os dados do CAS Content Collection, o uso da modificação de RNA começou a aumentar muito em 1995 e está associado a comprimentos de sequência menores (Figura 5). A predominância de RNAs de 18 a 27 nucleotídeos modificados reflete o uso desse comprimento de sequência em formas específicas de RNA (siRNAs e ASOs). O exame de modificações em medicamentos de RNA aprovados pela FDA confirma a correlação entre o tipo de RNA e suas modificações.
Modificações de base no RNA
Os nucleotídeos não canônicos com modificações que interferem na formação de ligações de hidrogênio podem desestabilizar termicamente a formação de um duplex com o alvo e, assim, melhorar a especificidade do alvo limitando a ligação fora dele. Além disso, a modificação pode melhorar o desempenho do RNA terapêutico. O uso da base modificada de N1-metilpseudouridina em mRNAs terapêuticos, como nas vacinas de mRNA para a Covid-19, melhora a tradução e diminui os efeitos colaterais citotóxicos e a resposta imune ao mRNA. As vacinas de mRNA, Comirnaty da Pfizer e Spikevax da Moderna, também usam tampas de 7-metilguanosina ligadas por um trifosfato 5' à extremidade 5' do mRNA, duplicando as tampas de mRNA encontradas na natureza que evitam a degradação da extremidade 5' do mRNA
Modificações na ribose
Modificações na posição 2’ da ribose no RNA podem aumentar a estabilidade e reduzir os efeitos fora do alvo. As modificações mais comuns na posição 2' incluem 2'-O-metil, 2'-fluoro, 2'-O-metoxietil (MOE) e 2'-amina.
Modificações de esqueleto
Modificações no grupo fosfato no esqueleto açúcar-fosfato podem melhorar a entrega de RNA ao neutralizar a carga negativa que pode interferir no transporte através das membranas e conferir maior resistência às nucleases, estendendo assim suas meias-vidas de eliminação de tecido. Uma das modificações de esqueleto mais utilizadas é o fosforotioato.
Pesquisa relacionada a nanocarreadores de RNA
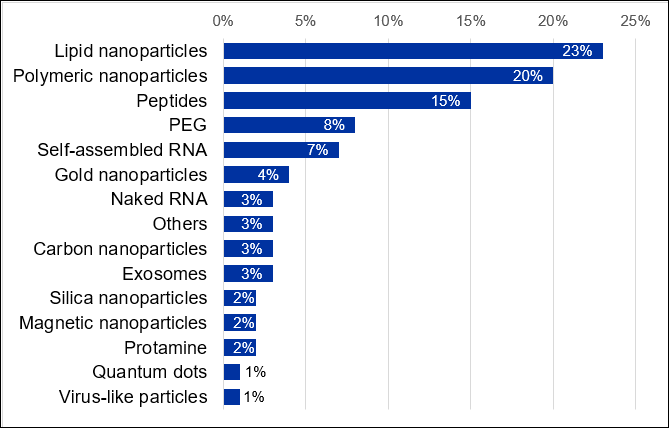
Embora as barreiras biológicas, como a imunogenicidade e a estabilidade da nuclease, sejam geralmente abordadas pela modificação da estrutura química do RNA, são necessários sistemas de entrega adicionais para superar outras barreiras no corpo. O encapsulamento de RNA em nanopartículas é uma maneira bem-sucedida de proteger e entregar RNA. Atualmente, existem cerca de 7.000 publicações científicas no CAS Content Collection relacionadas aos sistemas de entrega de RNA. Os estudos relacionados ao carreador de RNA são dominados pelas nanopartículas lipídicas, seguidas de perto pelos nanocarreadores poliméricos (Figura 6).
Conclusões
As terapias de RNA representam uma categoria de medicamentos em rápida expansão que deve mudar o padrão de tratamento para muitas doenças. Elas têm diversas vantagens em comparação com medicamentos tradicionais baseados em pequenas moléculas e moléculas biológicas, pois são de baixo custo, relativamente simples de fabricar e capazes de atingir locais anteriormente “não passíveis de tratamento”. Os desafios clássicos experimentados com sua estabilidade, entrega e efeitos fora do local podem ser eliminados ou reduzidos por meio de modificações químicas e nanocarreadores de RNA. Uma busca no CAS Content Collection destacou doenças infecciosas como a Covid-19 e o câncer como áreas terapêuticas-chave para RNAs e mostrou que a taxa de aumento dos volumes de publicação sobre circRNA, exossomo RNA, lncRNA e CRISPR são particularmente altas, com uma explosão atual notável na pesquisa relacionada ao CRISPR.
Ouça os especialistas
Para obter insights adicionais, assista o recente webinar da ACS para ver o que mais empolga os atuais líderes em terapias de RNA. Esse painel de discussão apresenta especialistas com os mais diversos históricos de pesquisa, dentre eles:
- Dr. John P. Cooke, Diretor Médico do Centro de terapias de RNA
- Dr. Robert DeLong, Professor associado do Centro de Inovação em Nanotecnologia na Universidade Estadual de Kansas
- Dr. Barb Ambrose, Cientista de Informações Sênior do CAS.
- Dr. Ramana Doppalapudi, Vice-presidente de Química da Avidity Biosciences
- Moderado pelo Dr. Gilles Georges, Vice-presidente e Diretor executivo científico do CAS