
No aniversário de um dos maiores e mais devastadores incidentes industriais já registrados, lembramos a tragédia de Beirute – uma explosão tão imensa que foi ouvida a 200 km de distância em Chipre. O epicentro da detonação foi em um armazém portuário e o combustível foi de 2.750 toneladas de nitrato de amônio
O nitrato de amônio é um dos fertilizantes mais utilizados, elemento importante de muitos outros compostos industriais, como explosivos de mineração, e usado como nutriente para a produção de antibióticos e leveduras. Como tantos outros produtos químicos usados em processos industriais, ele traz riscos que podem ser mitigados por meio de armazenamento seguro e procedimentos robustos de manuseio.
As investigações em Beirute ainda estão abertas, mas acredita-se que um incêndio começou em um armazém no porto e se espalhou para uma área onde o nitrato de amônio estava armazenado; um armazenamento sem segurança, perto de fogos de artifício e sem medidas de isolamento ou prevenção de incêndio, o que levou à sua explosão. Em segundos, este incidente matou mais de 200 pessoas, feriu mais de 5.000 e deixou cerca de 300.000 moradores desabrigados. Infelizmente, este evento não foi único, e explosões e incêndios causados por produtos químicos, como nitrato de amônio, são muito comuns. Em última análise, se uma substância pode liberar energia rapidamente, ela implica em um risco potencial de explosão ou incêndio. Mas, por que certos produtos químicos possuem essas características?
Ligações químicas fracas e produtos estáveis formam uma parceria explosiva
Se uma substância tiver ligações químicas fracas, principalmente se produzir produtos estáveis, é provável que represente um risco de incêndio ou explosão. Combustíveis, como a gasolina, queimam porque sua combustão produz substâncias estáveis com ligações químicas mais fortes; no caso da gasolina, esses produtos são o dióxido de carbono e a água. A gasolina requer calor ou uma fonte de ignição, como uma faísca ou chama, para queimar porque as ligações nos reagentes do combustível não são quebradas facilmente.
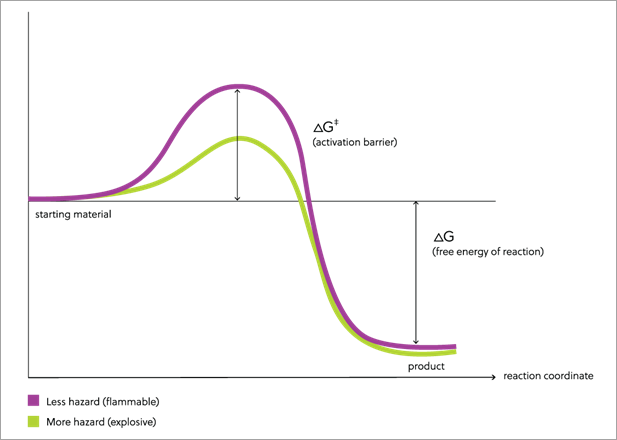
Por exemplo, a Figura 1 mostra um modelo conceitual para uma reação como a queima de gasolina. A linha roxa mostra como a energia livre muda durante uma reação de reagentes para produtos. Quando a gasolina queima, ela forma produtos estáveis (água e dióxido de carbono) contendo fortes ligações, liberando uma grande quantidade de energia no processo. Isso é mostrado na figura pela diferença de altura do ponto inicial à esquerda até o final da reação à direita. À medida que aumenta a diferença de energia livre entre os reagentes e os produtos, também aumenta a energia que pode ser liberada quando ocorre a reação.
Para passar dos reagentes aos produtos, no entanto, as moléculas devem ter energia suficiente para iniciar a reação. As reações geralmente começam quebrando ligações, e ligações fortes requerem quantidades substanciais de energia para serem quebradas. Assim, para que a reação de uma molécula estável comece, a reação deve receber uma grande quantidade de energia. Essa energia é chamada de energia de ativação e é mostrada pela altura da colina no meio da via de reação.
Uma vez superada a barreira, a reação ocorre. Como é grande a diferença de energia livre entre reagentes e produtos, a reação de uma molécula pode fornecer energia suficiente para ajudar outras moléculas a superar a barreira de ativação. A reação pode então acelerar e ser difícil de parar até que os reagentes sejam consumidos. Depois que começa um incêndio com gasolina, é difícil extingui-lo. Além disso, como os produtos são gasosos (dióxido de carbono e vapor), os produtos ocupam muito mais espaço do que os reagentes. A expansão do volume transfere energia ao entorno; se a reação ocorrer em um espaço fechado, pode ocorrer uma explosão. Como é necessária muita energia para que a gasolina queime, é mais fácil evitar ações que forneçam essa energia e, portanto, mais fácil prevenir incêndios.
Reveja exemplos de produtos químicos explosivos aqui e, para segurança química adicional ou recursos de substâncias, confira a Biblioteca de Segurança Química e o Commom Chemistry do CAS.
Outras substâncias oferecem riscos maiores. Muitas delas contêm ligações químicas fracas. A Figura 1 (linha verde) também mostra um modelo para uma reação como a combustão de uma molécula contendo uma ligação fraca. Como a gasolina, a diferença de energia livre (como mostrado pela diferença de altura) entre os reagentes à esquerda e os produtos à direita é grande; os produtos contêm ligações fortes e a reação libera uma grande quantidade de energia quando ocorre. A altura da barreira para esta reação, no entanto, é muito menor do que para a combustão da gasolina.
As reações geralmente começam com a quebra de uma ligação, e a presença de uma ligação fraca fornece um lugar fácil para uma reação começar. Uma vez que a ligação é quebrada, a reação pode então acontecer. Quando os produtos são muito mais baixos em energia do que os reagentes, como neste caso, a reação de uma molécula pode liberar energia para fazer com que outras moléculas reajam. E, como a barreira à reação é menor, mais moléculas podem ser induzidas a reagir a partir da reação de uma molécula da substância na Figura 1 (verde) do que da reação de uma molécula da substância na Figura 1 (roxo). A presença da ligação fraca significa que a reação, uma vez iniciada, acelera rapidamente. Se os produtos forem gases, eles também vão transferir energia ao entorno; se a reação for suficientemente rápida, pode ocorrer uma explosão ou detonação. A barreira mais baixa à reação de uma substância que contém uma ligação fraca significa que ela consome menos energia para iniciar sua reação e, portanto, as maneiras pelas quais ela pode ser manipulada são mais limitadas. Em alguns casos, a reação pode começar com um impacto, fricção ou faísca, e, portanto, o manuseio de tais substâncias requer muito mais cuidado para evitar incêndio ou explosão.
As azidas (RN3) ilustram perfeitamente este ponto. Essas substâncias contêm três átomos de nitrogênio conectados com ligações de força desigual. Os átomos de nitrogênio podem formar ligações fortes – a ligação tripla entre os átomos de nitrogênio no gás nitrogênio molecular (N2) é uma das ligações químicas conhecidas mais fortes; no entanto, os átomos de nitrogênio também podem formar ligações simples e duplas, que são consideravelmente mais fracas. Uma das ligações nitrogênio-nitrogênio na azida é fraca e não requer muita energia para quebrar, levando a uma rápida decomposição que produz N₂. Como a ligação nitrogênio-nitrogênio no N2 é muito mais estável que as ligações nitrogênio-nitrogênio na azida reagente, essa decomposição libera grandes quantidades de energia.
As azidas inorgânicas e orgânicas têm sensibilidades variadas. A azida de sódio inorgânica pode ser manuseada com segurança em condições cotidianas, mas é empregada como um gerador de gás rápido em airbags de veículos, enquanto as azidas de metais pesados altamente voláteis, como a azida de chumbo, são usadas como iniciadores de explosivos. As azidas orgânicas são comumente usadas na síntese de produtos químicos mais complexos, incluindo produtos farmacêuticos e polímeros. Azidas orgânicas com baixo peso molecular ou altas proporções atômicas de nitrogênio (N) para carbono (C) podem ser explosivas e houve vários incidentes relatados de explosões de laboratório devido à formação de azidas de baixo peso molecular a partir de reações entre azidas inorgânicas e diclorometano . Um aminoácido modificado com azida usado para a preparação de proteínas modificadas também foi considerado explosivo.
Os peróxidos (ROOR) são outra classe de moléculas com características potencialmente explosivas. Os peróxidos contêm ligações fracas de oxigênio-oxigênio; quando essas ligações quebram, os peróxidos produzem intermediários radicais (radicais livres) que são úteis em reações químicas. Os radicais intermediários são particularmente úteis para iniciar a polimerização e são comumente detectados como intermediários na combustão; mesmo pequenas quantidades de radicais podem atuar como catalisadores e, em alguns casos, catalisam sua própria formação. Os peróxidos também se fragmentam para produzir oxigênio molecular (O₂); enquanto a ligação simples oxigênio-oxigênio é fraca, a ligação dupla oxigênio-oxigênio no O2 é forte, então essa fragmentação libera energia.
A fraca ligação oxigênio-oxigênio significa que os peróxidos podem se decompor facilmente, liberando radicais livres e O₂, uma combinação volátil e explosiva, principalmente quando concentrados. Foram relatados vários incêndios significativos em instalações químicas que trabalham com peróxidos, incluindo um no Texas, EUA, quando o furacão Harvey e inundações sem precedentes causaram falhas nos mecanismos de segurança. Os peróxidos também podem se formar espontaneamente a partir da exposição de éteres ao oxigênio. Esses peróxidos formam cristais que podem explodir quando submetidos a choque físico, fricção ou reação com certos metais. Normalmente, os éteres são formulados com pequenas quantidades de inibidores como o BHT (hidroxitolueno butilado, usado como conservante) para evitar a formação de peróxidos. Os inibidores são consumidos pelo oxigênio. Caso os éteres sejam mantidos por longos períodos de tempo na presença de oxigênio, estarão suscetíveis à formação de peróxido.
O flamejante desejo de se tornar estável
Outras substâncias têm ligações que, embora apresentem alguma dificuldade de se romper por conta própria, podem reagir facilmente sob certas condições para formar produtos muito mais estáveis. À medida que são formadas novas ligações, a energia é liberada como calor, podendo causar incêndios ou explosões. Por exemplo, alquilas metálicas são usadas como catalisadores na síntese de uma ampla gama de produtos químicos e materiais, mas geralmente são pirofóricas, queimando facilmente em contato com o ar.
O trimetilalumínio, em particular, reage com o ar ou a água para produzir produtos com ligações alumínio-oxigênio altamente estáveis, acarretando incêndios e explosões.
Os acrilatos são usados para polimerização em escala industrial; cada monômero de acrilato substitui sua ligação dupla por uma ligação simples adicional à medida que é incorporado à cadeia do polímero. Essa nova ligação é mais forte que a força cumulativa da ligação dupla, de modo que a reação de polimerização libera energia. Com frequência, a polimerização de acrilatos e outros alcenos é realizada usando iniciadores radicais como peróxidos para acionar as reações de polimerização, usando a mesma reatividade que em outras circunstâncias levaria à sua explosão. Em câmaras de polimerização em larga escala, quando a razão área de superfície para volume é muito baixa para dissipar o calor formado e quando os inibidores de polimerização descontrolada são consumidos, inativados ou removidos, os acrilatos podem polimerizar de forma explosiva.
Da mesma forma, solventes como dimetilsulfóxido (DMSO) podem reagir com uma variedade de substâncias, como ácidos, bases e eletrófilos, para reduzir as temperaturas de decomposição; reações mesmo em temperaturas mais baixas e aparentemente seguras ainda podem levar a uma explosão.
Aproveitando o grande facilitador do mundo moderno
Em seu centro, a química é possibilitada por mudanças de energia e, durante séculos, os humanos aproveitaram e exploraram essa energia para viajar pelo mundo, impulsionar a indústria e produzir a própria comida de nossas mesas, as roupas que usamos e as estruturas de nossas cidades. Ansiamos por produtos químicos explosivos e voláteis por sua energia e, ainda assim, sua potência pode ter consequências inesperadas e devastadoras. Ao entender como canalizar essa energia de maneira construtiva e identificar melhor as condições em que os produtos químicos reagem de maneira inesperada e prejudicial, podemos prever incidentes explosivos antes que aconteçam e descobrir como evitá-los.
Para obter mais informações sobre nitrato de amônio, seus perigos e regras de segurança, baixe nosso relatório completo do CAS Insights e assista ao nosso webinar que reúne os principais especialistas que discutirão as opções de formulação e o cenário da inovação.



