肠道微生物组:像人体的一个附加器官一样发挥作用
人体内有大量微生物——主要为细菌,但也有病毒、原生动物、真菌和古菌。 它们被统称为“微生物组”。 肠道微生物群、肠道菌群或微生物组是生活在人类和其他动物消化道中的微生物。 虽然有些细菌与疾病相关,但另一些细菌对健康的许多方面都尤为重要。 事实上,人体内的细菌细胞数量比人类本身的细胞还要多——大约40万亿个细菌细胞,而人类细胞只有30万亿个。 这些微生物的总重大概与大脑差不多。 它们像人体的一个附加器官一样,共同对人体健康发挥着巨大作用。 肠道微生物组的基因组总量是人体DNA总量的100多倍。 考虑到微生物群的巨大潜力,可以预期它在人体几乎所有的生理过程中都发挥作用。 肠道细菌与几种精神疾病有关,患有抑郁症、双相情感障碍、精神分裂症和自闭症等各种精神疾病的患者的肠道微生物的组成发生了显著变化。
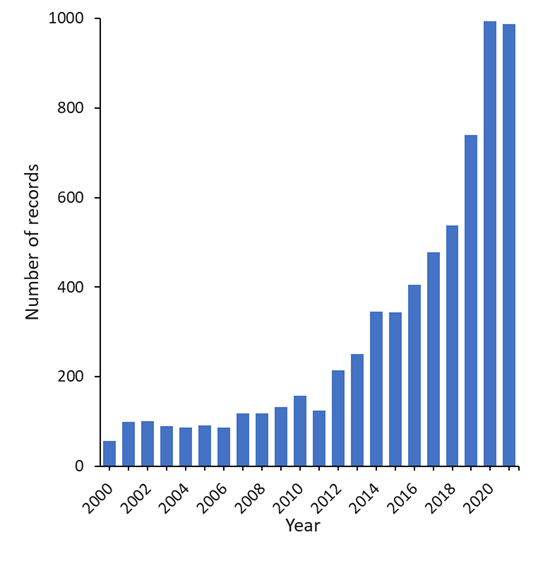
在CAS 内容合集TM 中的检索结果表明,自2000年以来,人们对与人类健康,特别是与心理健康相关的肠道微生物组的研究兴趣呈指数级增长。 目前,有7000多篇报道了肠道微生物组与心理健康相关的出版物(图1)。
婴儿出生即获得了第一剂微生物 人类肠道微生物组的发育
普遍认为子宫是一个无菌环境,细菌从新生儿出生时开始定植。 新生儿的微生物组因分娩方式而异:阴道分娩的婴儿的微生物组与母体阴道微生物组相似,剖宫产分娩的婴儿的微生物组与母体皮肤微生物组相似。 其他影响新生儿微生物组发育的各种因素,包括早产和喂养方式等。 在整个成年期,肠道微生物组组成的主要决定因素似乎是饮食。 随着饮食摄入的变化,微生物组的组成发生了快速变化。 以植物为基础的饮食与以动物为基础的饮食对应的微生物组的特征模式明显不同。 肠道微生物组的发育和改变也受到多种其他因素的影响。 在 CAS 内容合集中的检索结果,心理压力是影响肠道微生物组组成的第二大重要因素(仅次于饮食)。 其他因素还包括:分娩方式和婴儿喂养方式、环境条件、药物、生命周期的阶段和模式、共病和医疗程序(图2) 。 由微生物群功能组成和代谢活动的失衡、或其局部分布的改变引起的微生物群稳态的破坏被称为失调,表明人体微生物环境的失衡或适应不良。

考虑到目前公认的饮食对肠道微生物组组成的重要作用,以及肠道微生物组对健康的重要影响,极具价值的问题仍然是:为了保持我们肠道细菌的健康,哪种饮食是值得推荐的? 虽然还没有明确的答案指出哪些食物可以作为专门的疾病疗法,但一些主要的指导建议已经制定出来了。 高纤维饮食尤其会影响肠道微生物群。 膳食纤维只能被结肠中微生物群产生的酶消化和发酵。 发酵会释放短链脂肪酸,从而降低结肠的pH值。 高酸性环境决定了能够存活的微生物群的类型。 较低的pH值限制了某些有害细菌的生长,如艰难梭状芽胞杆菌(Clostridium difficile)。 菊粉、淀粉、树胶、果胶和低聚果糖等高纤维食物,已经成为众所周知的益生元,因为它们为人体的有益微生物群提供底物。 一般来说,水果、蔬菜、豆类以及小麦、燕麦、大麦等全麦食品中都含有大量的益生元纤维。 另一类非常有益的食物是含有益生菌的食物;益生菌是对消化系统有益的活细菌,还可能会进一步改善我们的肠道微生物组。 含有益生菌的食品包括发酵食品(如开菲尔)、含有活性菌的酸奶、泡菜、康普茶、泡菜、味增和泡菜。
肠道微生物群的组成细菌
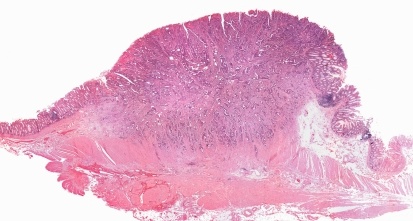
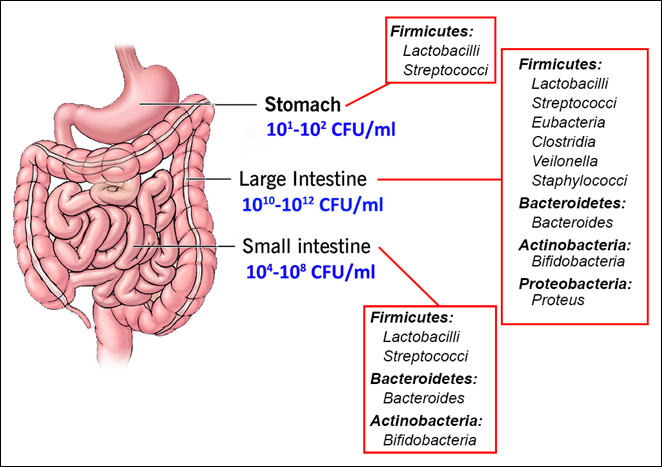
人类肠道微生物群可分为许多门类, 主要由厚壁菌门、拟杆菌门、放线菌门和变形菌门四门组成,其中厚壁菌门和拟杆菌门占肠道微生物群的 90%。 大多数细菌存活在胃肠道中,厌氧菌主要存活在大肠中(图 3)。
脑肠轴——肠道微生物组被称为“第二大脑”
如今已经很确定的是:肠道和大脑处于不断的双向沟通中,微生物群及其代谢产物发挥着主要作用。 迈克尔·格尔森(Michael Gershon)在他1999年出版的新书中,将消化系统称为“第二个大脑”;同时,科学家们开始意识到,人类的肠道和大脑之间存在着不断的对话,肠道微生物显著地调节着大脑功能。
现在,人们普遍认为,肠道微生物群通过神经、内分泌和免疫途径与中枢神经系统通信,从而控制大脑功能。 研究表明,肠道微生物群在调节焦虑、情绪、认知和疼痛方面发挥着重要作用。 因此,新概念“脑肠轴(微生物群-肠道-大脑轴)”的诞生也表明,调节肠道微生物群可能是开发中枢神经系统疾病新疗法的有效策略。
肠道微生物群与COVID-19
最近有报道称, COVID-19 患者肠道微生物群组成与细胞因子和炎症标志物水平之间存在相关性。 这提示了肠道微生物组通过调节宿主免疫反应影响了COVID-19患病的严重程度。 此外,即使在病症缓解后,肠道微生物群失调也可能导致症状持续,这使我们需要了解肠道微生物是如何参与炎症和COVID-19病症的。
肠道微生物神经活性代谢产物
脑肠轴异常已成为神经疾病病理生理学的关键因素,因此越来越多的研究致力于了解肠道微生物代谢产物的神经活性潜力。 我们来了解如下主要的神经活性肠道微生物代谢产物:
神经递质
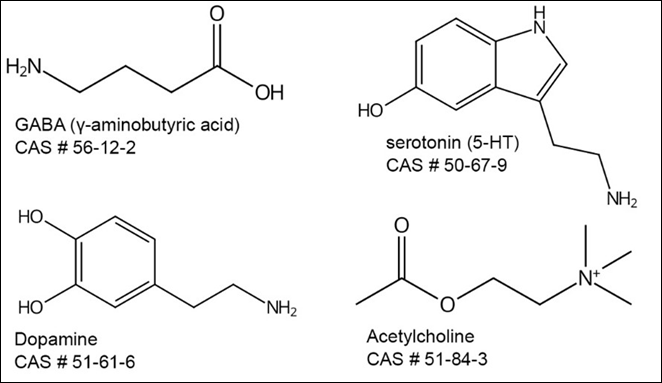
肠道微生物组产生调节大脑活动的神经递质。 大多数中枢神经系统的神经递质也存在于胃肠道中,在那里它们发挥局部效用,如调节肠道运动、分泌和细胞信号传导。 肠道微生物群的成员可以合成神经递质,如乳酸杆菌和双歧杆菌产生GABA;大肠杆菌产生血清素和多巴胺;乳酸杆菌产生乙酰胆碱(图4)。 它们通过迷走神经向大脑发送信号。
短链脂肪酸
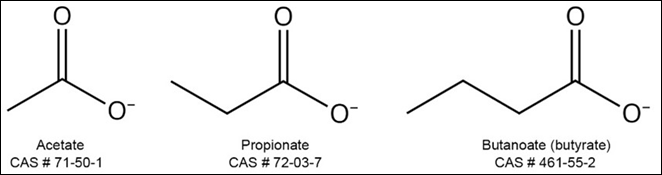
短链脂肪酸,是在由盲肠和结肠中的细菌利用膳食碳水化合物作为底物,进行厌氧发酵产生的小分子有机化合物。短链脂肪酸很容易被大肠吸收。 短链脂肪酸参与消化、免疫和中枢神经系统功能,尽管对其影响存在不同的观点。 肠道微生物产生的三种含量最高的短链脂肪酸是乙酸、丁酸和丙酸(图5)。 已有实验证明,小鼠服用短链脂肪酸后其抑郁症状有所缓解。 发酵膳食纤维产生短链脂肪酸的革兰氏阳性厌氧菌是粪杆菌和粪球菌。 粪杆菌是一种肠道中含量丰富的微生物,对包括抑郁症在内的多种疾病具有重要的免疫作用和临床意义。
色氨酸代谢产物
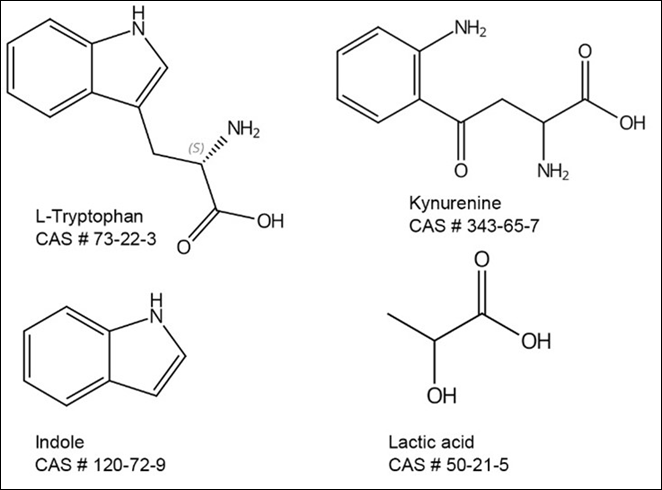
色氨酸是参与蛋白质合成的一种必需氨基酸。 它被细菌酶(色氨酸酶)代谢分解,产生具有既定情绪调节特性的神经活性分子,包括血清素、犬尿氨酸和吲哚(图6)。 人们发现,膳食中摄入色氨酸可以调节人类中枢神经系统的血清素浓度,而色氨酸的耗竭则会导致抑郁症的加重。
乳酸
乳酸(图6)是一种主要由乳酸菌(如乳酸乳杆菌、加氏乳杆菌和罗伊氏乳杆菌)、双歧杆菌和变形杆菌发酵产生的有机酸。 乳酸可以被几种细菌转化为短链脂肪酸,从而形成短链脂肪酸库。 乳酸被血液吸收,可以穿过血脑屏障。 乳酸在大脑中枢神经系统信号传导中具有重要作用。 因为其代谢为谷氨酸的能力,它被神经元用作能量底物。 它也有助于突触的可塑性和触发记忆的发展。
维生素
肠道中的大多数细菌,如乳酸菌和双歧杆菌,合成维生素(特别是维生素B和维生素K),作为其在大肠中的代谢的一部分。 人类依靠肠道微生物群来产生维生素。 维生素是关键的微量营养素,在人体中(包括大脑)的多种生理过程中发挥着作用。 活跃的转运体将它们带过血脑屏障。 在中枢神经系统中,维生素的作用广泛,从能量稳态扩展到神经递质的产生中都发挥着作用。 维生素缺乏会对神经功能产生显著的负面影响。 叶酸(维生素B9)是一种微生物来源的维生素,其与抑郁症的病理学密切相关。
肠道微生物组的应用前景
最近的一项创新的研究性疗法是将粪便微生物群移植,并已经在临床试验中进行了测试,非常具有治疗前景。 在过去的5年里,CAS内容合集每年收录约1000余篇与粪便移植相关的文献。 例如,据报道,粪便微生物群移植能够解决 80-90% 由对抗生素无反应的复发性艰难梭菌引起的感染。 粪便微生物群移植作为一系列疾病的潜在治疗手段急待探究,其临床试验的独特作用也正被越来越多地研究。
目前,通过胃肠道微生物群调节肠脑轴的研究是一门新兴的创新前沿科学。 大部分可用数据是基于基础科学或动物模型,可能无法适用于有效的人类干预。 因此,特定的益生元化合物和益生菌的个体化处方,代表了理想的、个性化的营养方式和生活方式。 人们仍然对个体化处方充满希望。正在进行的进一步确定微生物组的功能和宿主-微生物的互作机制的努力,将使人们更好地了解微生物组在健康和疾病中的作用。
欢迎阅读我们近期的文章抑郁症和创伤后应激障碍(PTSD)的新希望,了解更多新兴趋势和疗法如何帮助抑郁症、焦虑症和创伤后应激障碍患者。