
En este aniversario de uno de los incidentes industriales más graves y devastadores que se han registrado, recordamos la tragedia de Beirut, una explosión tan brutal que se oyó desde Chipre, a 200 km de distancia. El epicentro de la detonación se situó en un almacén del puerto en el que se almacenaban 2750 toneladas de nitrato de amonio que sirvieron como combustible.
El nitrato de amonio es uno de los fertilizantes más usados, un elemento importante de muchos otros compuestos industriales, como los explosivos de minería, y un nutriente empleado para producir antibióticos y levadura. Al igual que otras muchas sustancias químicas utilizadas en procesos industriales, conlleva riesgos que se pueden mitigar mediante un almacenamiento seguro y unos procedimientos de manipulación controlados.
Las investigaciones sobre el accidente de Beirut siguen abiertas, pero se cree que se declaró un incendio en un almacén del puerto y se propagó a un área en la que se almacenaba nitrato de amonio. Un almacenamiento no seguro sin medidas de aislamiento o de prevención de incendios provocó la explosión. En cuestión de segundos, el incidente mató a más de 200 personas, hirió a más de 5000 y dejó sin hogar a unos 300 000 residentes. Lamentablemente, este suceso no ha sido un caso único, y los incendios y explosiones causados por sustancias químicas, como el nitrato de amonio, son demasiado frecuentes. En esencia, si una sustancia puede liberar energía con rapidez, presenta riesgo de explosión o de incendio. ¿Pero por qué poseen estas características algunas sustancias químicas?
Los enlaces químicos débiles y los productos estables son una combinación explosiva
Si una sustancia tiene enlaces químicos débiles, en especial si genera productos estables, es probable que presente riesgo de incendio o explosión. Los combustibles, como la gasolina, arden porque su combustión produce sustancias estables con enlaces químicos más fuertes. En el caso de la gasolina, estos productos son el dióxido de carbono y el agua. La gasolina necesita calor o una fuente de ignición, como una chispa o una llama, porque los enlaces de los reactivos del combustible no se rompen fácilmente.
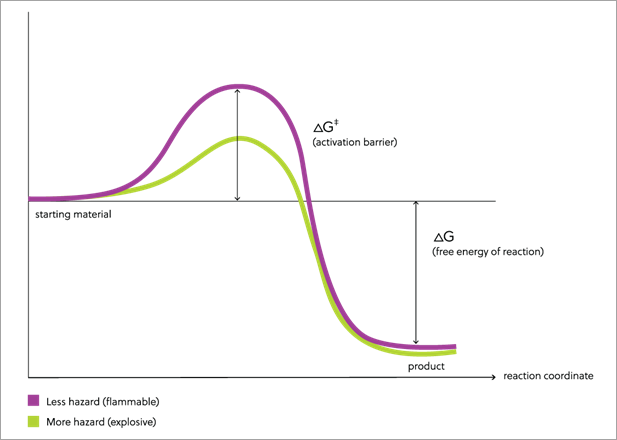
Por ejemplo, la figura 1 muestra un modelo conceptual de una reacción como la combustión de gasolina. La línea morada describe cómo cambia la energía libre durante la reacción que convierte los reactivos en productos. Cuando la gasolina se inflama, forma productos estables (agua y dióxido de carbono) que contienen enlaces fuertes y libera una gran cantidad de energía. En la figura, esto se refleja en la diferencia de altura entre el punto inicial de la izquierda y el final de la reacción, visible a la derecha. A medida que aumenta la diferencia de energía libre entre los reactivos y los productos, la energía que se puede liberar en la reacción también aumenta.
Para llegar de los reactivos a los productos, sin embargo, las moléculas deben tener suficiente energía para iniciar la reacción. A menudo, las reacciones comienzan con la rotura de los enlaces, y los enlaces fuertes necesitan una cantidad considerable de energía para romperse. Así, para que comience la reacción de una molécula estable, se tiene que suministrar una gran cantidad de energía a la reacción. Esta energía se denomina "barrera de activación" y está representada por la altura de la colina en el punto medio de la ruta de la reacción.
Una vez superada la barrera, se puede producir la reacción. Como la diferencia de energía libre entre los reactivos y los productos es grande, la reacción de una molécula puede proporcionar suficiente energía para ayudar a otras moléculas a superar la barrera de activación. De este modo, la reacción se puede acelerar y será difícil detenerla hasta que se hayan agotado los reactivos. Una vez que comienza un incendio con gasolina, puede ser difícil extinguirlo. Además, como los productos son gaseosos (dióxido de carbono y vapor), ocupan mucho más espacio que los reactivos. La expansión del volumen transfiere energía al entorno. Si la reacción tiene lugar en un espacio cerrado, puede producirse una explosión. Como hace falta más energía para lograr que la gasolina se inflame, es fácil evitar las reacciones que suministran esa energía y, por tanto, resulta más sencillo prevenir los incendios.
Puede encontrar ejemplos de sustancias químicas explosivas aquí. Para ver otros recursos sobre sustancias o seguridad química, consulte la Chemical Safety Library y CAS Common Chemistry.
Otras sustancias presentan riesgos mayores. Muchas de ellas contienen enlaces químicos débiles. La figura 1 (línea verde) también muestra un modelo de una reacción como la combustión de una molécula que contiene un enlace débil. Al igual que en el caso de la gasolina, la diferencia de energía libre (representada por la diferencia de altura) entre los reactivos de la izquierda y los productos de la derecha es grande. Los productos contienen enlaces fuertes y la reacción libera una gran cantidad de energía cuando se produce. Sin embargo, en esta reacción la altura de la barrera es mucho menor que en la combustión de la gasolina.
A menudo, las reacciones empiezan con la rotura de un enlace, y la presencia de un enlace débil proporciona un punto en el que es fácil que comience la reacción. Una vez que se rompe el enlace, la reacción puede seguir su curso hasta que se completa. Cuando los productos tienen mucha menos energía que los reactivos, como en este caso, la reacción de una molécula puede liberar energía que hace que otras moléculas reaccionen. Como la barrera de la reacción es más baja, la reacción de una molécula de la sustancia representada por la línea verde en la figura 1 (verde) puede hacer que reaccionen más moléculas que una sola molécula de la sustancia representada por la línea morada de la figura 1. La presencia del enlace débil significa que la reacción, una vez iniciada, puede acelerarse rápidamente. Si los productos son gases, transferirán trabajo a su entorno y, si la reacción es lo bastante rápida, puede producirse una explosión o una detonación. Una barrera de reacción más baja en una sustancia que contiene un enlace débil significa que hace falta menos energía para poner en marcha esa reacción y, por consiguiente, las formas de controlarla son más limitadas. En algunos casos, el impacto, la fricción o las chispas que se producen al manipularla bastan para iniciar la reacción y, por ello, el manejo de esas sustancias requiere mucho más cuidado para prevenir los incendios y las explosiones.
Las azidas (RN3) son un buen ejemplo de esto. Estas sustancias contienen tres átomos de nitrógeno conectados por enlaces con diferentes fuerzas. Los átomos de nitrógeno pueden formar enlaces fuertes: el enlace triple entre los átomos de nitrógeno en el gas de nitrógeno molecular (N2) es uno de los enlaces químicos más fuertes que se conocen. Sin embargo, los átomos de nitrógeno también pueden formar enlaces simples y dobles, que son bastante más débiles. Uno de los enlaces nitrógeno-nitrógeno de la azida es débil y no necesita mucha energía para romperse, lo que provoca una descomposición rápida que produce N₂. Como el enlace nitrógeno-nitrógeno del N2 es mucho más estable que los enlaces nitrógeno-nitrógeno de la azida utilizada como reactivo, esta descomposición libera grandes cantidades de energía.
Las azidas inorgánicas y orgánicas tienen distintas sensibilidades. La azida de sodio inorgánica se puede manipular de forma segura en condiciones normales, pero se usa como generador rápido de gas en los airbags de los vehículos, mientras que las azidas de metales pesados como la azida de plomo, que son muy volátiles, se utilizan como iniciadores en explosivos. Las azidas orgánicas se suelen usar en la síntesis de sustancias químicas más complejas, como algunos productos farmacéuticos y polímeros. Las azidas orgánicas con un peso molecular bajo o con relaciones atómicas altas entre nitrógeno (N) y carbono (C) pueden ser explosivas, y se han documentado varios incidentes de explosiones en laboratorios debidas a la formación de azidas de bajo peso molecular por reacciones entre azidas inorgánicas y diclorometano. Un aminoácido modificado con azida que se usa para la preparación de proteínas modificadas también resultó explosivo.
Los peróxidos (ROOR) son otra clase de moléculas con características potencialmente explosivas. Los peróxidos contienen enlaces oxígeno-oxígeno débiles. Cuando estos enlaces se rompen, los peróxidos generan términos intermedios radicales (radicales libres) que son útiles en las reacciones químicas. Los intermedios radicales son especialmente útiles para iniciar la polimerización y se han detectado en muchos casos como términos intermedios de la combustión. Incluso una pequeña cantidad de radicales puede actuar como catalizadora y, en algunos casos, catalizan su propia formación. Los peróxidos también se fragmentan para producir oxígeno molecular (O₂). Mientras que el enlace simple oxígeno-oxígeno es débil, el enlace doble oxígeno-oxígeno del O2 es fuerte, de modo que esta fragmentación libera energía.
El enlace oxígeno-oxígeno débil significa que los peróxidos se pueden descomponer fácilmente liberando radicales libres y O₂, una combinación volátil y explosiva, en especial cuando está concentrada. Se han documentado incendios graves en instalaciones químicas que trabajan con peróxidos, incluida una de Texas, en Estados Unidos, cuando el huracán Harvey y una inundación sin precedentes provocaron un fallo de los mecanismos de seguridad. Los peróxidos se forman también espontáneamente al exponer éteres al oxígeno. Estos peróxidos forman cristales que pueden explotar cuando se someten a sacudidas físicas, fricción o reacciones con algunos metales. Los éteres se formulan normalmente con pequeñas cantidades de inhibidores como el BHT (hidroxitolueno butilado, empleado como conservante) para evitar la formación de peróxidos. Los inhibidores son consumidos por el oxígeno. Si los éteres permanecen periodos largos de tiempo en presencia de oxígeno, se pueden formar peróxidos.
La imperiosa necesidad de alcanzar la estabilidad
Otras sustancias tienen enlaces que, aunque no se rompen fácilmente por sí solos, pueden reaccionar con facilidad en ciertas condiciones para generar productos que son mucho más estables. A medida que se forman nuevos enlaces, se libera energía que puede producir calor, incendios o explosiones. Por ejemplo, los alquilos metálicos se usan como catalizadores en la síntesis de una amplia gama de sustancias químicas y materiales, pero son en muchos casos pirofóricos, lo que quiere decir que se inflaman fácilmente en contacto con el aire.
El trimetilaluminio, en particular, reacciona con el aire o con el agua para generar productos con enlaces aluminio-oxígeno muy estables, lo que provoca incendios y explosiones.
Los acrilatos se usan para la polimerización a escala industrial. Cada monómero de acrilato reemplaza su enlace doble por otro enlace simple al incorporarse a la cadena polimérica. Este nuevo enlace es más fuerte que la fuerza combinada del enlace doble, de manera que la reacción de polimerización genera energía. La polimerización de los acrilatos y otros alquenos se produce en muchos casos usando iniciadores radicales como los peróxidos para iniciar reacciones de polimerización, recurriendo así a la misma reactividad que en otras circunstancias provoca su explosión. En las cámaras de polimerización a gran escala, cuando la proporción entre el área superficial y el volumen es demasiado baja para disipar el calor formado y cuando los inhibidores de la polimerización incontrolada se han consumido, inactivado o eliminado, los acrilatos se pueden polimerizar de manera explosiva.
Del mismo modo, disolventes como el dimetilsulfóxido (DMSO) pueden reaccionar con una amplia gama de sustancias, como ácidos, bases y electrófilos, para reducir las temperaturas de descomposición. Incluso a temperaturas más bajas, aparentemente seguras, estas reacciones pueden provocar explosiones.
Controlar el gran motor del mundo moderno
En esencia, la química es posible gracias a los cambios energéticos. Durante siglos, los humanos han controlado y explotado esta energía para recorrer el mundo, impulsar la industria y producir los alimentos que servimos en la mesa, las prendas con las que nos cubrimos y las estructuras de nuestras ciudades. Las sustancias químicas explosivas y volátiles son codiciadas por su energía, pero esta potencia puede tener consecuencias inesperadas y devastadoras. Entender cómo se puede canalizar esta energía de formas constructivas e identificar mejor las condiciones en las que las sustancias químicas pueden reaccionar de maneras inesperadas y perjudiciales nos ayudará a prever los incidentes explosivos antes de que se produzcan y a aprender a prevenirlos.
Para obtener más información sobre el nitrato de amonio, sus riesgos y sus normas de seguridad, descargue el informe de CAS Insights completo y vea el seminario web, en el que varios expertos destacados hablan sobre las opciones de formulación y el panorama de la innovación.

