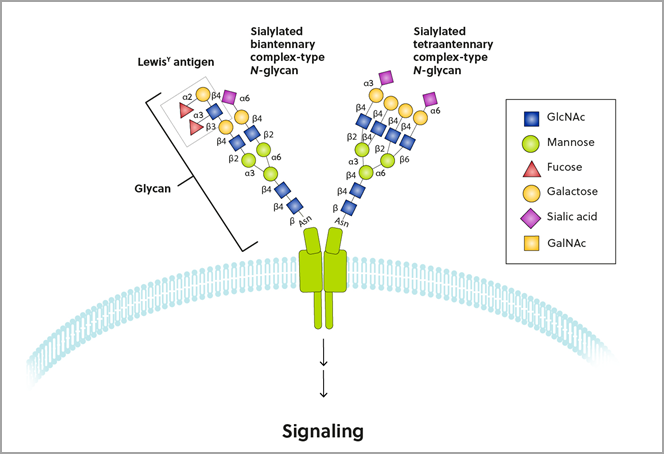
糖は、細胞内の正常な生理学的プロセスにとって極めて重要であるだけでなく、病理学的プロセスにおいても重要な役割を果たします。 バクテリアやウイルスなどは、糖を識別して宿主を感染させるということさえ行っています。 糖鎖生物学の分野は依然として分かりにくい研究テーマではあるものの、近年さまざまな分野の研究者から多くの関心を集めるようになっています。 このツールのひとつが生体直交化学です。これはタンパク質やペプチドと結合した炭水化物構造、グリカンのイメージングに利用できます(図1)。
最近、生体直交化学の分野を長年けん引してきたキャロリン・ベルトッジ氏の研究グループが、生体直交化学を用いて新しい生体分子である糖鎖RNAに関する驚くべき発見をしています。 ここでは、生体直交化学の世界とその応用について、特に糖鎖生物学の分野の前進にどう貢献したか、そして今後どのような機会が待ち受けているかについて詳しく説明します。
生体直交化学とは
生体直交化学という用語は、長年この分野をけん引してきたベルトッジ氏の研究グループにより作られたものです。 生体直交化学とは、生体分子への影響や生化学的プロセスへの干渉を最小限に抑えながら、生物学的環境で発生させる一連の反応のことを指します。 生体直交化学のプロセスは、生体内で発生するのに必要とされるものと同じ厳格な条件の下行われます。
- 反応は、生理環境の温度とpHで発生しなければならない。
- 反応による生成物は、選択的かつ高収率で得られる必要があり、また水や内因性求核試薬、求電子試薬、還元剤または複雑な生物環境で見られる酸化体による影響を受けてはならない。
- 反応は、低濃度でも迅速でなければならず、そして安定して反応生成物を生成する必要がある。
- 反応には、生体系には自然に存在しない官能基が関係している必要がある。
生体直交化学の用途
CASコンテンツ・コレクションTMを使って、2010年から2020年までの生体直交化学の応用に関する出版動向を分析することができました(図2)。 その結果、2010年から2020年にかけて生体直交化学で最も利用されたのはイメージングであり、創薬と薬物送達がそれに続くことが分かりました。
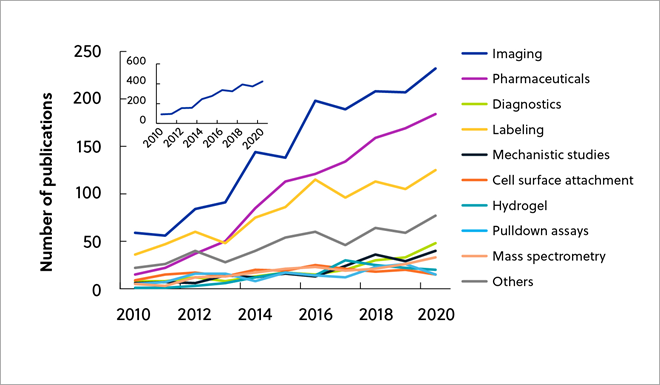
(* 2010年が初期基準点として選択されたのは、「生体直交化学」という用語が記載された文献が前年に比べて大幅に増加した最初の年であるため。 生体直交化学を意味する「bioorthogonal」または「bio-orthogonal」という用語を含む総文献数のうち、その約90%は2010年以降に公開されている。)
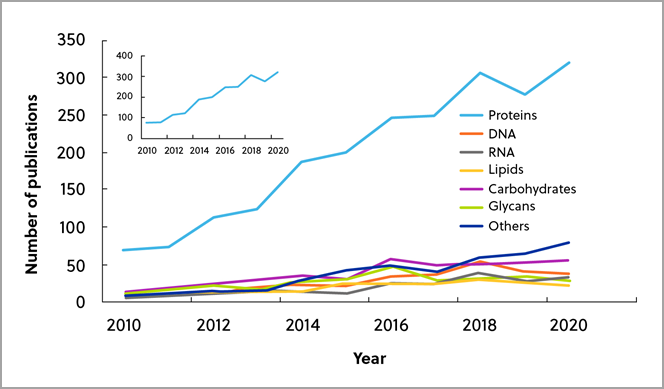
さらに、その出版物のうち最も多くなっているのは、タンパク質の生体直交化学関連です。これはその手法が現在最も確立されているためであると考えられます。なお、比較的新しいグリカン分野など、他の分野も着実に増加傾向にあります(図3)。
グリカンのイメージング
生体直交化学は、グリカンの構造や局在化そして生物学的機能を理解する上で不可欠なツールであることが証明されています。 グリカンは、細胞壁に一般的に見られるペプチドやタンパク質そして脂質などと結合したオリゴ糖で、そのため細胞型を選択的に視覚化するのに利用できます。 グリカンの代謝前駆体には、アジ化物や末端アルキンそして歪みアルキンなど、多くの生体直交機能が含まれます。 グリカンは、適切な生体直交パートナーを使用することで視覚化できます。たとえばアジ化物はホスフィン含有エステルやチオエステルをシュタウディンガーまたはトレースレス シュタウディンガー ライゲーションによって、また末端アルキンや歪みアルキンは、それぞれCuAACまたはSPAACを使用して識別されます。
糖鎖生物学を前進させる生体直交化学
これまでRNAは、グリコシル化の主要な標的ではありませんでした。 そんな中、代謝標識と生体直交化学のお陰で実現できた重要な最近の発見として「糖鎖RNA」があります。 ベルトッジ氏の研究グループを率いたライアンA.フリン博士は、一連の化学的そして生化学的アプローチを使うことで、保存されている小さなノンコーディングRNAがシアル化グリカンを保有していること、そしてそれら糖鎖RNAが培養細胞およびインビボの複数の細胞型および哺乳動物種に存在することを発見しました。
この発見では、クリック反応可能なアジド基で官能化された細胞または動物を前駆体糖で代謝的に標識するという戦略がとられました。 アジド糖は、細胞グリカンに組み込まれた後ビオチンプローブと生体直交反応させることが可能になり、濃縮や同定そして視覚化ができるようになります。 シアル酸のアジド標識前駆体である過アセチル化N-アジドアセチルマンノサミン(Ac4ManNAz)を使うと、標識細胞からの高度に精製されたRNA調製物はアジド反応性を示すことがわかりました。 糖鎖RNAの集合は、正準N-グリカン生合成機構に依存しており、その結果シアル酸とフコースが濃縮された構造になります。 生体細胞のさらなる分析により、糖鎖RNAの大部分が細胞表面に存在し、そこで抗dsRNA抗体およびSiglec受容体ファミリーのメンバーと相互作用することが明らかになっています。 糖鎖RNAの役割を調査するためには、さらなる研究が必要です。
生体直交化学のお陰で、RNA生物学と糖鎖生物学との間に直接的な関係性が確立され、今後もまだまだ数多くの発見が期待できます。
今後の生体直交化学の見通し
生体直交化学は、科学や医学に幅広く応用可能であり、また近年ではそれによってさまざまな研究が大きく前進しています。 糖鎖RNAの発見を通じてグリコシル化の分野を発展させたことに加え、薬物送達や薬剤標的でも応用が有望視されており、今後はその応用はさらに拡大していくものと見込まれています。 例としては、以下などが挙げられます。
- 医薬品の原位置合成。生体直交化学は、より小さな前駆体から薬剤を合成する際に役立つ可能性があります。 必要に応じて必要な時に創薬することにより、薬剤の効果が高まり毒性を低く抑えられるようになります。また、それにより 薬理学的介入の範囲も拡大されるでしょう。
- グリカンの標識化。葉酸リガンドを使うことで、アジド標識ガラクトサミンを含む脂質ナノ粒子が生成されています。 腫瘍組織において増加した葉酸受容体の存在により、LNPの内在化が起こり、続いて腫瘍細胞への積荷の放出が行われました。 腫瘍膜にアジド官能化ジベンゾシクロオクチンが組み込まれた結果、腫瘍細胞がヒト血清に曝露されると免疫応答を引き起こします。
- クリック反応による放出。この方法では、生体直交化学を用いて薬物放出のタイミングと位置を制御し、選択的に標的細胞に対して毒性を投与する薬剤を作り出すことができます。
継続的な開発と反応に対する改良を続けることで、生体直交化学はさらなる研究のための重要なツールとなるでしょう。
生体直交化学とその幅広い用途の詳細については、Bioconjugate Chemistry の記事と関連CAS Insights Reportを参照してください。