
AIの活用による発見はさらに勢いを増しており、重大な成果を上げています。そしてこれには創薬も含まれます。AIが設計した最初の薬剤候補の臨床試験が始まることが、2020年初頭にExscientia社により報告されました。AIによる創薬の重要な瞬間です。 その後、Insilico Medicine社、Evotec社、Schrödinger社など複数の企業が第I相臨床試験を発表しています。 AIを活用したソリューションにより、臨床開発を加速させた候補薬も複数あります。 AIベースの創薬に注力する製薬会社のうち、約160の創薬プログラムが公開されており、そのうち15製品が臨床開発中とされています。
構造的に新規性のある分子は、有望な新薬候補になる可能性が著しく高いため、AI設計による分子の新規性を測定する方法を検討することが不可欠になってきます。 CASは、AIによる新薬の革新性をより適切に評価するために、新規分子化合物(NME)の構造的新規性に基づいた創薬イノベーションの新たな指標を発表しました。
そこで、ヒトの臨床試験が始まる最初3つのAI設計の薬剤候補に対し、この初期段階AI創薬用の新しい尺度を用いて構造的新規性を評価してみました。 これら3つの分子(DSP-1181、EXS21546、DSP-0038)はすべて第I相試験中で、Exscientia社のAIプラットフォームを使って発見されたものです。 正確な構造は明らかにされていないものの、最近の特許出願やExscientia社のIPO目論見書に含まれている詳細から、特定の分子にある程度絞り込んで分析することができます。
AI創薬の最初の3つの薬剤候補は、どれほど画期的なのでしょうか。 分析の結果は以下のとおりです。
AI創薬におけるDSP-1181
DSP-1181が日本で第1相臨床試験を開始すると発表されたのは2020年1月でした。 DSP-1181は、Exscientia社と大日本住友製薬株式会社の共同研究の一環として発見されたセロトニン5-HT1a受容体のアゴニストです。 現在、強迫性障害(OCD)の治療薬として研究されています。
US10800755(DSP-1181ファミリーで特許が付与された2つのうちの1つ)では、3つの薬分子のみが具体的に請求項に記載されています。 構造解析の結果、請求項の分子(例1、8、11)はいずれも、1967年にFDAが承認した第一世代(定型)抗精神病薬として頻用されているハロペリドールと形状が共通していることが判明しました(下表参照)。 抗精神病薬はOCDの治療薬としてFDAから承認されていませんが、ハロペリドールなどの抗精神病薬はOCD患者の選択的セロトニン再取り込み阻害薬(SSRI)を増強するために用いられ、ある程度の成功を収めています。
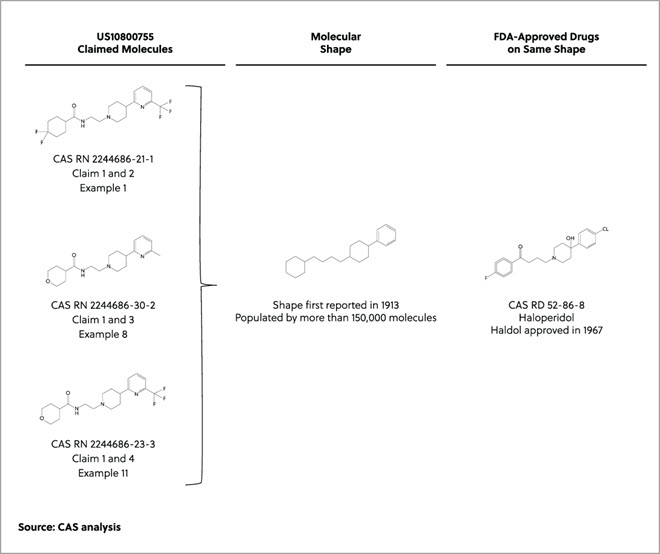
また、この特許には、生物活性データが開示された38の例示分子が含まれており、Exscientia社の目論見書によれば、これはDSP-1181の発見の際に合成・アッセイされた350の分子の11%に相当します。 これら例示された薬分子の形状は、上の表で明らかなようにFDA承認薬ハロペリドールと58%が共通した形状になっており、構造的多様性に欠けています。 さらに、例示された分子の21%が、28種の他のFDA承認薬で共通している形状に集中しています。これには、例えば抗てんかん薬で気分安定薬でもあり、OCD治療に時折使用されているラモトリギンが含まれています。 残り8つの例示薬分子は、他の3つの形状に分散されています。
AI創薬におけるEXS21546
2020年12月、Exscientia社の最も先進的な社内リード薬剤候補のEXS21546が、複数の種類の腫瘍に対する免疫腫瘍治療薬として英国で第I相臨床試験を開始しました。 EXS21546は、Exscientia社とEvotec社の共同研究の一環として発見されたアデノシンA2a受容体拮抗薬です。
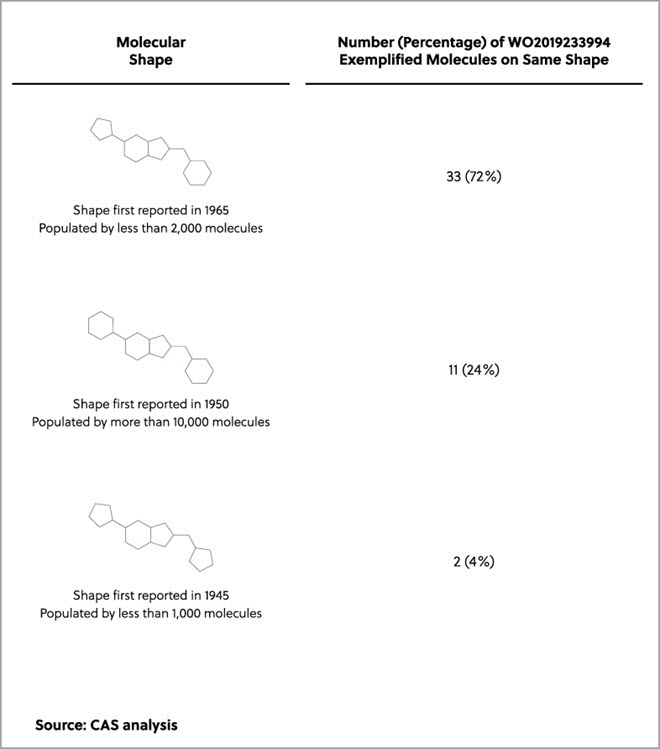
その特許であるWO2019233994には、生物活性データが開示された46の例示分子が含まれており、Exscientia社の目論見書によると、これはEXS21546の創薬時に合成・アッセイされた163分子の28%に相当します。 例示された分子は、環の大きさが1~2原子分しか違わないため、3つの構造的に類似した形状を反映しています(下表参照)。 これらの形状は、現在FDAで承認されている薬剤とは共通しないものの、我々の分析により、いくつかの報告済みのA2a拮抗薬と共通していることが判明しました。これには、ヤンセン社が同定し、そしてWO2010045006、WO2010045013、WO2010045017(いずれも2000年代後半に出願した特許)に開示されているものも含まれます。
AI創薬におけるDSP-0038
DSP-0038の米国での第1相臨床試験の開始が2021年5月に発表されました。 DSP-0038は、Exscientia社と大日本住友製薬株式会社の共同研究の一環として開発され、5-HT1a受容体アゴニストと5-HT2a受容体アンタゴニストの二重標的になっています。 現在、アルツハイマー病精神疾患の治療薬として研究されています。
US10745401(現在DSP-0038特許ファミリーの中で唯一付与されている特許)では、3種類の分子のみが具体的に請求項に記載されています。 請求項の分子(例109、135、171)の形状は、その環の大きさが1〜2原子分しか違わないため、構造的に類似しています(下表参照)。 弊社による臨床試験データの分析では、請求項の分子のうち2つ(例135と171)について、さまざまな精神疾患の治療に使用されているFDA承認済の非定型抗精神病薬と形状が同じであることが判明しました。 残りの形状は、現在FDAで承認されている薬剤とは共通しないものの、吉富薬品株式会社とサントリー株式会社が特定し、US5141930とUS6258805(いずれも1990年代に出願された特許)で開示されているいくつかのセロトニン受容体作動薬/拮抗薬の形状と構造的に類似しています。 そのリンカーの長さは、例109の形状から数原子分しか違いません。
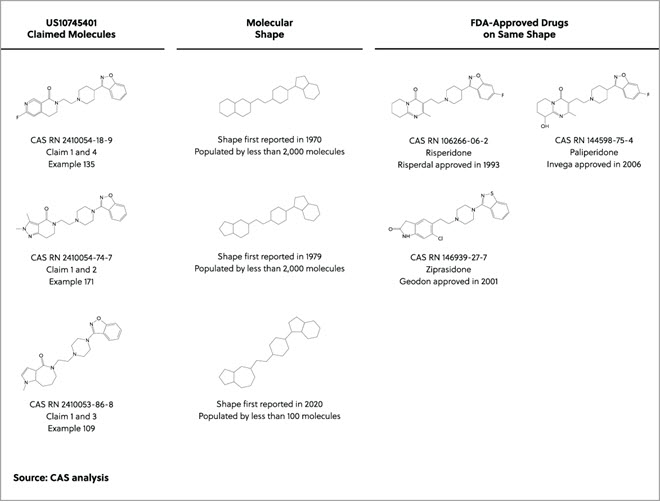
また、この特許には、194の例示薬分子とその生物活性データが開示されたものが含まれており、Exscientia社の目論見書によれば、これはDSP-0038の発見時に合成・アッセイされた500の分子のほぼ40%に相当します。 これらの例示された分子の形状は、上の表で明らかなように78%がFDA認可済み医薬品と同じ形状を共有し、また93%が請求項の3つの分子の形状に集中しているため、構造的多様性に欠けています。 残り14の例示分子は、他の8つの形状に分散されています。
AI創薬に関するまとめ
これらのAI創薬の候補薬の構造的革新性は、世界的に脚光を浴びるまでには行かないかもしれませんが、だからといって、AIが創薬に与える潜在的な影響が小さくないわけではありません。 AIに完璧な基準を求めるのではなく、AIが設計した薬分子の新規性は、薬化学者が設計した分子と同じ基準で判断されるべきものです。 今回の場合、医薬品化学者はこれらの分子を見たら、おそらく既存の科学文献に基づき、従来のアプローチで創薬された薬剤候補として同定していたはずです。
未来科学者ロイ・アマラの有名な言葉に、「我々は技術の効果を短期的には過大評価し、長期的には過小評価する傾向がある」というのがあります。これは今回においても非常に関連性のある指摘です。 AIによる創薬などの新技術は、当初は過大評価されますが、時間が経てば世界を大きく変える可能性があります。
臨床的利点が、構造的に新規性のある薬物としばしば関連付けられることが多いことを考えると、化学空間の限界をさらに押し上げることが新薬の探索においていかに重要かは明らかです。製薬業界のイノベーションを測定するのは困難ですが、CASは過去数十年の間に医薬品のイノベーションが大幅に増加したことを明確に示しました。ACSの出版物を参照していただければ、どのように構造的新規性が提案され、そして製薬イノベーションの最新トレンドを分析するために使用されたかを確認することができます。



