Até dezembro de 2021, foram aplicadas mais de 8 bilhões de doses de vacina para a doença do coronavírus de 2019 (Covid-19), incluindo cerca de 217 milhões de doses de “reforço”. O alvo principal é a chamada proteína “spike” ou “S”, uma proteína viral essencial que desempenha um papel fundamental ao permitir que o vírus invada as células hospedeiras.
Embora as vacinas sejam imprescindíveis, o desenvolvimento de tratamentos para a Covid-19 revelou que as proteínas intrinsecamente desordenadas podem desempenham um papel patológico crítico. Historicamente, os biólogos acreditavam que a sequência de aminoácidos de cada proteína determina sua estrutura tridimensional, o que, por sua vez, determina sua função. No entanto, há um grande grupo de proteínas e regiões que não possuem uma estrutura 3D fixa ou ordenada, mas ainda exibem atividades biológicas essenciais – as chamadas proteínas e regiões intrinsecamente desordenadas (Figura 1).
Esse distúrbio proteico está codificado em sequências de aminoácidos e é abundante em todos os organismos vivos e nos vírus. Uma compreensão mais profunda das relevantes regiões de características da proteína do SARS-CoV-2 pode permitir um progresso mais rápido no desenvolvimento de tratamentos para a Covid-19.
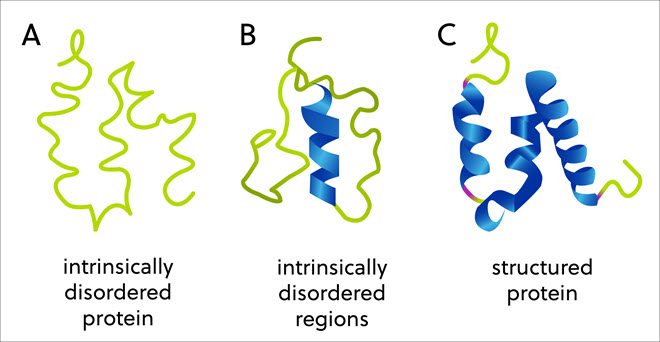
Exemplos de proteínas intrinsecamente desordenadas
A variabilidade natural encontrada nas "proteínas intrinsecamente desordenadas" (IDPs) ou nas "regiões intrinsecamente desordenadas (IDPRs)" podem ser observadas nos três reinos da vida. Elas estão ligadas a processos importantes como catálise enzimática, regulação alostérica, sinalização celular, transcrição, entre outros.
No entanto, elas também desempenham um papel nas doenças, incluindo neurodegeneração, diabetes, doenças cardiovasculares, amiloidose, doenças genéticas e câncer. Além disso, as proteínas virais geralmente contêm tais regiões, que foram correlacionadas com a virulência porque conferem a capacidade das proteínas virais se ligarem, de maneira fácil e indiscriminada às proteínas do hospedeiro.
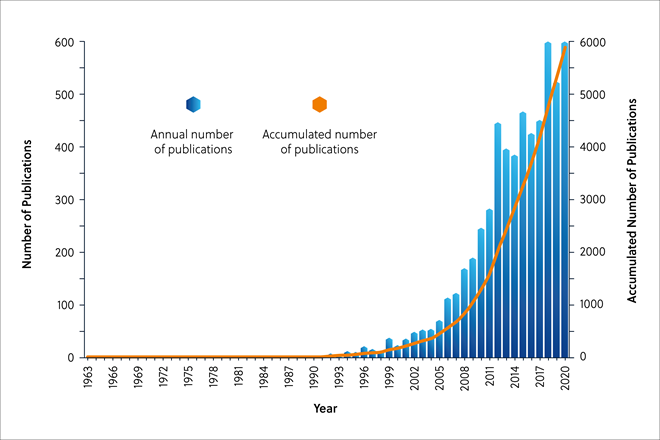
O interesse nas IDPs/IDPRs na ciência das proteínas tem crescido rapidamente desde o ano 2000, como demonstrado pela pesquisa no CAS Content CollectionTM (Figura 2), e seu papel no design de medicamentos, inclusive para a Covid-19, estão começando a ser explorados.
Proteínas intrinsecamente desordenadas no SARS-CoV-2
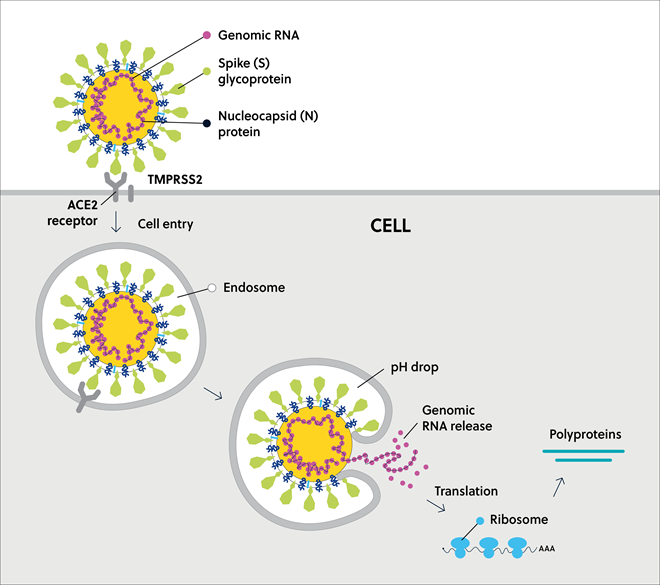
O SARS-CoV-2 forma um virion contendo seu RNA genômico empacotado em uma partícula que compreende: a proteína S, importante para a entrada nas células hospedeiras; a proteína de membrana (M) que facilita a montagem viral; a proteína do pequeno envelope do canal iônico (E); e a proteína do nucleocapsídeo (N), que se junta ao RNA viral para formar o nucleocapsídeo (Figura 3).
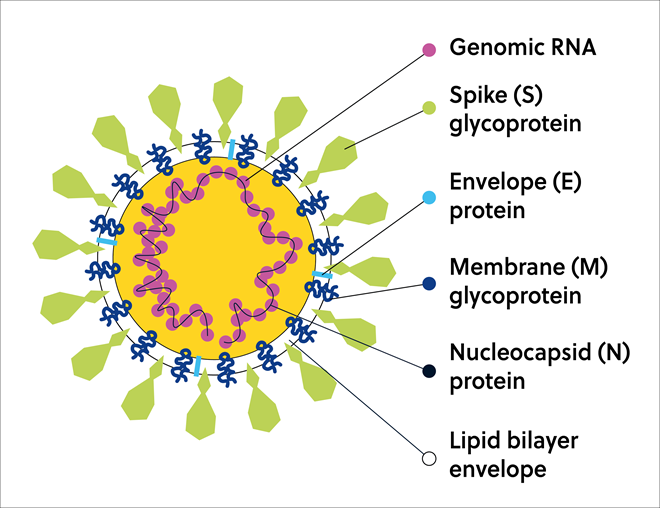
IDPs/IDPRs não são comuns no proteoma SARS-CoV-2. A bem da verdade, o proteoma SARS-CoV-2 exibe níveis significativos de ordem estrutural, exceto pela proteína do nucleocapsídeo (N), as proteínas do SARS-CoV-2 são proteínas altamente ordenadas que contêm poucas regiões de proteínas intrinsecamente desordenadas. É digno de nota, no entanto, que as regiões desordenadas existentes contribuem significativamente para o funcionamento e virulência do vírus e, portanto, são alvos promissores de drogas para a descoberta de medicamentos antivirais; tal abordagem já provou ser valiosa na identificação de novos candidatos a medicamentos.
Proteína do nucleocapsídeo (N)
A proteína N de ligação ao RNA estabiliza o RNA genômico dentro da partícula do vírus e regula a transcrição, replicação e empacotamento do genoma viral. A proteína N é altamente desordenada – sua porcentagem média de desordem intrínseca prevista é de cerca de 65%. Essas regiões desordenadas parecem ser importantes na manutenção do nucleocapsídeo e, portanto, podem servir como alvos para o design de medicamentos. Regiões desordenadas dentro da proteína N também parecem ser importantes para permitir que a proteína se agregue por meio de um processo denominado “separação de fase líquido-líquido”, possivelmente como uma forma de interromper a formação natural de grânulos de estresse, importantes na imunidade da célula hospedeira. Assim, a interrupção do processo de separação de fase líquido-líquido da proteína N é promissora para a intervenção antiviral e oferece novos alvos e estratégias para o desenvolvimento de medicamentos para combater a Covid-19.
Proteína spike (S)
A proteína S ornamenta a superfície do vírus como uma coroa. Ela é fundamental para a entrada do vírus no hospedeiro (Figura 4) e, como tal, tem sido alvo para medicamentos comumente utilizados no desenvolvimento de vacinas contra a Covid-19. A ligação com o receptor e a fusão da membrana, as etapas iniciais da infecção, estão relacionadas a regiões de desordem intrínseca significativa.
Análises da proteína S indicam que tanto os locais de clivagem da subunidade S associados à maturação de S e o peptídeo de fusão S estão associados a IDPRs. Considerando que a digestão proteolítica é consideravelmente mais rápida em regiões de proteínas não estruturadas comparada com as estruturadas, essa especificidade estrutural da proteína SARS-CoV-2 S pode ter uma alta importância funcional.
Durante a infecção pelo vírus SARS-CoV-2, as IDPRs podem ser detectadas na interface da proteína spike e do receptor ACE2, o receptor encontrado nos tecidos humanos ao qual o vírus faz a ligação. Os principais resíduos da proteína spike têm uma forte afinidade de ligação ao ACE2, uma provável explicação para a alta transmissibilidade do SARS-CoV-2.
Tanto a ligação com o receptor quanto a fusão da membrana, as etapas iniciais e importantes na infecção pelo coronavírus, estão relacionadas a regiões de desordem intrínseca significativa na proteína S. Elas são os alvos principais para inibir a infecção pelo SARS-CoV-2.
Proteína da membrana (M)
A proteína M é a principal proteína transmembrana encontrada em grande número no virion. O SARS-CoV-2 possui uma das camadas externas de proteção mais duras entre os coronavírus – isso está possivelmente relacionado ao baixo distúrbio intrínseco da proteína M (6%) e pode ser responsável pela alta resiliência e transmissibilidade do vírus. De fato, foi demonstrada uma correlação entre a virulência de vários vírus e a porcentagem de desordem intrínseca de suas proteínas M, com proteínas M menos desordenadas sendo associadas a vírus mais contagiosos.
Perspectivas futuras: as fronteiras do design de medicamentos
Atualmente, existe uma grande preocupação em todo o mundo com o aparecimento de novos vírus e a ocorrência de epidemias associadas. Portanto, é de grande importância conhecer as estruturas e funções das proteínas virais para identificar alvos terapêuticos originais para a prevenção e tratamento de doenças.
Em nossa publicação revisada por pares na ACS Infectious Diseases, resumimos as informações disponíveis sobre o proteoma SARS-CoV-2 no que diz respeito à ocorrência de distúrbio intrínseco em suas proteínas. Na verdade, já se reconhece que o proteoma SARS-CoV-2 exibe níveis substanciais de ordem estrutural – apenas a proteína N é altamente desordenada. Embora outras proteínas do SARS-CoV-2 sejam caracterizadas por graus mais baixos de desordem, suas IDPRs existentes contribuem de maneira significativa para o funcionamento e a virulência do vírus e são alvos promissores de medicamentos para o design de medicamentos antivirais.
As IDPs são onipresentes e têm inúmeras funções biológicas cruciais que complementam a funcionalidade das proteínas ordenadas. No entanto, quando ocorre um mau funcionamento (por exemplo, expressão incorreta, processamento incorreto ou regulação incorreta), as IDPs/IDPRs tendem a se engajar em interações indesejáveis e se envolver no desenvolvimento de vários estados patológicos. De fato, muitas proteínas associadas à neurodegeneração, diabetes, doenças cardiovasculares, amiloidose e doenças genéticas, bem como a maioria das proteínas relacionadas ao câncer humano, são IDPs ou contêm IDPRs longas..
Embora seja possível utilizar as técnicas de biologia estrutural no desenvolvimento de medicamentos, a prática do design racional de medicamentos tem tradicionalmente subestimado a presença de desordem intrínseca nas proteínas alvo. Seria claramente um grande benefício compreender a estrutura dessas regiões no SARS-CoV-2 e outros proteomas patogênicos para o desenvolvimento de medicamentos para a Covid-19 e outros, continuando a expandir os limites do design de medicamentos.



