
Los exosomas son un subconjunto de nanovesículas extracelulares liberadas por las células como parte de su fisiología normal o cuando se dan ciertas patologías. En nuestra entrada anterior sobre la evolución de los exosomas, analizamos el progreso de estas nanopartículas naturales desde su descubrimiento inicial al auge reciente de la investigación de las vesículas extracelulares.
En la segunda parte de esta serie de tres entradas exploraremos nuevos datos obtenidos en CAS Content Collection™, la mayor recopilación de conocimiento científico publicado seleccionada por expertos, y resumiremos las principales aplicaciones de los exosomas en los campos de la administración de fármacos y el diagnóstico.
Tendencias de investigación en alza sobre las aplicaciones médicas de los exosomas
Usamos CAS Content Collection para analizar la presencia y las tendencias de algunos conceptos clave en las publicaciones científicas relacionadas con las aplicaciones de los exosomas en la administración de fármacos y el diagnóstico (figura 1). Las palabras clave "targeting" (enfermedad objetivo) y "biomarker" (biomarcador) ocuparon los primeros puestos, lo que refleja el interés creciente por el uso terapéutico de los exosomas. El análisis de los conceptos clave en el periodo comprendido entre los años 2017 y 2021 reveló un aumento brusco del término “blood-brain barrier” (barrera hematoencefálica) a lo largo de los dos últimos años, lo que indica que este es un tema candente en la investigación sobre el uso médico de los exosomas. Como descubrimos en la primera parte, los exosomas pueden atravesar la barrera hematoencefálica. La capacidad de cruzar esta barrera tan selectiva no solo los hace valiosos como herramientas diagnósticas, sino que proporciona además una vía para administrar una carga terapéutica en el cerebro, lo que ayuda a tratar el cáncer y las lesiones cerebrales traumáticas.
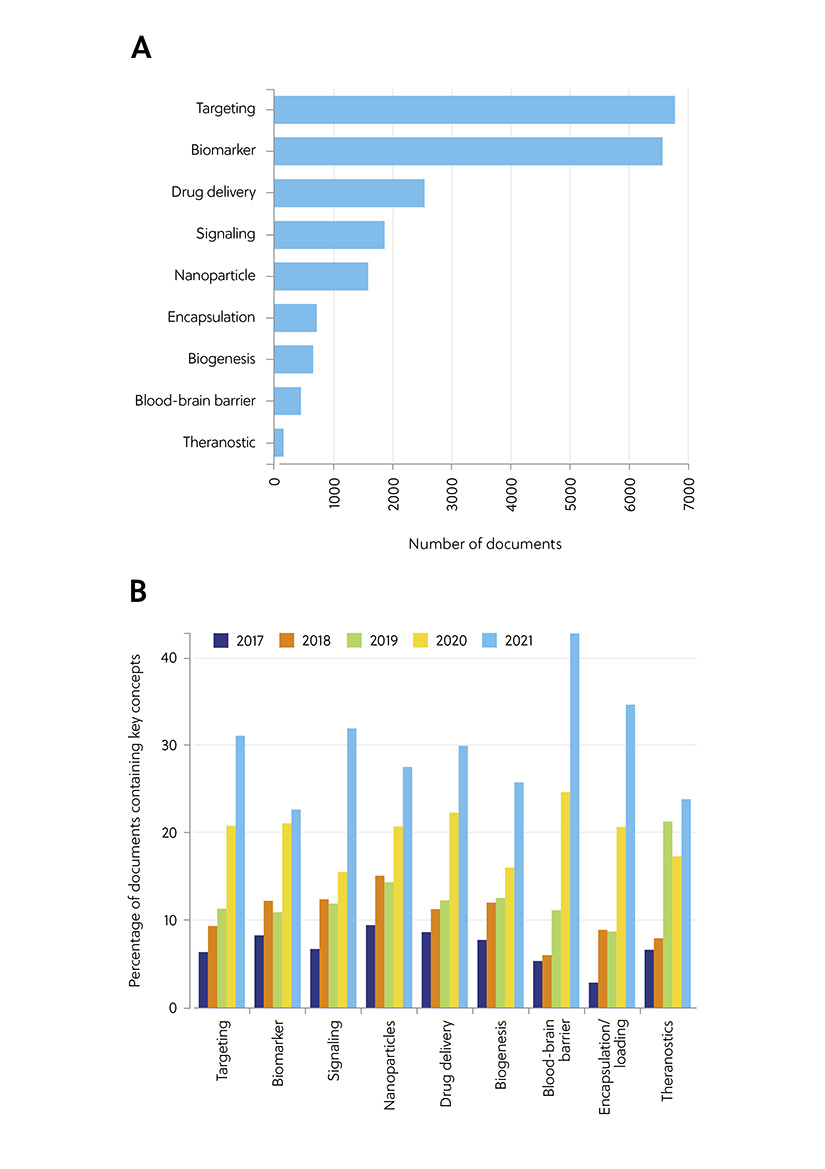
Figura 1. Conceptos clave en las publicaciones científicas relacionadas con las aplicaciones de los exosomas en la administración de fármacos y el diagnóstico: (A) Número de publicaciones que exploran conceptos clave relacionados con las aplicaciones terapéuticas y diagnósticas de los exosomas. (B) Tendencias de los conceptos clave presentados en los artículos relacionados con las aplicaciones terapéuticas y diagnósticas de los exosomas durante los años 2017-2021. Los porcentajes se calculan a partir del número de publicaciones anuales sobre cada concepto clave, normalizado en función del número total de publicaciones sobre el mismo concepto en el mismo periodo de tiempo.
El primer paso crucial para el uso médico de los exosomas: aislamiento y purificación
Para que los exosomas se puedan utilizar a gran escala en la práctica médica, es esencial distinguir estas nanopartículas con precisión de un amplio espectro de residuos celulares y contaminantes. No hay un único método estandarizado para la separación y el análisis de exosomas, y cada método tiene un conjunto específico de fortalezas y limitaciones (resumidas en la tabla 1). Aunque en el pasado la ultracentrifugación era el método de referencia, en los últimos años los métodos basados en la precipitación y los microfluidos han ganado popularidad por su capacidad de purificar exosomas sin causar posibles daños (figura 2). Se ha sugerido el uso de una combinación de varios de estos métodos como estrategia prometedora para mejorar los resultados del aislamiento. Este consiste en proporcionar subconjuntos de exosomas con una elevada pureza en cuanto a tamaño, morfología, concentración, presencia de marcadores enriquecidos con exosomas y ausencia de contaminantes.
Tabla 1. Principales métodos de aislamiento y purificación de exosomas
| Método | Ventajas | Desventajas |
| Ultrafiltración |
|
|
| Ultracentrifugación |
|
|
| Inmunoafinidad |
|
|
| Precipitación de polímeros |
|
|
| Cromatografía por exclusión de tamaño |
|
|
| Microfluidos |
|
|
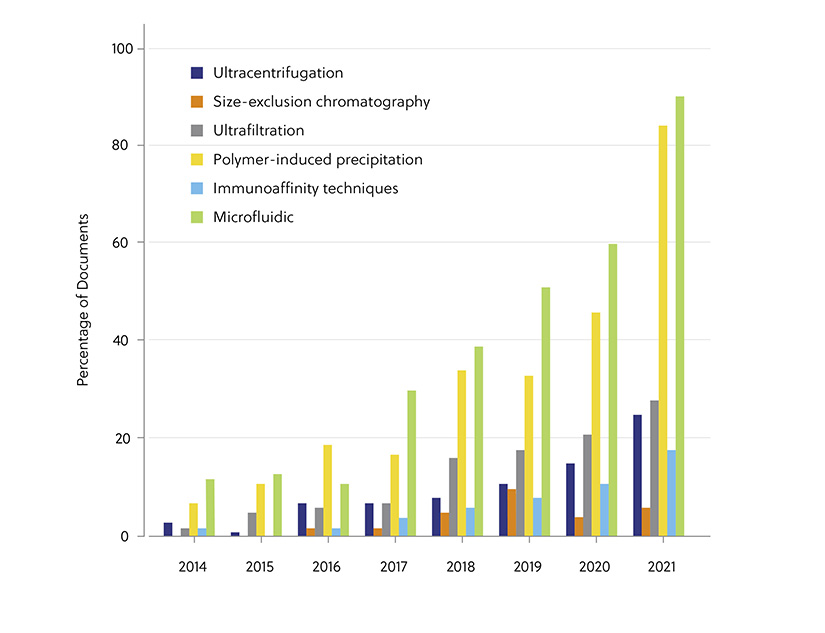
Figura 2. Tendencias del número de documentos relacionados con las aplicaciones terapéuticas y diagnósticas de los exosomas para varios métodos de aislamiento de exosomas durante los años 2014-2021. (Los porcentajes se calculan a partir del número de publicaciones anuales sobre cada método de aislamiento, normalizado en función del número total de publicaciones sobre el mismo método de aislamiento en el mismo periodo de tiempo).
Exosomas y administración de fármacos
Una vez que los exosomas se han extraído y purificado, ¿cómo los convertimos en sistemas eficaces para la administración de fármacos? Por suerte, los exosomas están diseñados para esta función y combinan las ventajas de los nanoportadores sintéticos y los sistemas de administración de fármacos mediados por células sin sus limitaciones. El primer paso para controlar estas propiedades es la “carga”, el proceso consistente en introducir los materiales terapéuticos en los exosomas. Para este fin se han empleado varios métodos de carga, cada uno con sus propias ventajas y desventajas (tabla 2).
Tabla 2. Técnicas de carga
| Método | Ventajas | Desventajas |
| Transfección celular |
|
|
| Coincubación directa |
|
|
| Sonicación |
|
|
| Electroporación |
|
|
| Congelación-descongelación |
|
|
| Extrusión |
|
|
Como mensajeros intercelulares, los exosomas desempeñan un papel crucial en diferentes procesos fisiológicos. Los exosomas secretados por distintos tejidos y células tienen propiedades distintivas. Por ejemplo, se ha descubierto que los exosomas derivados de tumores afectan a propiedades de los tumores como el crecimiento, la angiogénesis, la invasión y la metástasis. En cambio, los exosomas de células madre mesenquimatosas tienen propiedades que permiten su uso como adyuvantes para reforzar y complementar otras modalidades terapéuticas. De hecho, una empresa de Estados Unidos, Direct Biologics, está explorando la utilidad del fármaco ExoFlo, derivado de las células madre mesenquimatosas, en ensayos clínicos para la colitis ulcerosa, el rechazo de órganos sólidos y la COVID-19, por mencionar solo algunos ejemplos.
Aunque las aplicaciones terapéuticas potenciales de los exosomas son muy amplias, el área más común de la investigación exosómica es, con diferencia, el cáncer, seguida de la inflamación y la infección. Al analizar la correlación entre las células donantes de exosomas y las enfermedades en las que se han aplicado, surge un patrón claro. Las células presentadoras de antígeno y las células NK se usan principalmente en estudios sobre el cáncer. Los macrófagos y las células madre se usan sobre todo en la inflamación, mientras que las células presentadoras de antígeno y los linfocitos T se suelen usar en la infección (figura 3).
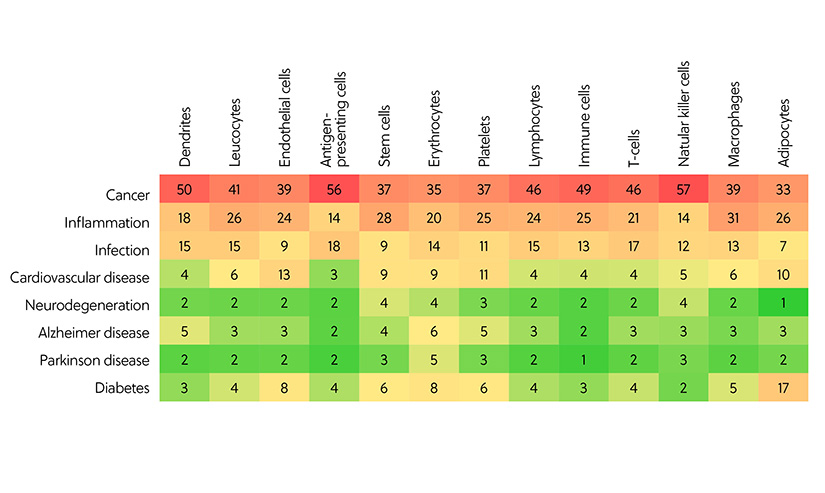
Figura 3. Correlación entre las células donantes de exosomas y las enfermedades en las que se han aplicado los exosomas en los estudios relacionados con sus aplicaciones terapéuticas y diagnósticas. La correlación viene representada por el número de documentos encontrados en CAS Content Collection.
Variedad de las enfermedades en las que se aplican los exosomas
Otra aplicación destacada de los exosomas que está creciendo rápidamente es su uso como agentes terapéuticos. Los sistemas de exosomas se han usado como herramientas terapéuticas o diagnósticas en una amplia selección de enfermedades. Nuestro análisis de CAS Content Collection muestra que la mayoría de las publicaciones (68 %) sobre el uso terapéutico de los exosomas están asociadas con el cáncer. Se ha comprobado que el microARN (miARN) exosómico inhibe la proliferación, la migración y la invasión de las células cancerosas. Esta estrategia ha sido explorada en varios subtipos de células malignas, incluidas las del cáncer de vejiga, colorrectal y de mama. Los exosomas tienen además un enorme potencial terapéutico en enfermedades neurodegenerativas, inflamatorias y cardiovasculares, que también se representan (figura 4).
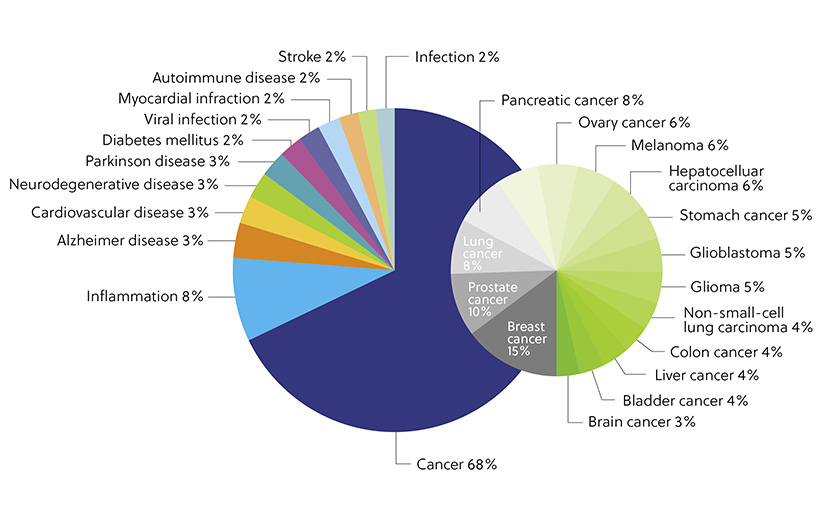
Figura 4. Distribución de las publicaciones de CAS Content Collection relacionadas con aplicaciones terapéuticas y diagnósticas de los exosomas para distintas enfermedades.
Dado que los exosomas participan en la patogenia de enfermedades como el cáncer, una buena estrategia terapéutica puede requerir reducir una producción y circulación elevada de exosomas a niveles normales para prevenir el progreso de la enfermedad. Varios estudios en curso están explorando los efectos de modular la vía terapéutica de los exosomas en varios pasos, entre los que se incluyen su producción, su liberación y su captación. La eliminación física de exosomas también se ha explorado en células cancerosas. Los investigadores creen que esta eliminación puede dificultar la comunicación entre las células tumorales que contribuyen al avance del tumor.
Uso diagnóstico de los exosomas
Para que su uso clínico sea viable, un biomarcador debe tener varias propiedades. Debe ser fácilmente accesible, rentable y específico, tener una sensibilidad elevada y ser medible. Por sus excepcionales propiedades, los exosomas cumplen varias de estas condiciones y son superiores a otros biomarcadores serológicos convencionales, sobre todo en lo que respecta a la sensibilidad y la precisión del diagnóstico.
Este uso terapéutico de los exosomas tiene varias ventajas. En primer lugar, puesto que el estado patológico de las células tiene una gran influencia en el contenido de los exosomas (como se ha observado en la enfermedad de Alzheimer), estudiar estas vesículas extracelulares puede permitirnos conocer el estado patológico del tejido. Son, además, estables de forma natural, ya que cuentan con una doble capa lipídica que les permite resistir la degradación incluso en microentornos extremos. Desde el punto de vista práctico, los exosomas se pueden aislar de una forma sencilla y no invasiva en fluidos biológicos como la orina, la sangre e incluso las lágrimas. Una vez extraídos, se pueden almacenar mediante procesos de congelación, liofilización o secado por pulverización. Por último, a diferencia de muchos biomarcadores serológicos convencionales, los exosomas pueden atravesar la barrera hematoencefálica y proporcionar información sobre las células cerebrales que sería difícil obtener de otro modo. Actualmente se están explorando varios biomarcadores de proteínas (tabla 3) y biomarcadores de ácidos nucleicos (tabla 4) exosómicos. Puede encontrar la lista completa de estos biomarcadores en el artículo Exosomes – Nature’s Lipid Nanoparticles, A Rising Star in Drug Delivery and Diagnostics de ACS.
Tabla 3. Ejemplos de proteínas exosómicas para aplicaciones de diagnóstico clínico
| Proteína(s) | Enfermedad | Fluido corporal |
| CD81 | Hepatitis C crónica | Plasma sanguíneo |
| CD63, caveolina-1, TYRP2, VLA-4, HSP70, HSP90 | Melanoma | Plasma sanguíneo |
| Receptor VIII de factor de crecimiento epidérmico | Glioblastoma | Plasma sanguíneo |
| Survivina | Cáncer de próstata | Plasma sanguíneo |
| c-src | Discrasias de células plasmáticas | Plasma sanguíneo |
| NY-ESO-1 | Cáncer de pulmón | Plasma sanguíneo |
| PKG1, RALGAPA2, NFX1, TJP2 | Cáncer de mama | Plasma sanguíneo |
| Glipicano-1 | Cáncer de páncreas | Suero sanguíneo |
| Glipicano-1 | Cáncer colorrectal | Plasma sanguíneo |
| AMPN VNN1, PIGR | Colangiocarcinoma | Suero sanguíneo |
| CD24, EpCAM, CA-125 | Cáncer de ovario | Plasma sanguíneo |
| CD91 | Cáncer de pulmón | Suero sanguíneo |
| Fetuina-A, ATF 3 | Insuficiencia renal aguda | Orina |
| CD26, CD81, S1c3A1, CD10 | Insuficiencia hepática | Orina |
| NKCC2 | Síndrome de Bartter de tipo 1 | Orina |
| EGF, subunidad α de Gs, resistina, proteína 3 inducida por ácido retinoico | Cáncer de vejiga | Orina |
| A2M, HPA, MUC5B, LGALS3BP, IGHA1, PIP, PKM1/M2, GAPDH | Carcinoma de células escamosas | Saliva |
| LMP1, Galectina-9, BARF-1 | Cáncer nasofaríngeo | Sangre, saliva |
| CALML5, KRT6A y S100P | Síndrome del ojo seco | Lágrimas |
Tabla 4. miARN exosómicos como agentes terapéuticos y diagnósticos para el cáncer
| miARN | Tipos de cáncer | Aplicaciones |
| miR-378 | Carcinomas amicrocíticos de pulmón | Pronóstico |
| miR-423, miR-424, let7-i y miR-660 | Cáncer de mama | Diagnóstico |
| miR-423-3p | Cáncer de próstata | Pronóstico; resistencia a la castración |
| miR-30a | Carcinoma de células escamosas de la cavidad bucal | Tratamiento; sensibilidad al cisplatino |
| miR-106b-3p | Cáncer colorrectal | Tratamiento |
El interés por el uso de los exosomas como biomarcadores se refleja en el gran crecimiento del número de documentos relacionados con aplicaciones terapéuticas y diagnósticas de los exosomas, como revela un análisis de CAS Content Collection (figura 5). Aunque a primera vista se podría pensar que los documentos relacionados con el uso terapéutico predominan sobre el resto, el porcentaje general de documentos se distribuye por igual entre las dos aplicaciones.
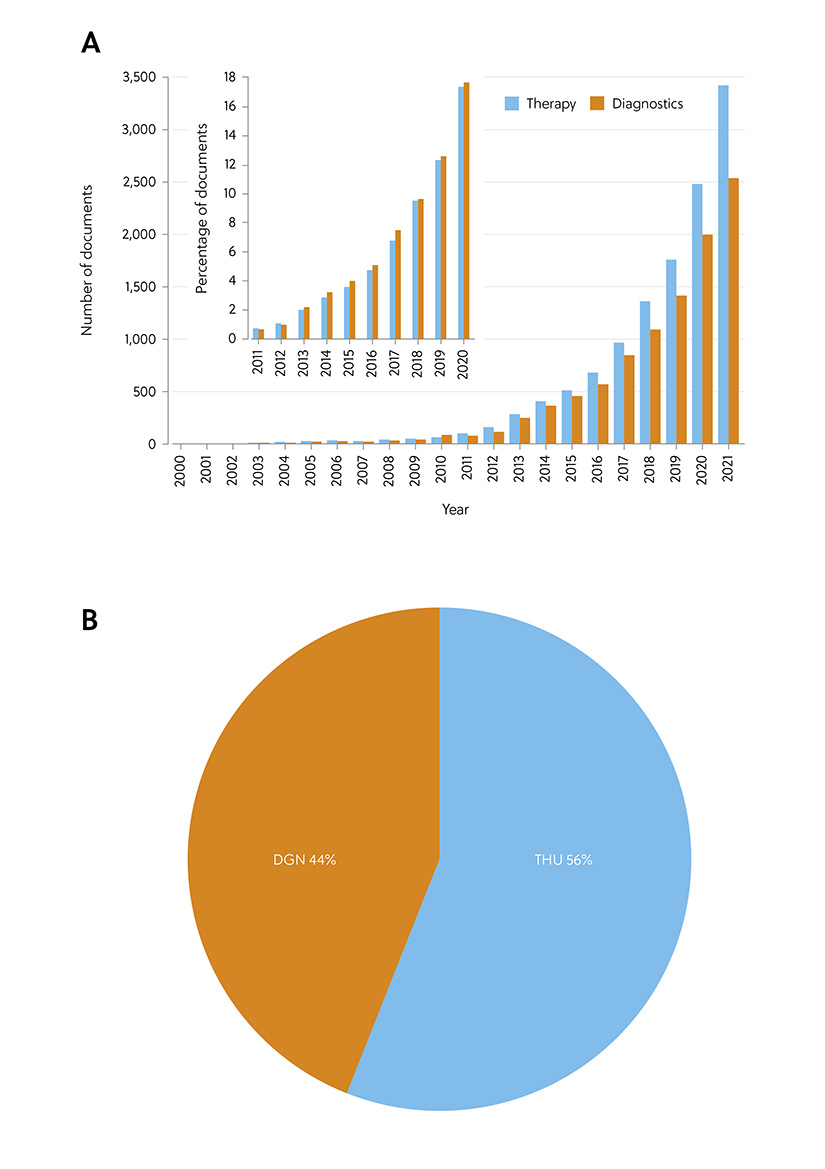
Figura 5. Comparación entre las aplicaciones diagnósticas y terapéuticas de los exosomas: (A) Comparación entre el número de documentos relacionados con aplicaciones terapéuticas y el número de documentos sobre aplicaciones diagnósticas de los exosomas; gráfico insertado: crecimiento anual del número de documentos relacionados con aplicaciones terapéuticas comparado con el de los relacionados con aplicaciones diagnósticas de los exosomas. (B) Comparación entre el número de documentos relacionados con aplicaciones terapéuticas y el número de documentos sobre aplicaciones diagnósticas de los exosomas por indicadores de funciones (THU, terapéutico; DGN, diagnóstico).
Aunque la investigación sobre el uso médico de los exosomas es prometedora, muchos estudios permanecen en la fase preclínica. Dicho eso, ¿cómo de cerca estamos de aprovechar todo el potencial terapéutico y diagnóstico de los exosomas? ¿Cuáles son los obstáculos y los desafíos que dificultan los avances? En el último artículo de la serie, revelaremos los actores clave en la investigación de los exosomas y ofreceremos información actualizada sobre las principales iniciativas de investigación en este interesante y dinámico campo. Mientras tanto, puede obtener más información en el informe sobre los exosomas de CAS Insights.



