
Les exosomes sont un sous-ensemble nanométrique de vésicules extracellulaires libérées par les cellules dans le cadre de leur physiologie normale ou dans certaines pathologies. Dans notre blog précédent consacré à l'évolution exosomale, nous évoquions les progrès de ces nanoparticules naturelles, depuis leur découverte initiale jusqu'à l'essor récent de la recherche sur les vésicules extracellulaires.
Dans la deuxième partie de ce blog en trois volets, nous explorerons d'autres informations extraites de la Collection de contenus CAS™, la plus grande collection organisée par des humains de connaissances scientifiques publiées, récapitulant les applications essentielles de la thérapie par exosomes dans l'administration de médicaments et les diagnostics.
Les tendances croissantes de la recherche sur les thérapies par exosomes
En utilisant CAS Collection de contenus, nous avons analysé la présence et les tendances de certains concepts clés dans les publications scientifiques pertinentes pour les applications d'exosomes dans l'administration de médicaments et les diagnostics (Figure 1). Les mots clés « ciblant » et « biomarqueur » sont arrivés en tête, ce qui témoigne de l'intérêt croissant pour les exosomes dans la thérapeutique. Il est significatif que l'analyse des concepts clés au cours des années 2017-2021 ait révélé une forte hausse du terme « barrière hémato-encéphalique » au cours des deux dernières années, ce qui indique qu'il s'agit d'un sujet majeur dans la recherche de thérapies par exosomes. Comme nous l'avons appris dans la première partie, les exosomes peuvent franchir la barrière hémato-encéphalique. L'aptitude à franchir cette limite extrêmement sélective rend non seulement les exosomes précieux en tant qu'outils de diagnostic, mais pourrait aussi fournir un moyen d'administrer des thérapies dans le cerveau afin de traiter le cancer et les lésions traumatiques du cerveau.
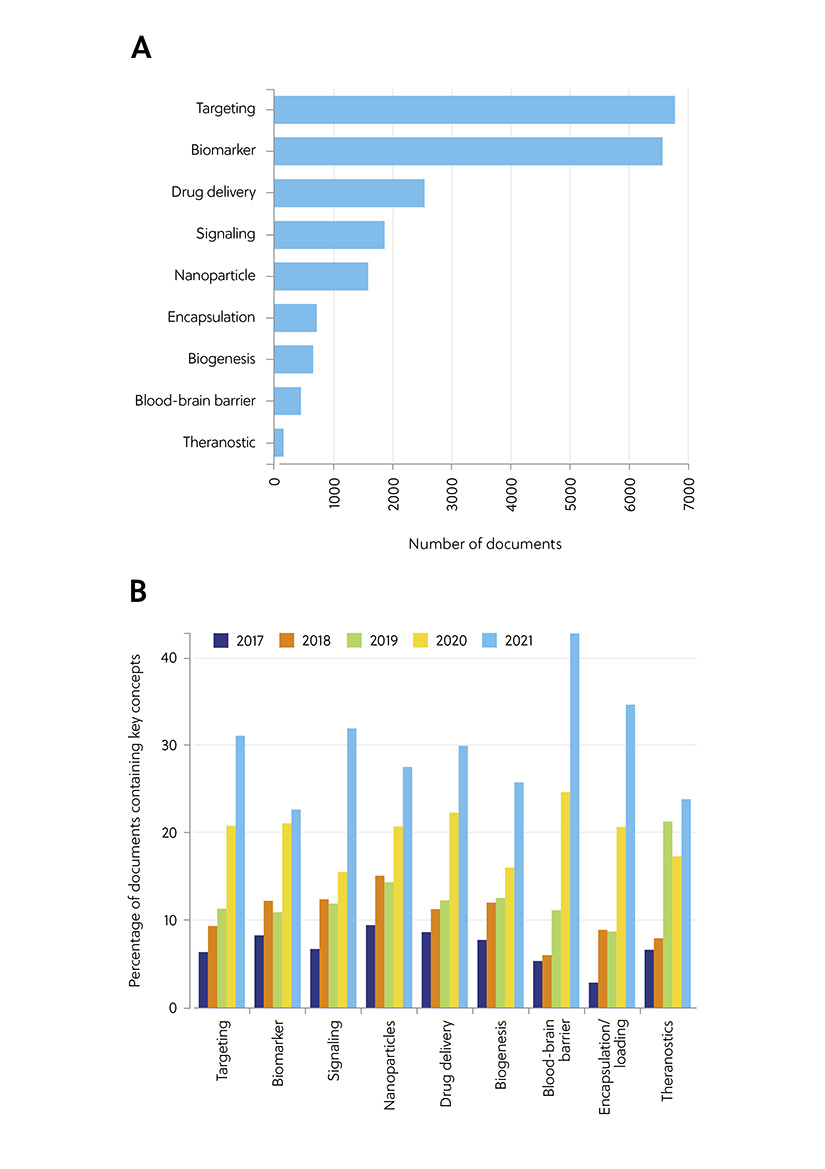
Figure 1. Concepts majeurs dans les publications scientifiques pertinentes pour les applications d'exosomes dans l'administration de médicaments et les diagnostics : (A) Nombre de publications explorant les concepts majeurs liés aux applications des exosomes dans la thérapie et les diagnostics. (B) Tendances dans les concepts clés présentées dans les articles consacrés aux applications de thérapies et de diagnostics par exosomes au cours de la période 2017 - 2021. Les pourcentages sont calculés à partir des nombres de publications annuelles pour chaque concept clé, normalisés par le nombre total de publications concernant le même concept au cours de la même période.
La première étape vitale de la thérapie par exosomes : isolation et purification des exosomes
Avant de pouvoir être utilisés dans la pratique médicale à grande échelle, il est essentiel de distinguer avec précision les nanoparticules que sont les exosomes dans un large spectre de débris cellulaires et de composants parasites. Il n'existe pas d'approche standardisée unique de la séparation et de l'analyse des exosomes. Chaque approche présente des points forts et des limites uniques (résumés dans le Tableau 1). Alors que l'ultracentrifugation était autrefois considérée comme la référence absolue, depuis quelques années, les méthodes de précipitation et de microfluidique se sont avérées plus populaires en raison de leur aptitude à purifier les exosomes sans provoquer de dommages potentiels (Figure 2). Une combinaison de plusieurs de ces méthodes a été suggérée comme une stratégie prometteuse pour améliorer les résultats en termes d'isolation. Cela a pour but de fournir des sous-ensembles d'exosomes présentant un niveau élevé de pureté en matière de taille, de morphologie, de concentration, de présence de marqueurs enrichis en exosomes et d'absence de contaminants.
Tableau 1. Principales méthodes d'isolation/de purification des exosomes
| Méthode | Avantages | Inconvénients |
| Ultrafiltration |
|
|
| Ultracentrifugation |
|
|
| Affinité immunologique |
|
|
| Précipitation de polymères |
|
|
| Chromatographie d'exclusion stérique |
|
|
| Microfluidique |
|
|
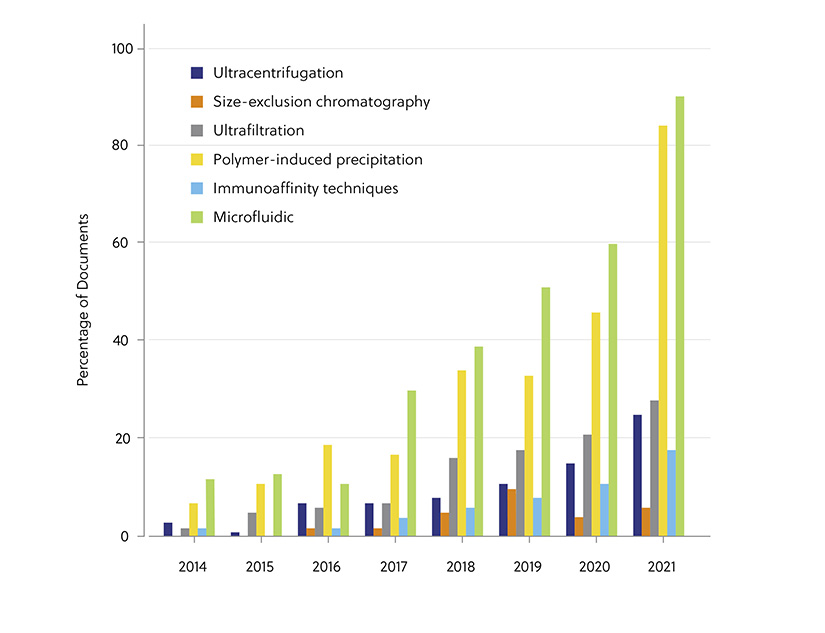
Figure 2. Tendances et nombre de documents consacrés aux applications de thérapies et de diagnostics par exosomes concernant différentes méthodes d'isolation des exosomes au cours de la période 2014-2021. Les pourcentages sont calculés à partir des nombres de publications annuelles pour chaque méthode d'isolation, normalisés par le nombre total de publications concernant la même méthode d'isolation au cours de la même période.
Thérapie par exosomes et administration des médicaments
Une fois les exosomes extraits et purifiés, comment les transformer en systèmes efficaces d'administration des médicaments ? Heureusement, les exosomes sont faits pour ce rôle, alliant les avantages des nanotransporteurs synthétiques et des systèmes d'administration de médicaments induits par les cellules, tout en évitant leurs limites. La première étape de l'exploitation de ces propriétés est le « chargement de la cargaison », le processus consistant à remplir les exosomes de matériaux thérapeutiques. Plusieurs méthodes de chargement de cargaison ont été employées à cette fin, chacune présentant ses avantages et ses inconvénients (Tableau 2).
Tableau 2. Techniques de chargement de cargaison
| Méthode | Avantages | Inconvénients |
| Transfection cellulaire |
|
|
| Co-incubation directe |
|
|
| Sonication |
|
|
| Électroporation |
|
|
| Congélation-décongélation |
|
|
| Extrusion |
|
|
En tant que messagers entre cellules, les exosomes jouent un rôle essentiel dans différents processus physiologiques. À ce titre, les exosomes secrétés par différents tissus et cellules démontrent des propriétés uniques. Par exemple, les exosomes dérivés de tumeurs se sont avérés affecter certaines propriétés tumorales telles que la croissance, l'angiogenèse, l'invasion et la métastase. À l'inverse, les exosomes issus de cellules souches mésenchymateuses (MSC) possèdent des propriétés qui les rendent idéales en tant qu'adjuvants pour soutenir et compléter d'autres modalités thérapeutiques. En fait, un laboratoire américain, Direct Biologics, étudie l'utilité de l'ExoFlo thérapeutique dérivé des MSC dans des essais cliniques portant sur la colite ulcéreuse, le rejet des organes solides et la COVID-19, pour ne citer que quelques exemples.
Même si les applications potentielles de la thérapie par exosomes sont très vastes, le domaine de recherche exosomale de loin le plus courant est le cancer, suivi de l'inflammation et de l'infection. En analysant la corrélation entre les cellules donneuses d'exosomes et les maladies auxquelles ils sont appliqués, on voit apparaître un modèle clair. Les cellules présentatrices d'antigènes et les cellules tueuses naturelles sont les plus fréquemment utilisées dans les études sur le cancer. Les macrophages et les cellules souches sont plus couramment utilisés dans le cas de l'inflammation, alors que les cellules présentatrices d'antigène et les lymphocytes-T sont souvent utilisés contre l'infection (Figure 3).
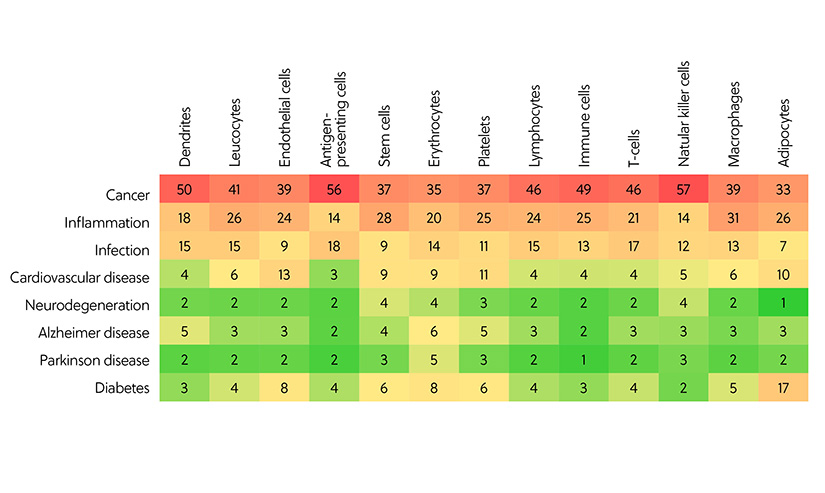
Figure 3. La corrélation entre les cellules donneuses d'exosomes et les maladies auxquelles les exosomes ont été appliqués lors des études liées à la thérapie par exosomes et aux diagnostics, telle que représentée par le nombre de documents figurant dans CAS Collection de contenus.
Les applications ciblées variées de la thérapie par exosomes
Une autre application notable et en expansion rapide des exosomes concerne leur utilisation en tant qu'agents thérapeutiques. Des systèmes exosomaux ont été utilisés en tant qu'outils thérapeutiques ou diagnostiques contre un large éventail de troubles. Notre analyse de CAS collection de contenus démontre que la plupart des publications (68 %) consacrées à la thérapie par exosomes sont associées au cancer. Les microARN des exosomes (MiRNA) ont démontré leur aptitude à inhiber la prolifération, la migration et l'invasion des cellules cancéreuses. Cette approche a été explorée dans différents sous-types de cellules malignes, notamment celles du cancer de la vessie, du cancer colorectal et du cancer du sein. Les exosomes présentent aussi un potentiel thérapeutique considérable contre les maladies neurodégéneratives, inflammatoires et cardiovasculaires, lesquelles sont également représentées (Figure 4).
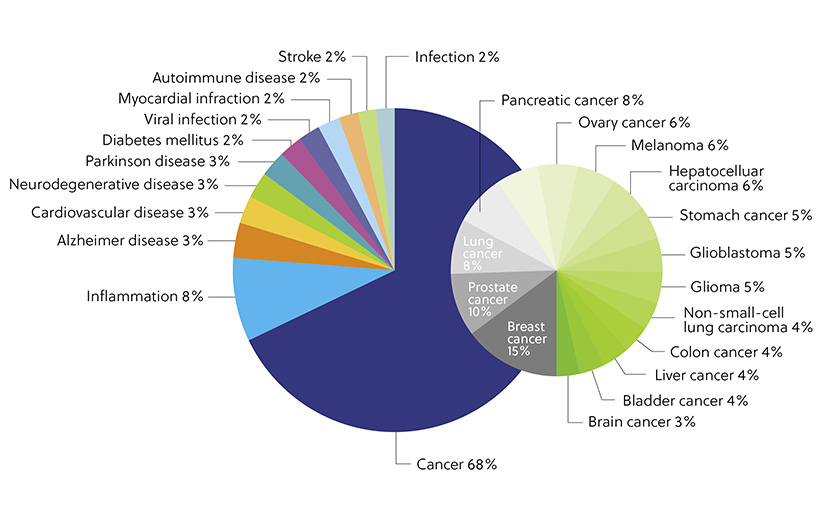
Figure 4. Répartition des publications de CAS Collection de contenus consacrées aux applications de la thérapie et des diagnostics par exosomes concernant les maladies ciblées.
Dans la mesure où les exosomes sont impliqués dans la pathogenèse de maladies telles que le cancer, une stratégie thérapeutique efficace pourrait passer par la réduction de la production et de la circulation élevées des exosomes à des niveaux normaux pour prévenir la progression de la maladie. Plusieurs études en cours étudient les impacts de la modulation de la voie thérapeutique des exosomes à différentes étapes, notamment leur production, leur libération et leur absorption. L'élimination physique des exosomes a également été examinée contre les cellules cancéreuses, les chercheurs supposant que cette élimination pourrait entraver la communication entre les cellules tumorales qui contribue à la progression des tumeurs.
Utilisations diagnostiques des exosomes
Pour être utilisable pour un usage clinique, un biomarqueur doit démontrer plusieurs propriétés. Il doit être facilement accessible, économique, spécifique, hautement sensible et mesurable. Compte tenu de leurs propriétés uniques, les exosomes réunissent déjà plusieurs de ces caractéristiques, démontrant une supériorité par rapport aux biomarqueurs classiques à base de sérum, en particulier en termes de sensibilité et de précision.
L'utilisation d'exosomes dans cette voie thérapeutique présente plusieurs avantages. Tout d'abord, comme le statut pathologique des cellules affecte considérablement le contenu des exosomes (comme on l'a observé dans le cas de la maladie d'Alzheimer), l'étude de ces vésicules extracellulaires pourrait fournir une fenêtre sur l'état de pathologie des tissus. Ils présentent également une stabilité innée, avec une bicouche lipidique qui leur permet de supporter la dégradation, même dans des micro-environnements hostiles. En termes d'utilisation pratique, les exosomes peuvent être isolés facilement et de manière non invasive dans des fluides biologiques tels que l'urine, le sang et même les larmes. Une fois extraits, ils peuvent être stockés par congélation, lyophilisation ou séchage par pulvérisation. Enfin, contrairement à de nombreux biomarqueurs sériques classiques, les exosomes peuvent traverser la barrière hémato-encéphalique, fournissant des informations au sujet des cellules du cerveau qui seraient autrement difficiles à obtenir. Plusieurs candidats biomarqueurs de protéines (Tableau 3) et biomarqueurs d'acides nucléiques (Tableau 4) exosomaux sont actuellement à l'étude. Pour accéder à la liste complète de ces biomarqueurs, reportez-vous à notre publication de l'ACS, Exosomes – Nature’s Lipid Nanoparticles, A Rising Star in Drug Delivery and Diagnostics (Exosomes - Les nanoparticules lipidiques de la nature, étoiles montantes de l'administration de médicaments et des diagnostics).
Tableau 3. Exemples de protéines exosomales dans des applications diagnostiques cliniques
| Protéine(s) | Maladie | Fluide corporel |
| CD81 | Hépatite C chronique | Plasma sanguin |
| CD63, cavéoline-1, TYRP2, VLA-4, HSP70, HSP90 | Mélanome | Plasma sanguin |
| Récepteur du facteur de croissance épidermique VIII | Glioblastome | Plasma sanguin |
| Survivine | Cancer de la prostate | Plasma sanguin |
| c-src | Dycrasies plasmocytaires | Plasma sanguin |
| NY-ESO-1 | Cancer du poumon | Plasma sanguin |
| PKG1, RALGAPA2, NFX1, TJP2 | Cancer du sein | Plasma sanguin |
| Glypican-1 | Cancer du pancréas | Sérum sanguin |
| Glypican-1 | Cancer colorectal | Plasma sanguin |
| AMPN VNN1, PIGR | Cholangiocarcinome | Sérum sanguin |
| CD24, EpCAM, CA-125 | Cancer des ovaires | Plasma sanguin |
| CD91 | Cancer du poumon | Sérum sanguin |
| Fétuine-A, ATF 3 | Insuffisance rénale aiguë | Urine |
| CD26, CD81, S1c3A1, CD10 | Insuffisance hépatique | Urine |
| NKCC2 | Syndrome de Bartter de type 1 | Urine |
| EGF, sous-unité α des G, résistine, protéine 3 induite par l'acide rétinoïque | Cancer de la vessie | Urine |
| A2M, HPA, MUC5B, LGALS3BP, IGHA1, PIP, PKM1/M2, GAPDH | Carcinome à cellules squameuses | Salive |
| LMP1, Galectine-9, BARF-1 | Cancer du nasopharynx | Sang, salive |
| CALML5, KRT6A et S100P | Sécheresse oculaire | Larmes |
Tableau 4. Les miARN exosomaux en tant qu'agents thérapeutiques et diagnostiques du cancer
| miARN | Types de cancer | Applications |
| miR-378 | Cancer du poumon non à petites cellules | Pronostic |
| miR-423, miR-424, let7-i et miR-660 | Cancer du sein | Diagnostic |
| miR-423-3p | Cancer de la prostate | Pronostic ; résistance à la castration |
| miR-30a | Carcinome épidermoïde de la cavité buccale | Thérapeutique ; sensibilité à la cisplatine |
| miR-106b-3p | Cancer colorectal | Thérapeutique |
L'intérêt des exosomes en tant que biomarqueurs est reflété par la croissance considérable du nombre de documents concernant les applications de la thérapie et des diagnostics par exosomes, comme le révèle l'analyse de CAS Collection de contenus (Figure 5). Même s'il semble au premier abord que les documents consacrés aux thérapeutiques soient les plus nombreux, le pourcentage général de documents est également réparti entre les deux applications.
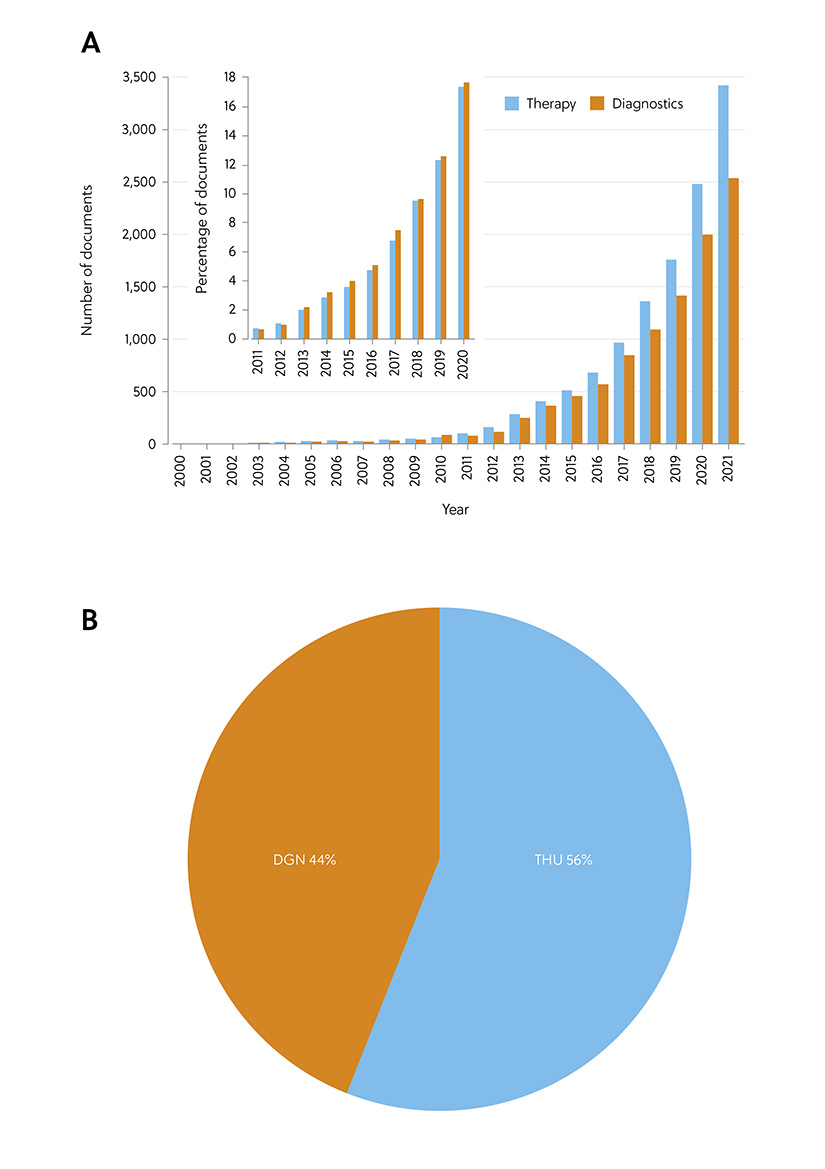
Figure 5. Application diagnostique ou thérapeutique des exosomes : (A) Comparaison du nombre de documents liés aux applications thérapeutiques vs diagnostiques des exosomes ; Encadré : Croissance annuelle du nombre de documents concernant les applications thérapeutiques vs diagnostiques des exosomes. (B) Comparaison du nombre de documents liés aux applications thérapeutiques vs diagnostiques des exosomes en ce qui concerne les indicateurs de leur rôle (THU, thérapeutique ; DGN, diagnostique).
Même si les recherches actuelles sur la thérapie par exosomes sont prometteuses, de nombreuses études restent en phase préclinique. Cela dit, sommes-nous proches d'une utilisation du plein potentiel des exosomes dans la thérapeutique et les diagnostics ? Quels sont les obstacles et les défis qui se dressent sur notre chemin ? Dans notre dernier article de cette série, nous découvrirons les acteurs majeurs de la recherche sur les exosomes et des mises à jour sur les initiatives de recherche clés dans ce domaine fascinant et dynamique. En attendant, vous pourrez en savoir plus dans notre rapport Insight sur les exosomes.



