
Un gran logro en el campo de la nanotecnología acelera la producción de vacunas
Aunque han seguido surgiendo focos de COVID-19 provocados por las variantes delta, los datos corroboran que las vacunas son eficaces para prevenir la hospitalización y la muerte. A pesar de que ya se han administrado más de 4000 millones de dosis de vacunas en todo el mundo, solo el 27 % de la población mundial y el 1,1 % de los habitantes de los países de renta baja han recibido al menos una dosis de la vacuna de la COVID-19. Si bien la producción y distribución de estas vacunas se enfrenta a numerosos obstáculos a lo largo de la cadena de suministro (refrigeración, costes y transporte), uno en concreto es la producción de nanopartículas lipídicas para las vacunas.
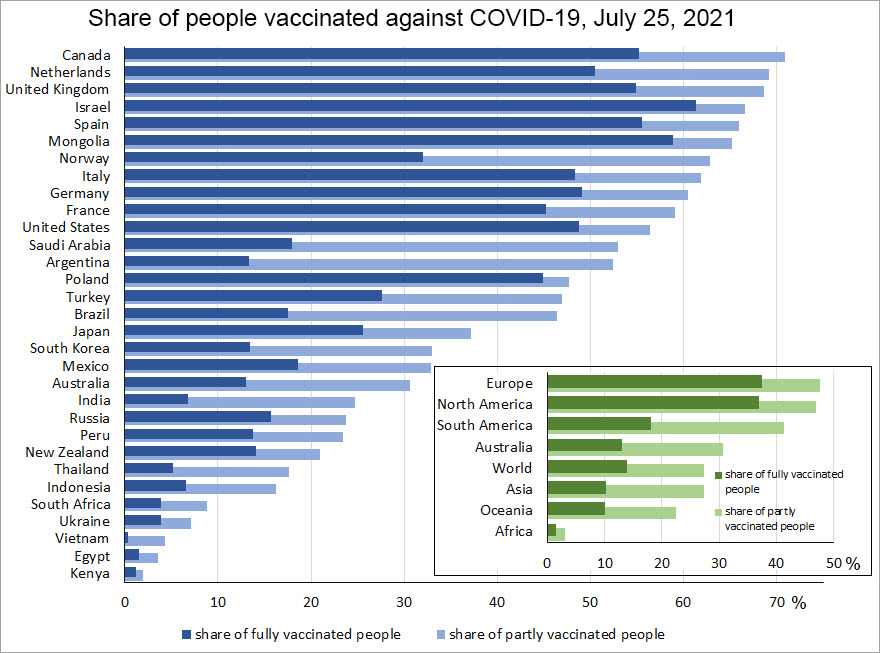
Figura 1: desglose de la proporción de personas vacunadas por país y continente
¿Por qué las nanopartículas lipídicas son esenciales para los agentes terapéuticos de ARNm?
La administración de agentes terapéuticos de ARNm en el cuerpo humano supone un gran desafío debido a las propiedades y la inestabilidad característica de los ácidos nucleicos:
- La carga negativa y la hidrofilia impiden la difusión pasiva a través de las biomembranas.
- La unión a determinadas proteínas séricas, la captación por parte de los fagocitos y la degradación por acción de las nucleasas endógenas son factores que restringen la eficacia de la administración.
- Por este motivo, se requieren vectores de entrega que, por una parte, protejan a los ácidos nucleicos de la degradación y, por otra, permitan su llegada a las células diana para que la administración sea eficaz.
El uso de nanopartículas lipídicas (NPL) es un método eficaz para proteger y transportar el ARNm a las células, como se ha constatado en el caso de las nuevas vacunas de ARNm para la COVID-19.
La producción de vacunas está limitada por la producción de nanopartículas lipídicas
Si el incremento de la producción de cualquier tratamiento ya es difícil, la producción de estas nanopartículas lipídicas para satisfacer la demanda mundial de vacunas es un reto incluso más importante. La síntesis de los lípidos catiónicos ionizables exclusivos, desarrollados y optimizados específicamente para estas vacunas, es un proceso complejo que consta de varios pasos. Con todo, la producción a gran escala de NPL se enfrenta a un obstáculo incluso mayor: la tarea de combinar los lípidos y el ARNm en las nanopartículas.
La técnica de elaboración es de suma importancia para la producción eficiente de un producto farmacéutico. Con los métodos tradicionales de producción de NPL —que incluyen las fases de hidratación en película fina, evaporación en fase invertida, inyección de disolvente y eliminación de detergente—, se suelen obtener partículas grandes (>100 nm) y heterogéneas con una baja eficiencia de encapsulación, por lo que se precisa un paso adicional de reducción del tamaño, por ejemplo, extrusión o sonicación. Además, estos métodos son difíciles de aplicar a gran escala y no son reproducibles sistemáticamente.
Un nuevo enfoque: la tecnología de microfluidos
En los últimos tiempos, la tecnología de microfluidos se ha revelado como un método eficaz para la producción de NPL. El método de la tecnología de microfluidos consiste en hacer pasar una corriente de una solución de lípidos en alcohol por un canal al que más adelante envuelve una corriente coaxial de una fase acuosa (figura 2A). La difusión recíproca del alcohol y el agua a través de la interfase alcohol/agua provoca que los lípidos precipiten y se agrupen en NPL. Las técnicas de microfluidos son fiables, ampliables y altamente reproducibles. En el caso de la formulación de vacunas de ARNm, la mezcla lipídica incluye un lípido catiónico ionizable, así como un lípido PEGilado y lípidos auxiliares (fosfatidilcolina, colesterol), y la fase acuosa contiene el ácido nucleico. El lípido catiónico interactúa con el ácido nucleico con carga negativa, lo que da lugar a NPL de alta eficiencia de encapsulación. Es posible producir LNP de tamaños de partícula definidos y con una distribución estricta del tamaño de partícula mediante el control exacto de los parámetros de la tecnología de microfluidos, como la velocidad de flujo y las proporciones de los componentes. Sin embargo, el rendimiento del proceso es limitado (
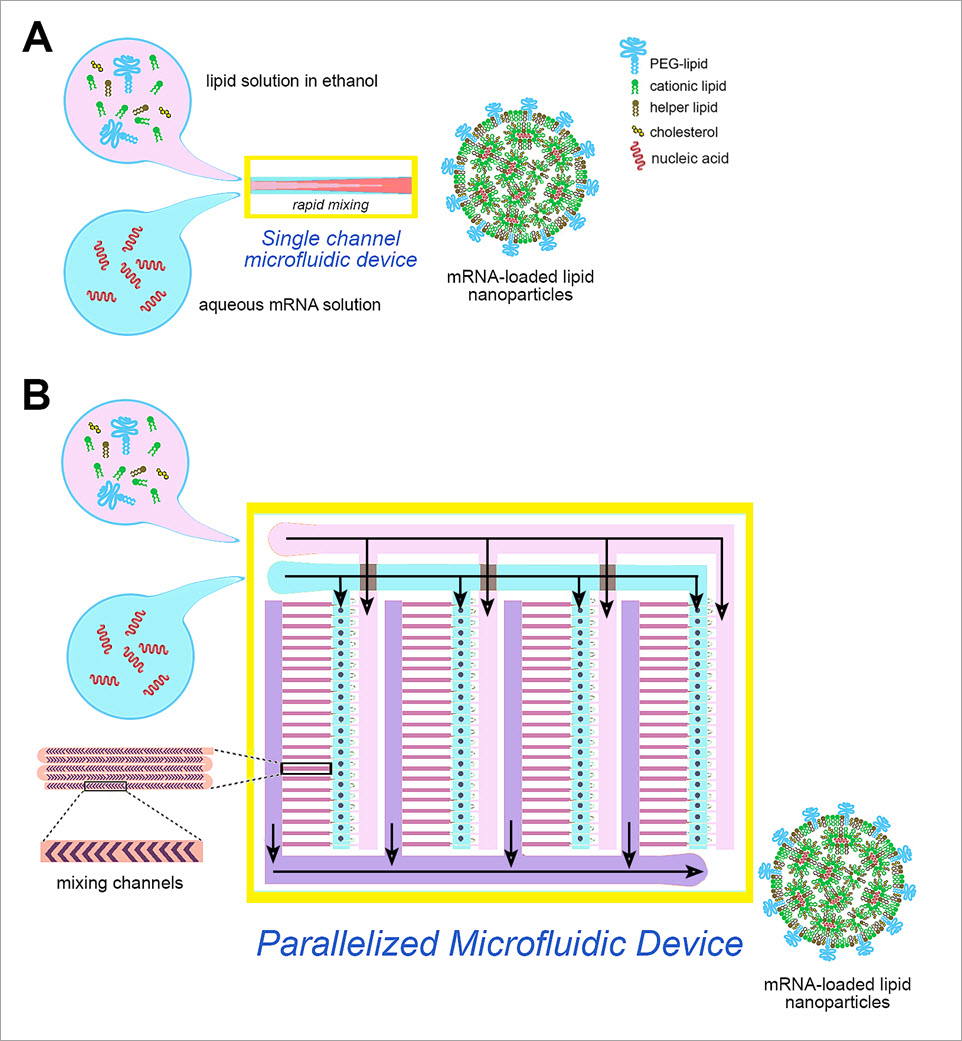
Figura 2. Dispositivo de microfluidos de un solo canal (A) e innovador dispositivo de microfluidos paralelizado (B) compuesto por 128 microcanales de mezcla que trabajan en paralelo
Los resultados preliminares son prometedores
El reciente desarrollo de una nueva tecnología de fabricación ha permitido multiplicar por más de cien los volúmenes actuales de producción de microfluidos. En este sentido, se ha desarrollado un dispositivo de microfluidos que consta de 128 microcanales de mezcla que funcionan en paralelo —un dispositivo de microfluidos paralelizado— que utiliza una tecnología de plataforma de integración de microfluidos a enorme escala (VLSMI). En los microcanales se mezclan cantidades exactas de lípidos y ARNm y el resultado son nanopartículas lipídicas cuyo tamaño y cantidad de ARNm encapsulado se pueden controlar con precisión. Este dispositivo, cuyo rendimiento es cien veces superior al de un dispositivo de microfluidos de un solo canal (18,4 l/h), tiene otra ventaja extraordinaria: la posibilidad de ampliarlo aún más para permitir la producción industrial de nanopartículas lipídicas portadoras de ARN. Los resultados publicados indican que el dispositivo de microfluidos paralelizado produce nanopartículas lipídicas eficaces para su uso en agentes terapéuticos y vacunas basados en ARN de interferencia pequeño y ARNm.
La producción de nanopartículas lipídicas propiciará el desarrollo de más tratamientos de ARNm
El desarrollo de estas vacunas y otros tratamientos podría suponer toda una revolución médica de la mano de las tecnologías de edición genética y los agentes terapéuticos de sustitución de proteínas. En la actualidad, se están llevando a cabo ensayos clínicos para evaluar varias vacunas de ARNm basadas en NPL frente a diversas enfermedades infecciosas, como las vacunas de ARNm modificado con nucleósidos para el virus del Zika, el citomegalovirus, la tuberculosis y la gripe. Las vacunas terapéuticas de ARNm ofrecen muchas posibilidades en el ámbito de la inmunoterapia contra los melanomas, el cáncer de ovario, el cáncer de mama y otros tumores sólidos.
El uso de ARNm para la expresión de proteínas terapéuticas es muy prometedor para el tratamiento de una amplia gama de enfermedades mediante la aplicación de una terapia de sustitución de proteínas. Esta nueva tecnología de fabricación de microfluidos responde a la necesidad clínica de contar con un proceso de producción de NPL ampliable, muy preciso y reproducible que permita la formulación rápida de NPL para una extensa gama de agentes terapéuticos y vacunas de ARN. Aunque es posible que esto, por sí solo, no resuelva el desafío de la distribución mundial, sin duda constituye un avance fundamental para esta nueva generación de posibles curas y vacunas que el ARNm puede impulsar.
