
ナノテクノロジーの飛躍的進歩がワクチン生産を加速
デルタ株の出現により、COVID-19のホットスポットはいまだ継続的に発生している反面、データは依然として予防接種が入院や死亡を防ぐのに効果的であることを示しています。 世界中では40億回分以上のワクチンが投与されましたが、このCOVID-19ワクチンの接種を1回以上受けたのは、世界人口の27%、低所得国では人口のわずか1.1%にすぎません。 これらワクチンの製造と流通にはサプライチェーンの点で数多くの課題がありますが(冷蔵、コスト、そして輸送など)、その中でも特に顕著なのはワクチン用の脂質ナノ粒子の製造です。
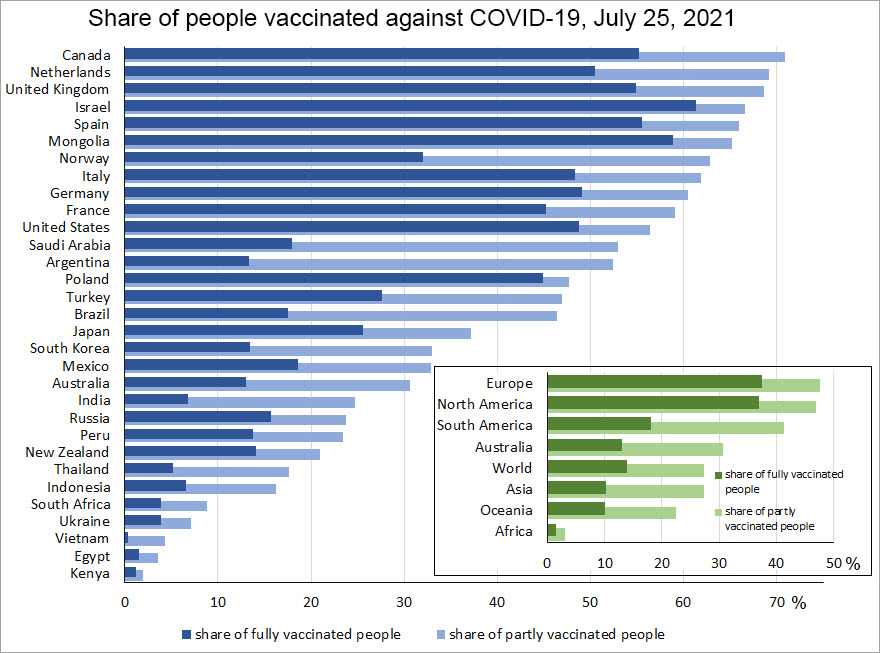
図1:ワクチン接種済の人口割合、国および大陸別の内訳
mRNA治療薬には、なぜ脂質ナノ粒子が不可欠なのですか。
mRNA治療薬の人体への送達は、核酸に固有の不安定性や、以下などの特性により、長い間大きな課題でした。
- その負電荷と親水性により、生体膜間の受動拡散が妨げられてしまう
- 血清タンパク質との結合、食細胞による摂取、内因性ヌクレアーゼによる分解で、効率的な送達が妨げられてしまう
- 分解から保護し、標的細胞に送達して効率的に取り込まれるためには、送達ベクターが必要になる
最近のmRNA COVID-19ワクチンに見られるように、脂質ナノ粒子(LNP)は、mRNAを効果的に保護して細胞に送達するのに優れていることが証明されました。
ワクチンの生産は脂質ナノ粒子の生産量に制限される
どんな治療薬であれ、その生産規模を拡大することは困難ですが、しかしワクチンの世界的な需要に対応できるような脂質ナノ粒子の生産は、さらに大きな課題です。 これらのワクチン用に特別に開発および最適化された独自のイオン化可能な陽イオン性脂質の合成は、複雑な多段階プロセスです。 ところが、LNPを大規模に製造するには、さらに大きな課題があります。脂質とmRNAを組み合わせてナノ粒子にするという課題です。
実際、製剤の効率的な製造には、その製造技術が最も重要です。 従来のLNP製造方法には、薄膜水和や逆相蒸発、溶媒注入、界面活性剤除去などがありますが、一般的にカプセル化収率が低く、大きく(> 100 nm)不均一な粒子となるなど、押し出しまたは超音波処理といった追加の縮小処理手順を必要とします。 さらに、これらの方法はスケールアップが難しく、一貫した再現性がありません。
マイクロ流体力学という新たな手法
近年LNPの製造ではマイクロ流体力学が成功を収めています。 マイクロ流体フォーカシング法では、アルコール中の脂質溶液の流れを、水相の同軸の流れと交差して覆われている流路を通過させます(図2A)。 アルコール・水の界面間におけるアルコールと水の相互拡散により、脂質が沈殿し、自己組織化してLNPになります。 マイクロ流体技術は、ロバストでスケーラブルであり、また高度に再現性のある技術です。 mRNAワクチン製剤の場合、脂質混合物には、イオン化可能な陽イオン性脂質、PEG-脂質、ヘルパー脂質(ホスファチジルコリン、コレステロール)が含まれる一方、水相には核酸が含まれます。 陽イオン性脂質は負に帯電した核酸と相互作用し、高いカプセル化効率のLNPをもたらします。 定義済みのサイズと狭いサイズのLNPの分布は、流量や成分比などのマイクロ流体操作パラメータを正確に制御することで生成できます。 ただし、この処理のスループットには制限があり(
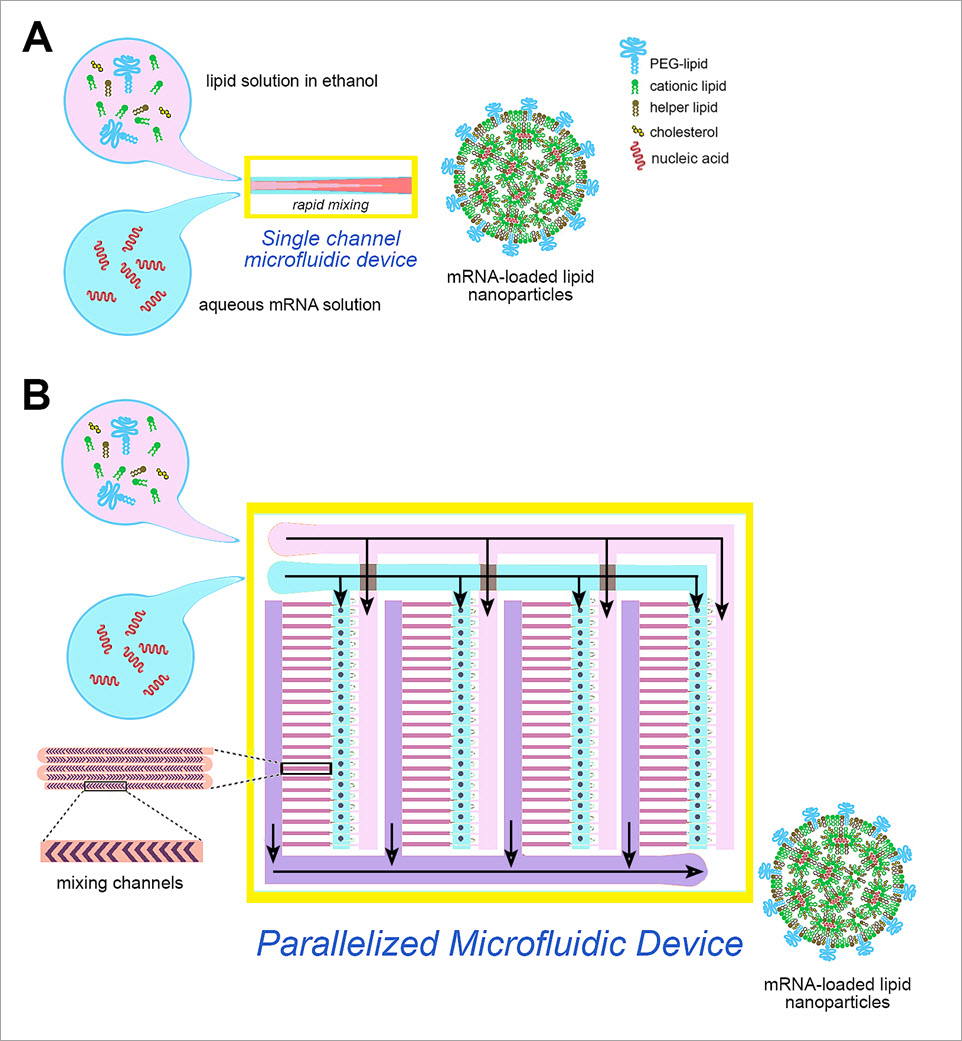
図2 シングルチャネルのマイクロ流体デバイス(A)と128個のマイクロミキシングチャネルを含む新しい並列化イクロ流体デバイス(B)
期待できる初期の結果
最近の製造技術の飛躍的進歩により、現在のマイクロ流体による生産率で100倍以上の向上が実現しました。 128個の並列マイクロミキシングチャネルを含んだマイクロ流体デバイスが構築されています。これは非常に大規模なマイクロ流体統合(VLSMI)プラットフォーム技術を使用した並列マイクロ流体デバイスです。 チャネルは正確な量の脂質とmRNAを混合し、正確に制御されたサイズと量のカプセル化されたmRNAの脂質ナノ粒子を製造します。 このデバイスは、単一チャネルのマイクロ流体デバイスの100倍以上のスループット(18.4 L/h)があり、更なる規模拡大の可能性があるため、RNAを運ぶ脂質ナノ粒子の大量生産が可能になります。 公表された結果では、並列マイクロ流体デバイスは、siRNAおよびmRNAベースの治療薬およびワクチンでの使用に効果的な脂質ナノ粒子を生産することを示しています。
脂質ナノ粒子の生産でさらに多くのmRNA治療法が可能に
こういったワクチンや治療法の開発は、遺伝子編集やタンパク質置換治療によって医学に革命を起こす可能性を秘めています。 現在、LNPベースのmRNAワクチンは、ジカウイルスやサイトメガロウイルス、結核、そしてインフルエンザなどに対するヌクレオシド修飾mRNAワクチンなど、さまざまな感染症で臨床試験に入っています。 mRNA治療ワクチンは、黒色腫や卵巣癌、乳癌、およびその他の固形腫瘍に対する癌免疫療法において大きな可能性を秘めています。
治療薬のタンパク質の発現に対するmRNAの使用は、タンパク質補充療法の適用により、幅広い疾患の治療に大きな期待が持てます。 この新しく開発されたマイクロ流体製造技術は、拡張可能かつ高精度で再現性のあるLNP生成の臨床的ニーズに対応し、幅広いRNA治療薬やワクチン用のLNPの迅速な処方を可能にします。 これだけでは世界的な流通の課題を解決できませんが、mRNAが解き放つ可能性のある潜在的な治療法とワクチンの新時代における重要な進歩と言えます。
