La producción de plásticos baratos, duraderos y adaptables se ha multiplicado en las últimas décadas a medida que estos materiales se han infiltrado en todas las facetas de nuestras vidas. Sin embargo, este polímero, antes tan popular, tiene un lado oscuro. El plástico puede tardar cientos de años en degradarse. Dado que se producen cantidades astronómicas (más de 350 millones de toneladas cada año en todo el mundo), la contaminación por plástico es actualmente uno de los problemas medioambientales más apremiantes en nuestro planeta.
Un volumen mareante de plástico —150 millones de toneladas— llega cada año a los vertederos o se libera al medioambiente, y más de 8 millones de toneladas son transportadas por los ríos hasta el océano. La mayor parte de este volumen no se degrada, solo se fragmenta generando micropartículas. Estos microplásticos, sobradamente documentados, se pueden encontrar en el agua del mar, en el interior de los animales marinos e incluso en el sistema digestivo de los humanos. La contaminación por plástico es hoy en día uno de los problemas medioambientales más graves de la humanidad, y los investigadores no han escatimado esfuerzos para encontrar soluciones a esta difícil cuestión.
Despolimerización: la solución al problema del reciclaje de polímeros
Los plásticos están hechos de polímeros: cadenas largas creadas mediante la repetición de monómeros. La mayoría de los plásticos de uso general son termoplásticos o termoestables. Los termoplásticos, como el acrílico, la poliamida y el polietileno, se vuelven blandos y moldeables a temperaturas elevadas y se endurecen cuando se enfrían. Esta propiedad hace que sean relativamente fáciles de reciclar, porque se pueden reblandecer y moldear otra vez para crear nuevos productos, aunque el deterioro de la calidad limita los beneficios. Los plásticos termoestables, como el poliuretano, la resina epoxi y la resina de melamina, se endurecen al calentarse y es prácticamente imposible reciclarlos. Las dificultades del reciclaje de los termoplásticos y los plásticos termoestables significan que, a la postre, ambos contribuirán a la contaminación medioambiental.
Para reciclarlos de manera eficaz y reutilizarlos en nuevos productos, los residuos de plástico se deben descomponer en sus monómeros originales por medio de un proceso denominado despolimerización. Es un avance técnico esencial para desarrollar una economía circular de los materiales a nivel global. En los sistemas biológicos, puede ser necesario descomponer los polímeros por completo en los monómeros que los integran para favorecer la absorción y el crecimiento microbianos.
Para lograr la despolimerización, los científicos han estudiado la naturaleza en busca de enzimas microbianas que puedan descomponer los plásticos. En 2012, un equipo de investigadores de la Universidad de Osaka descubrió en una pila de compost una enzima que descomponía uno de los plásticos más utilizados en el mundo: el tereftalato de polietileno (PET, CAS Registry Number 25038-59-9, fórmula (C10H8O4)n).
La enzima, conocida como cutinasa de compost de hojas y ramas (LCC), rompe los enlaces entre los monómeros del PET, pero no tolera la temperatura de 65 °C necesaria para ablandar el PET y se desnaturaliza tras varios días actuando a esta temperatura, lo que limita su utilidad industrial. Dado que la despolimerización solo se puede producir en el plástico fundido, las enzimas deben ser estables a temperaturas elevadas.
Despolimerización de PET de doble acción con una bacteria del suelo poco conocida
El PET es un termoplástico y uno de los poliésteres más usados. La producción mundial de PET pasó de los 42 millones de toneladas en 2014 a 50 millones de toneladas en 2016 y se espera que llegue a los 87 millones de toneladas en 2022.
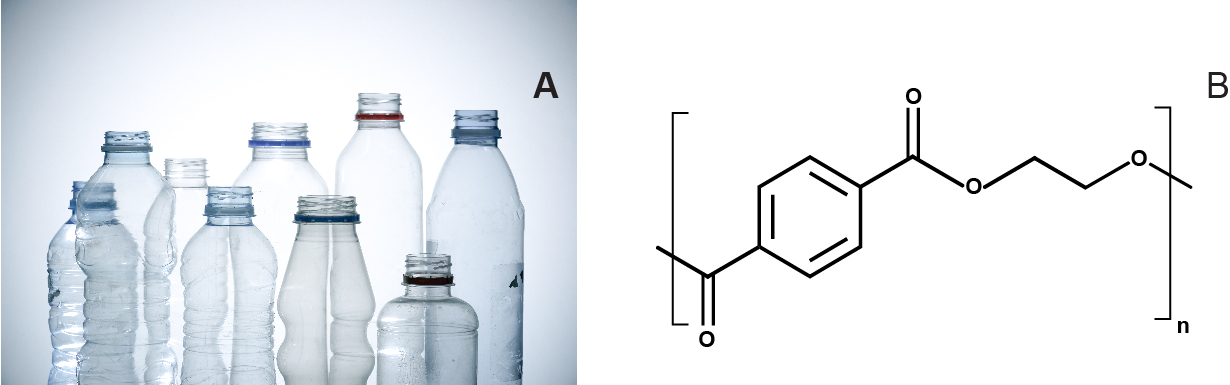
Este polímero sintético se fabrica a partir del ácido tereftálico derivado del petróleo (TPA) y el etilenglicol (EG). El PET es un polímero versátil que puede ser transparente, opaco o blanco dependiendo de su estructura cristalina y del tamaño de sus partículas (fig. 1). Se usa habitualmente para producir fibras para prendas de vestir y envases, incluidas las botellas de agua. El PET no orientado se puede termoformar (o moldear) para fabricar otros productos de envasado, como para los blísters1. Encontrar una manera eficaz de despolimerizar el PET será un paso clave en la lucha por reciclar el plástico y proteger el medioambiente.
La biodegradación del PET se ha estudiado a fondo porque las enzimas esterasas (enzimas que dividen los ésteres en un ácido y un alcohol) abundan en la naturaleza2. Sin embargo, se han documentado pocos casos de degradación biológica del PET o de su utilización para favorecer el crecimiento microbiano. Algunos organismos del grupo de los hongos filamentosos, como Fusarium oxysporum y Fusarium solani, se han desarrollado en un medio mineral que contenía hilos de PET3.
En 2016, Yoshida et al4 describieron el descubrimiento y la clasificación de la cepa bacteriana Ideonella sakaiensis 201-F6, que crecía en sedimentos contaminados con PET cerca de una planta de reciclaje de plástico de Japón. Esta bacteria gram negativa aeróbica con forma de varilla tiene la curiosa habilidad de usar el PET como su principal fuente de energía y de carbono para crecer.
La bacteria I. sakaiensis emplea un sistema de dos enzimas para despolimerizar el PET descomponiéndolo en sus elementos esenciales, el TPA y el EG, que a continuación se catabolizan produciendo una fuente de carbono y energía. Una de las dos enzimas, la proteína ISF6_4831, hidroliza y rompe las uniones de los ésteres. Muestra preferencia por los ésteres aromáticos en detrimento de los alifáticos y una inclinación clara hacia el PET, y se ha bautizado como PET hidrolasa (PETasa). La enzima PETasa de I. sakaiensis es una hidrolasa de serina similar a la cutinasa que ataca al polímero de PET y libera bis(2-hidroxietil) tereftalato (BHET), mono(2-hidroxietil) tereftalato (MHET) y TPA. A continuación, la PETasa descompone el BHET en MHET y EG. La segunda enzima, la proteína ISF6_0224 o MHET hidrolasa (MHETasa), hidroliza aún más el MHET soluble para producir TPA y EG (fig. 2). Las dos enzimas son necesarias, probablemente de forma sinérgica, para convertir el PET en sus dos monómeros benignos desde el punto de vista medioambiental, TPA y EG4, por acción enzimática, lo que hace posible un reciclaje completo del PET.
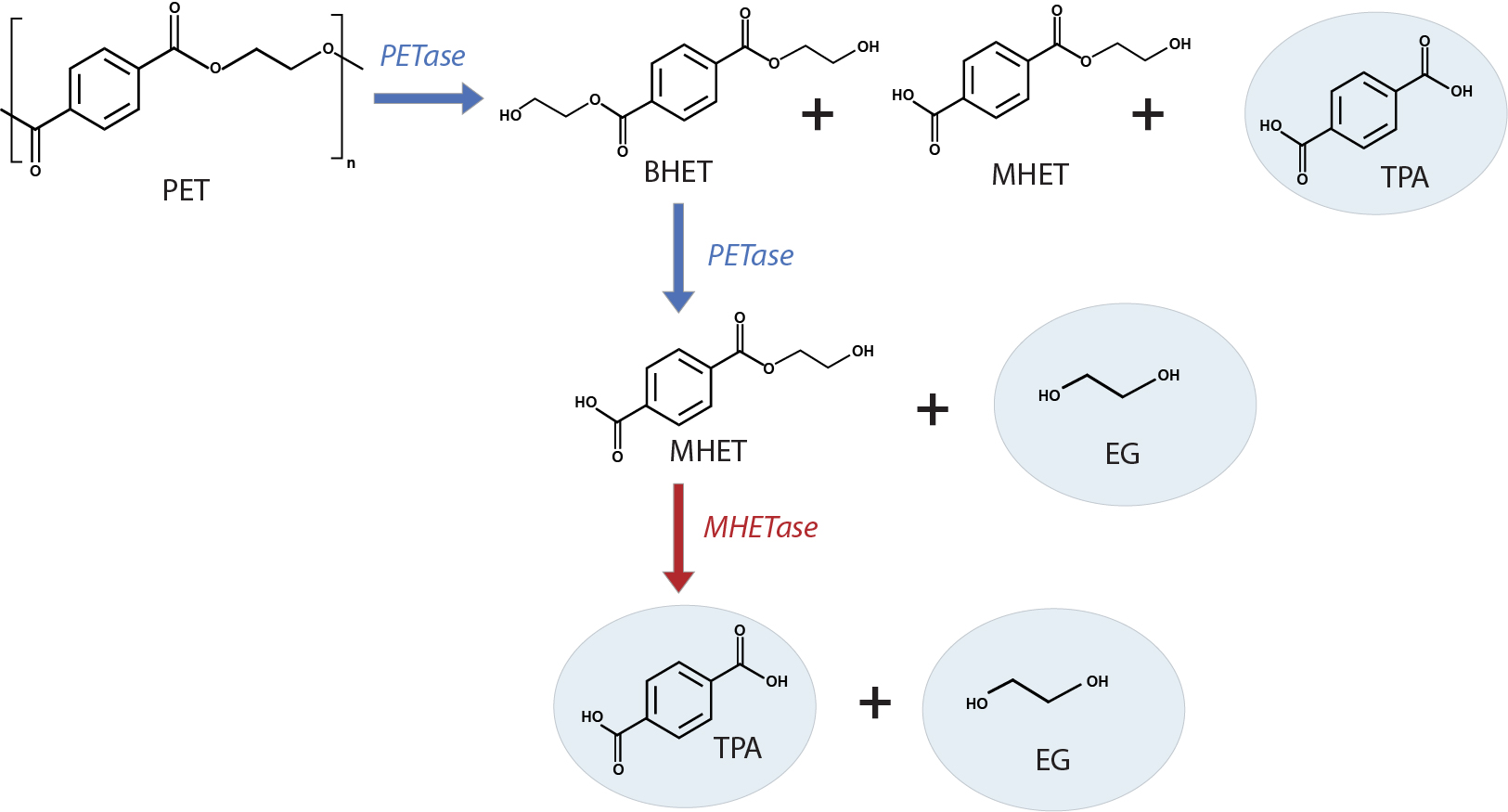
Fig. 2. Esquema de la despolimerización del PET: la PETasa cataliza la despolimerización del PET en bis(2-hidroxietil)-TPA (BHET), mono(2-hidroxietil) tereftalato (MHET) y ácido tereftálico (TPA). La MHETasa convierte el MHET en los monómeros TPA y etilenglicol (EG).
Una variante mutante de la PETasa potencia la degradación del PET
Los estudios de la secuencia y la estructura de la enzima PETasa han revelado similitudes con las enzimas cutinasas, desarrolladas por muchas bacterias para descomponer la cutina, un polímero ceroso natural que forma parte de la cutícula protectora de muchas plantas. El análisis de la estructura cristalina y los test bioquímicos han mostrado que la PETasa de I. sakaiensis 2 tiene una arquitectura de sitio activo abierta en el sitio de unión y que probablemente actúa siguiendo el mecanismo canónico de la catálisis de la serina hidrolasa5.
Partiendo de modificaciones estructurales de la PETasa y de una hendidura homóloga en el sitio activo de la cutinasa, se han producido variantes de la PETasa que se han probado en la degradación del PET, entre ellas una forma mutante con una mutación doble distal con respecto el centro catalítico. Se cree que esta área es capaz de corregir interacciones importantes de unión al sustrato6. Se ha descubierto que esta mutante doble, basada en la arquitectura de la cutinasa, tiene una capacidad de degradación del PET mayor que la de la PETasa en estado natural6 y se ha presentado una patente7.
Al estrechar la hendidura de unión mediante la mutación de dos residuos de sitios activos en las cutinasas, los investigadores han observado una mejora de la degradación del PET, lo que sugiere que la PETasa no tiene la estructura óptima para la degradación del PET cristalino, a pesar de desarrollarse en un entorno rico en PET. La enzima mutante solo necesita unos días para empezar a descomponer el plástico, un tiempo muy inferior a los siglos que dura este proceso en los océanos.
De una mutante doble a un cóctel doble de enzimas
Cuando se añade a la reacción la enzima MHETasa, la mezcla de enzimas descompone el PET dos veces más deprisa que la PETasa. La tendencia de degradación observada en el rango de cargas enzimáticas analizadas muestra niveles crecientes de los monómeros constituyentes a medida que aumenta la concentración de las dos enzimas. Esto indica que las reacciones están limitadas por las enzimas y no por el sustrato. El análisis de sinergia también indica que las velocidades de degradación aumentan con la carga de PETasa y que la presencia de MHETasa, incluso a una concentración baja comparada con la de PETasa, mejora la degradación total. Los experimentos actuales no indican una proporción óptima de la PETasa con respecto a la MHETasa.
La creación de una superenzima triplica la degradación del PET
En otros experimentos que exploran las propiedades y el alcance de la degradación del PET, los investigadores han creado una nueva superenzima uniendo la MHETasa y la PETasa en una sola cadena larga. Se han generado proteínas de fusión que unen de forma covalente el extremo C de la MHETasa al extremo N de la PETasa mediante conectores flexibles de glicina-serina y se han analizado para estudiar la degradación del PET amorfo (fig. 3). Cuando se compara el grado de degradación producido por diferentes enzimas, las proteínas de fusión superan el rendimiento de la PETasa y la MHETasa, así como el de la mezcla de enzimas sin unir.
Curiosamente, la superenzima no solo despolimeriza el PET, sino que también funciona en el PEF (furanoato de polietileno), un bioplástico derivado del azúcar que se usa en las botellas de cerveza.
La deconstrucción enzimática de algunos polímeros naturales, como la celulosa y la quitina, se produce en la naturaleza gracias a la acción de mezclas de enzimas secretadas por microbios que actúan de forma sinérgica8. Estos sistemas microbianos naturales han evolucionado a lo largo del tiempo para optimizar la degradación de esos polímeros. Parece que algunas bacterias del suelo, como I. sakaiensis, han evolucionado de un modo similar para utilizar un sustrato de poliéster con un sistema de dos enzimas4,9. A diferencia de la degradación natural, que puede tardar siglos, la superenzima puede convertir el PET en sus monómeros en tan solo unos días, aunque, por ahora, el proceso sigue siendo demasiado lento para resultar viable comercialmente.
Reciclaje sin fin con la degradación del plástico
Al volver a transformar el PET en sus monómeros constituyentes originales, la superenzima permitiría fabricar y reutilizar los plásticos sin limitaciones y reduciría la dependencia de los recursos fósiles. Y los hallazgos no terminan aquí…
En 2020, varios científicos lograron un importante avance al identificar una enzima que podía degradar el PET en tan solo 10 horas10. La investigación evaluó una amplia variedad de bacterias y enzimas para identificar posibles candidatas, entre ellas la cutinasa de compost de hojas y ramas (LCC), que se descubrió en 2012. Posteriormente, se produjeron cientos de enzimas PET hidrolasas mutantes utilizando distintos aminoácidos en el sitio de unión y mejorando la estabilidad térmica. A continuación, se evaluaron los mutantes bacterianos para identificar los más eficientes en la descomposición del PET. Tras ejecutar múltiples veces este proceso, se aisló una enzima mutante que es 10 000 veces más eficiente en la degradación del PET que la LCC natural. Además, es estable a 72 °C, una temperatura cercana al punto de fusión del PET. Este hallazgo supone un importante paso adelante en los esfuerzos dirigidos a conseguir un reciclaje infinito del PET y ya se encuentra en su fase piloto a nivel industrial10.
Y esto no es más que la punta del iceberg de las posibilidades que ofrecen estos organismos y sus enzimas. La mayoría de los plásticos son derivados de los combustibles fósiles, finitos en su creación pero ubicuos en nuestro entorno. La contaminación por plástico seguirá siendo un problema creciente a menos que encontremos la forma de crear una economía circular. Dentro de pocas décadas, no podremos producir los artículos de plástico que necesitamos si no logramos reciclar los residuos que ya existen. El reciclaje tradicional no es ni eficaz ni sostenible y, a menos que descompongamos los plásticos en sus monómeros constituyentes a escala industrial, no podemos esperar que se resuelva este problema. Por suerte, con la ayuda de la naturaleza, una evolución inteligente y una pizca de inventiva científica, quedan esperanzas de solucionarlo.
¿Le gustaría aprender más sobre las innovaciones "verdes"?
En la búsqueda de nuevas especies para impulsar la innovación, ningún rincón del planeta contiene tanta diversidad como la selva tropical de Brasil. Descubra cómo se están recopilando y extrayendo datos para uso público, y cómo puede ayudar esto a proteger entre el 15 y el 20 % de la biodiversidad de la Tierra.
(Lea Organizar los datos esenciales para impulsar la innovación basada en la biodiversidad de Brasil).
REFERENCIAS
(1) Pasbrig, E.; Claessens, P.; Walker, R. I.; Walker, R. Peelable cover film for pharmaceutical packaging, e.g. blister packs, comprises paper, aluminum foil or heat-resistant plastic, a layer of special plastic film, mesh or fabric, a layer of aluminum foil and a heat-sealing layer. EP1767347-A1; WO2007038488-A2; EP1928654-A2; AU2006294788-A1; US2008251411-A1; CN101316702-A; CA2623586-A1; JP2009509874-W; TW200727887-A; MX2008004201-A1; IN200801248-P2; ZA200802826-A; BR200616412-A2; WO2007038488-A3; EP1928654-A4.
(2) Han, X.; Liu, W. D.; Huang, J. W.; Ma, J. T.; Zheng, Y. Y.; Ko, T. P.; Xu, L. M.; Cheng, Y. S.; Chen, C. C.; Guo, R. T., Structural insight into catalytic mechanism of PET hydrolase. Nature Communications 2017, 8. DOI: 10.1038/s41467-017-02255-z
(3) Nimchua, T.; Eveleigh, D. E.; Sangwatanaroj, U.; Punnapayak, H., Screening of tropical fungi producing polyethylene terephthalate-hydrolyzing enzyme for fabric modification. J. Ind. Microbiol. Biotechnol. 2008, 35 (8), 843-850. DOI: 10.1007/s10295-008-0356-3
(4) Yoshida, S.; Hiraga, K.; Takehana, T.; Taniguchi, I.; Yamaji, H.; Maeda, Y.; Toyohara, K.; Miyamoto, K.; Kimura, Y.; Oda, K., A bacterium that degrades and assimilates poly(ethylene terephthalate). Science 2016, 351 (6278), 1196-1199. DOI: 10.1126/science.aad6359
(5) Rauwerdink, A.; Kazlauskas, R. J., How the Same Core Catalytic Machinery Catalyzes 17 Different Reactions: the Serine-Histidine-Aspartate Catalytic Triad of alpha/beta-Hydrolase Fold Enzymes. Acs Catalysis 2015, 5 (10), 6153-6176. DOI: 10.1021/acscatal.5b01539
(6) Austin, H. P.; Allen, M. D.; Donohoe, B. S.; Rorrer, N. A.; Kearns, F. L.; Silveira, R. L.; Pollard, B. C.; Dominick, G.; Duman, R.; El Omari, K.; Mykhaylyk, V.; Wagner, A.; Michener, W. E.; Amore, A.; Skaf, M. S.; Crowley, M. F.; Thorne, A. W.; Johnson, C. W.; Woodcock, H. L.; McGeehan, J. E.; Beckham, G. T., Characterization and engineering of a plastic-degrading aromatic polyesterase. Proc. Natl. Acad. Sci. U. S. A. 2018, 115 (19), E4350-E4357. DOI: 10.1073/pnas.1718804115
(7) Beckham, G. T.; Johnson, C. W.; Donohoe, B. S.; Rorrer, N.; McGeehan, J. E.; Austin, H. P.; Allen, M. D. New modified polyethylene terephthalate -digesting enzyme comprising amino acid mutation of an active site residue, is used to degrade a polymer e.g. polyester, aromatic polymer or semi-aromatic polymer and polyethylene terephthalate. WO2019168811-A1.
(8) Payne, C. M.; Knott, B. C.; Mayes, H. B.; Hansson, H.; Himmel, M. E.; Sandgren, M.; Stahlberg, J.; Beckham, G. T., Fungal Cellulases. Chem. Rev. 2015, 115 (3), 1308-1448. DOI: 10.1021/cr500351c
(9) Taniguchi, I.; Yoshida, S.; Hiraga, K.; Miyamoto, K.; Kimura, Y.; Oda, K., Biodegradation of PET: Current Status and Application Aspects. Acs Catalysis 2019, 9 (5), 4089-4105. DOI: 10.1021/acscatal.8b05171
(10) Tournier, V.; Topham, C. M.; Gilles, A.; David, B.; Folgoas, C.; Moya-Leclair, E.; Kamionka, E.; Desrousseaux, M. L.; Texier, H.; Gavalda, S.; Cot, M.; Guémard, E.; Dalibey, M.; Nomme, J.; Cioci, G.; Barbe, S.; Chateau, M.; André, I.; Duquesne, S.; Marty, A., An engineered PET depolymerase to break down and recycle plastic bottles. Nature 2020, 580 (7802), 216-219. DOI: 10.1038/s41586-020-2149-4