Gain new perspectives for faster progress directly to your inbox.
Imaginez un monde où la bataille contre le cancer ne s'appuierait plus sur uniquement sur les instruments brutaux de la chimiothérapie et de la radiothérapie qui, même s'ils sont efficaces, entraînent souvent des inconvénients majeurs pour le bien-être des patients. Le traitement par immuno-oncologie (IO) a marqué l'entrée dans une nouvelle ère en exploitant les défenses internes de l'organisme pour combattre les cellules cancéreuses et s'est déjà avéré efficace dans le traitement des cancers de la vessie, du sein et des cancers colorectaux, entre autres.
Comme tout domaine d'avant-garde, le paysage de la thérapie par IO est vaste et possède de multiples facettes. Non limité à une approche particulière, il englobe un riche ensemble de méthodologies et de stratégies visant à augmenter notre réponse immunitaire. Des médicaments qui renforcent le système immunitaire et galvanisent les défenses de notre organisme aux anticorps monoclonaux, qui ciblent des protéines spécifiques liées au cancer, l'immunothérapie contre le cancer est un domaine dynamique qui ne connaît pas de limites.
Nous avons exploité toute l'étendue de CAS Collection de contenus™, la plus grande base de données pluridisciplinaire de documents et de substances compilée par des humains afin de découvrir les tendances et les concepts émergents dans ce vaste domaine en évolution rapide. On a assisté récemment à une augmentation régulière de l'intérêt pour l'immunothérapie contre le cancer. (Figure 1).
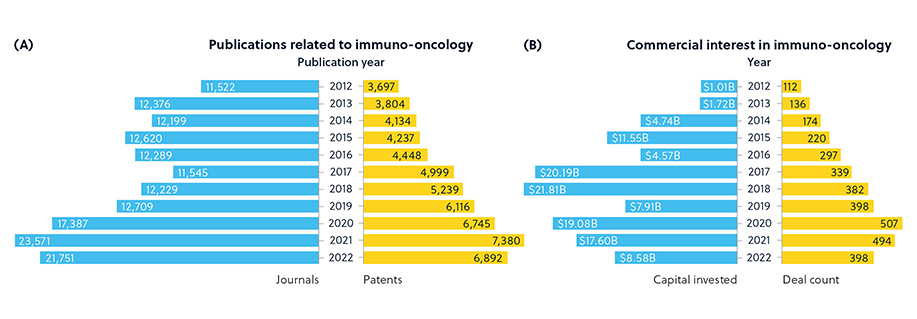
Exploration des tendances émergentes de l'immunothérapie contre le cancer
Une analyse approfondie des données issues de CAS Collection de contenus au sujet de l'immunothérapie contre le cancer a révélé un ensemble de données substantiel regroupant plus de 300 000 publications qui comprennent à la fois des journaux et des brevets consacrés à ce domaine. Cette analyse a exigé une approche méticuleuse, en commençant par l'élaboration d'une demande de recherche hautement spécifique de la part de spécialistes du sujet. Cette phase a été suivie d'un traitement du langage naturel, lequel a permis d'identifier des expressions, puis d'un examen manuel rigoureux de la part de nos spécialistes du domaine afin d'affiner lesdites expressions.
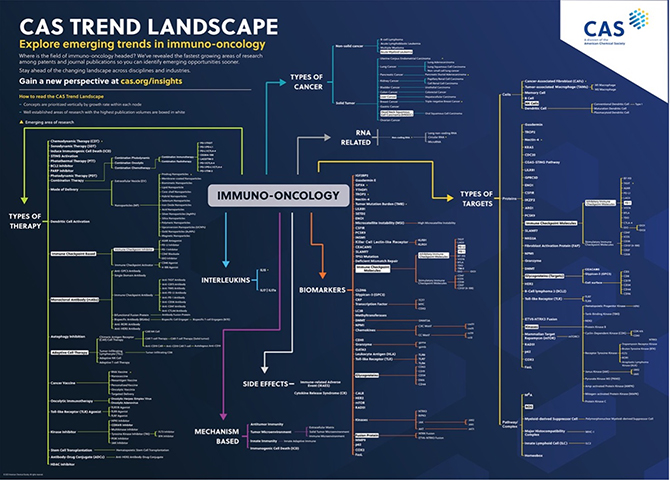
La question qui se pose naturellement est la suivante : qu'a révélé cette analyse complète des tendances et quelles sont les implications de ces résultats pour l'avenir de l'immunothérapie en oncologie ?
Inhibiteurs des points de contrôle : la pierre angulaire de l'immunothérapie contre le cancer
Les inhibiteurs de points de contrôle ont donné naissance à une révolution du paysage de l'oncologie, offrant des espoirs et des alternatives dans le traitement d'un large spectre de cancers. À ce titre, ces molécules recueillent la part du lion des publications.
Même si les inhibiteurs des points de contrôle immunitaires comme le récepteur 1 de mort cellulaire programmée (PD-1) et le ligand 1 de mort cellulaire programmée (PD-L1) sont largement utilisés dans la pratique clinique, les recherches en cours restent axées sur deux fronts majeurs : le développement de nouveaux inhibiteurs et le démantèlement des mécanismes sous-jacents de la résistance à ces thérapies révolutionnaires.
Toutefois, le développement de l'intérêt pour les différentes molécules inhibitrices des points de contrôle immunitaire reste irrégulier. Alors que les recherches sur des molécules telles que l'indoléamine 2,3-dioxygénase (IDO) et la protéine 4 cytotoxique associée aux lymphocytes T (CTLA-4) semblent augmenter lentement, d'autres, telles que le récepteur A2a de l'adénosine (A2AR), le gène 3 d'activation des lymphocytes (LAG-3), l'immunorécepteur de lymphocytes T avec domaines Ig et ITIM (TIGIT) et le B7-H3 présentent un potentiel de croissance rapide à l'avenir. Par conséquent, notre analyse du paysage des tendances offre des perspectives précieuses sur la trajectoire de ce domaine crucial de l'immunothérapie contre le cancer et enrichit notre compréhension de son potentiel.
Conjugués anticorps-médicaments, vaccins et au-delà : exploration des progrès supplémentaires de l'immunothérapie contre le cancer
L'immunologie contre le cancer a connu une évolution rapide au cours des 20 dernières années, avec des transformations des cibles émergentes au fil du temps (Figure 3). Une compréhension plus approfondie du rôle du système immunitaire dans le cancer a abouti au développement d'autres modalités majeures de traitement immunothérapeutique au-delà des inhibiteurs de points de contrôle, notamment la thérapie par lymphocytes T à récepteur (CAR), les conjugués anticorps-médicaments (ADC) et les vaccins contre le cancer.
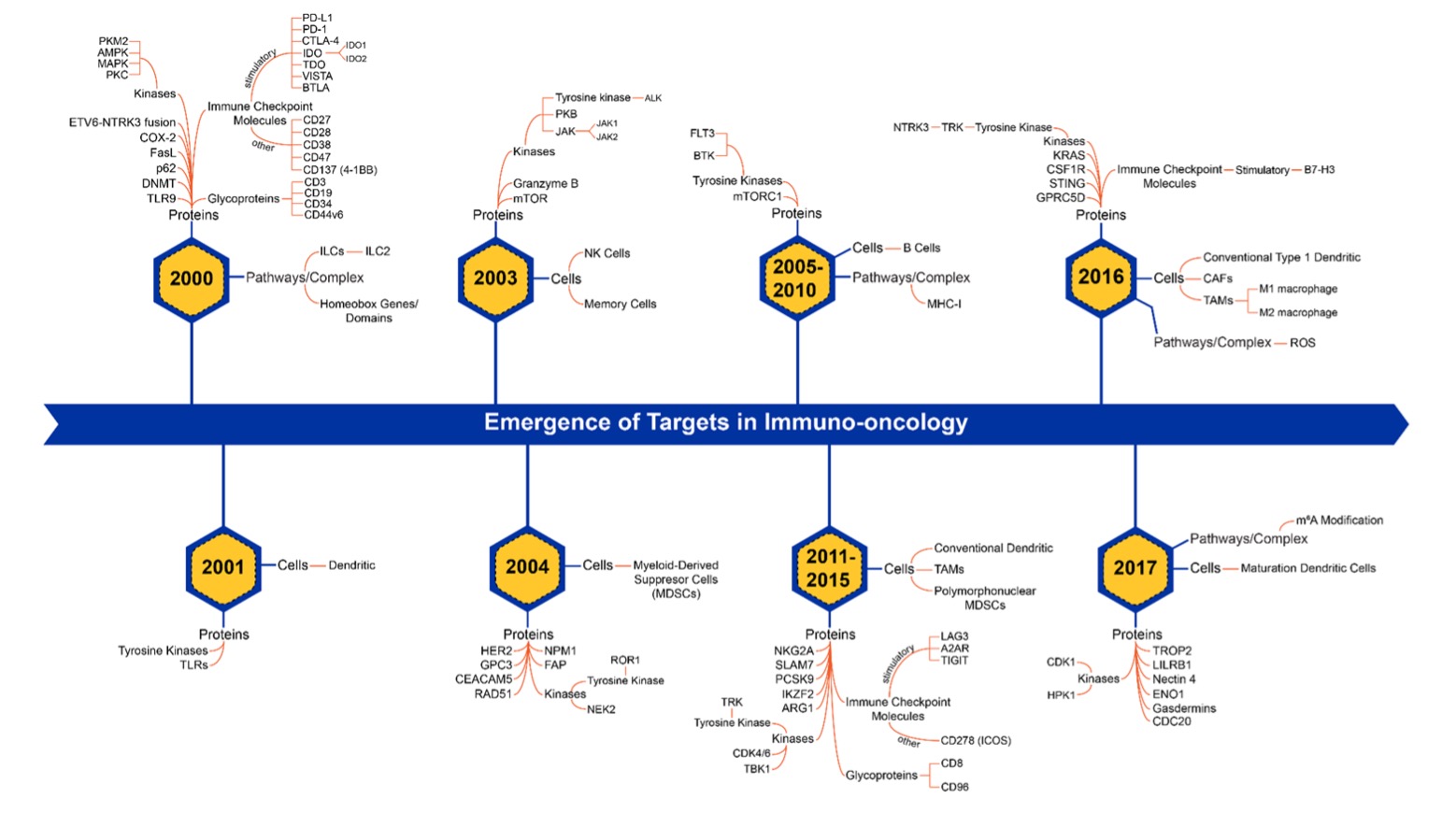
La thérapie par lymphocytes CAR-T implique la modification génétique des lymphocytes T du patient, pour leur permettre d'identifier et d'attaquer les cellules cancéreuses présentant des antigènes de surface spécifiques. On assiste depuis quelques années à une hausse rapide des publications sur les cellules CAR T, ce qui témoigne du rythme accéléré des progrès dans ce domaine, avec six thérapies cellulaires à cellules CAR-T déjà en cours d'utilisation.
| Nom | Antigène ciblé | Année d'approbation | Laboratoire | Maladie ciblée | CAS Numéro de registre (RN) |
| Kymriah (Tisagenlecleucel) | CD19 | 2017 | Novartis | Leucémie aiguë lymphoblastique (LAL) à cellules B et lymphome non-Hodgkinien (LNH) à cellules B | 1823078-37-0 |
| Yescarta (Axicabtagene ciloleucel) | CD19 | 2017 | Kite Pharma/Gilead | LNH à cellules B et lymphome folliculaire | 2086142-87-0 |
| Tecartus (Brexucabtagene autoleucel) | CD19 | 2020 | Kite Pharma/Gilead | LAL à cellules B et lymphome à cellules du manteau (LCM) | 2691112-12-4 |
| Breyanzi (Lisocabtagene maraleucel) | CD19 | 2021 | Juno Therapeutics, Bristol-Myers Squibb | LNH à cellules B | 2099722-39-9 |
| Abecma (Idecabtagene vicleucel) | Antigène de maturation des lymphocytes B (BCMA) | 2021 | Celgene Corporation, Bristol-Myers Squibb | Myélome multiple | 2306267-75-2 |
| Carvykti (Ciltacabtagene autoleucel) | BCMA | 2022 | Janssen Biotech | Myélome multiple | 2641066-71-7 |
Tableau 1. Traitements par cellules CAR-T approuvés par la FDA.
Les CAM sont apparus comme une autre force majeure de l'arsenal contre le cancer Ils donnent la priorité à une approche guidée par la précision, des anticorps monoclonaux s'associant à des médicaments cytotoxiques pour délivrer une cargaison puissante exclusivement au niveau des cellules cancéreuses. Le paysage des CAM reflète les progrès rapides des traitements par cellules CAR-T, avec un portefeuille de plus de 150 candidats uniques qui sont actuellement en phase d'essai clinique en plus des 14 CAM approuvés par la FDA et déjà en cours d'utilisation.
Les vaccins contre le cancer fonctionnent en programmant le système immunitaire pour qu'il s'attaque aux cellules cancéreuses « étrangères ». Notre analyse du paysage des tendances souligne la croissance continue des CAM et des traitements par cellules CAR-T et identifie les vaccins contre le cancer comme une tendance émergente, dans la mesure où les publications ont rapidement augmenté au cours des dernières années. Cela témoigne de l'élan sous-jacent à cette approche innovante, qui pourrait révolutionner la manière dont nous utilisons l'immunothérapie contre le cancer à l'échelle mondiale.
L'immunothérapie contre le cancer rencontre la nanomédecine : un paradigme changeant
L'efficacité des immunothérapies émergentes contre le cancer repose sur leur aptitude à atteindre avec précision les sites des tumeurs. Cette précision est obtenue grâce à des systèmes d'administration des médicaments ou des cellules, un composant essentiel pour l'optimisation de l'impact des traitements, tout en minimisant les effets hors cible. En outre, les systèmes d'administration des médicaments peuvent faciliter l'administration simultanée de multiples agents thérapeutiques. Cela ouvre la porte aux effets de synergie lorsqu'ils sont combinés avec d'autres traitements contre le cancer tels que la chimiothérapie, la radiothérapie ou d'autres traitements immuno-oncologiques.
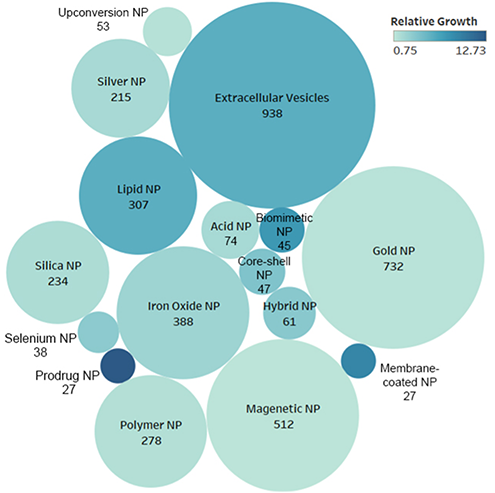
Depuis quelques années, les progrès de la science des matériaux et de la nanotechnologie ont donné naissance à différents nanomatériaux. Alors que les nanoparticules lipidiques étaient jusqu'à présent les principaux outils de l'administration d'immunothérapie, notre analyse du paysage des tendances révèle des développements prometteurs. Les systèmes d'administration de promédicaments, les conceptions biomimétiques et les nanoparticules encapsulées dans une membrane cellulaire apparaissent comme des nanotechnologies intéressantes.
L'avenir de l'immunothérapie contre le cancer : révélation de perspectives prometteuses
Dans le paysage en évolution constante de l'immuno-oncologie, le voyage est loin d'être terminé ; toutefois, il s'accélère à chaque pas. Chaque nouveau progrès permet de découvrir des cibles émergentes et des biomarqueurs qui pourraient dynamiser les innovations dans le domaine des traitements immuno-oncologiques. Ces découvertes fascinantes témoignent du potentiel inexploité de l'immunothérapie contre le cancer.
Pour en savoir plus sur le paysage en évolution constante de l'immuno-oncologie, veuillez consulter notre publication révisée par des pairs.



