Gain new perspectives for faster progress directly to your inbox.
假设有一个世界,在这个世界,抗癌斗争不再仅仅依赖于化疗和放疗这类粗暴手段。虽然这些手段很有效,但往往会对患者的健康造成高昂代价。 通过利用人体的先天防御功能来对抗癌细胞,免疫肿瘤 (IO) 疗法开创了一个新时代,并且已经在治疗膀胱癌、乳腺癌、结直肠癌等多种癌症中证明了其有效性。
与所有前沿领域一样,IO 疗法的前景兼具广阔性与多元性。 该疗法超越了单一的方法,包含了大量旨在增强免疫反应的不同方法和策略。 从激发人体防御功能的免疫增强药物,到针对特定癌症相关蛋白的单克隆抗体,癌症免疫疗法是一个不断发展、无限创新的领域。
CAS 内容合集™ 由人工编录而成,是规模最大的多学科文献和物质数据库,我们对该数据库开展了广泛的挖掘工作,旨在揭示这个快速发展广阔领域中出现的新兴趋势和概念。 最近,人们对癌症免疫疗法的兴趣稳定增长。 (图 1)。
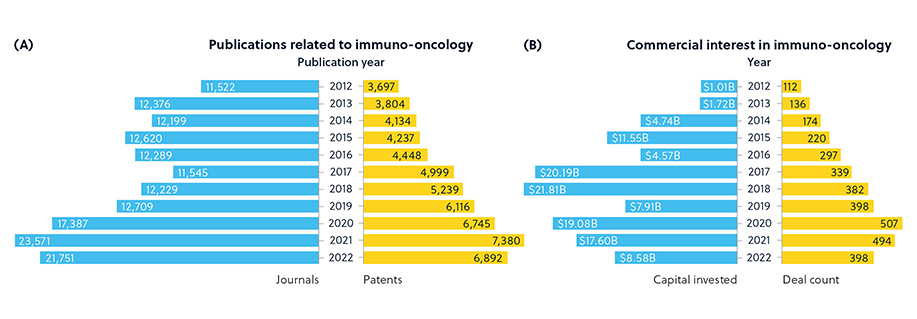
探索癌症免疫疗法的新兴趋势
通过对 CAS 内容合集中的癌症免疫疗法数据进行全面分析,我们获得了一个包含 350,000 多篇论文的庞大数据集,其中包括该领域的期刊和专利。 这项分析工作需要采用细致周密的方法,首先由主题专家 (SME) 拟定高度具体的检索词。 然后进行自然语言处理,识别短语,并由我们的 SME 进行严格的人工审查,对这些短语加以微调。
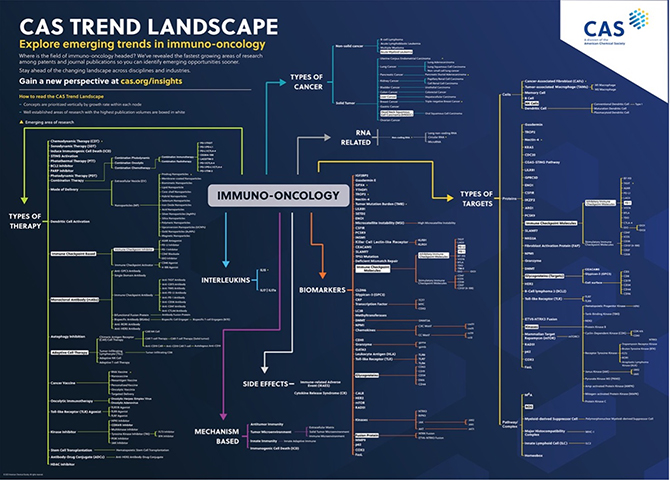
问题自然而言也随之产生:这项全面的趋势分析揭示了什么?对于肿瘤免疫疗法的未来有何影响?
检查点抑制剂: 癌症免疫疗法的基石
免疫检查点抑制剂引发了肿瘤学领域的变革,为治疗各种癌症带来了新希望和多种替代选择。 因此,出版物中有很大一部分都与这些分子有关。
虽然免疫检查点抑制剂,如程序性细胞死亡 1 受体 (PD-1) 和程序性细胞死亡配体 1 (PD-L1) 抑制剂已广泛应用于临床实践,但当前研究仍集中在两个关键方面:开发新型抑制剂,以及揭示这类革新疗法因何产生耐药性。
然而,人们对各种抑制性免疫检查点分子的兴趣并未持续增长。 针对吲哚胺 2,3-二氧化酶 (IDO) 和细胞毒性 T 淋巴细胞相关蛋白 4 (CTLA-4) 等分子的研究似乎增长缓慢,而针对腺苷 A2a 受体 (A2AR)、淋巴细胞活化基因 3 (LAG-3)、T 细胞免疫球蛋白和 ITIM 结构域蛋白 (TIGIT) 和 B7-H3 等其他分子的研究则显示出未来快速增长的潜力。 因此,我们的趋势格局分析针对关键癌症免疫治疗领域的发展轨迹提供了宝贵的见解,丰富了我们对其潜力的认识。
抗体药物偶联物、疫苗及其他: 探索癌症免疫疗法的进一步发展
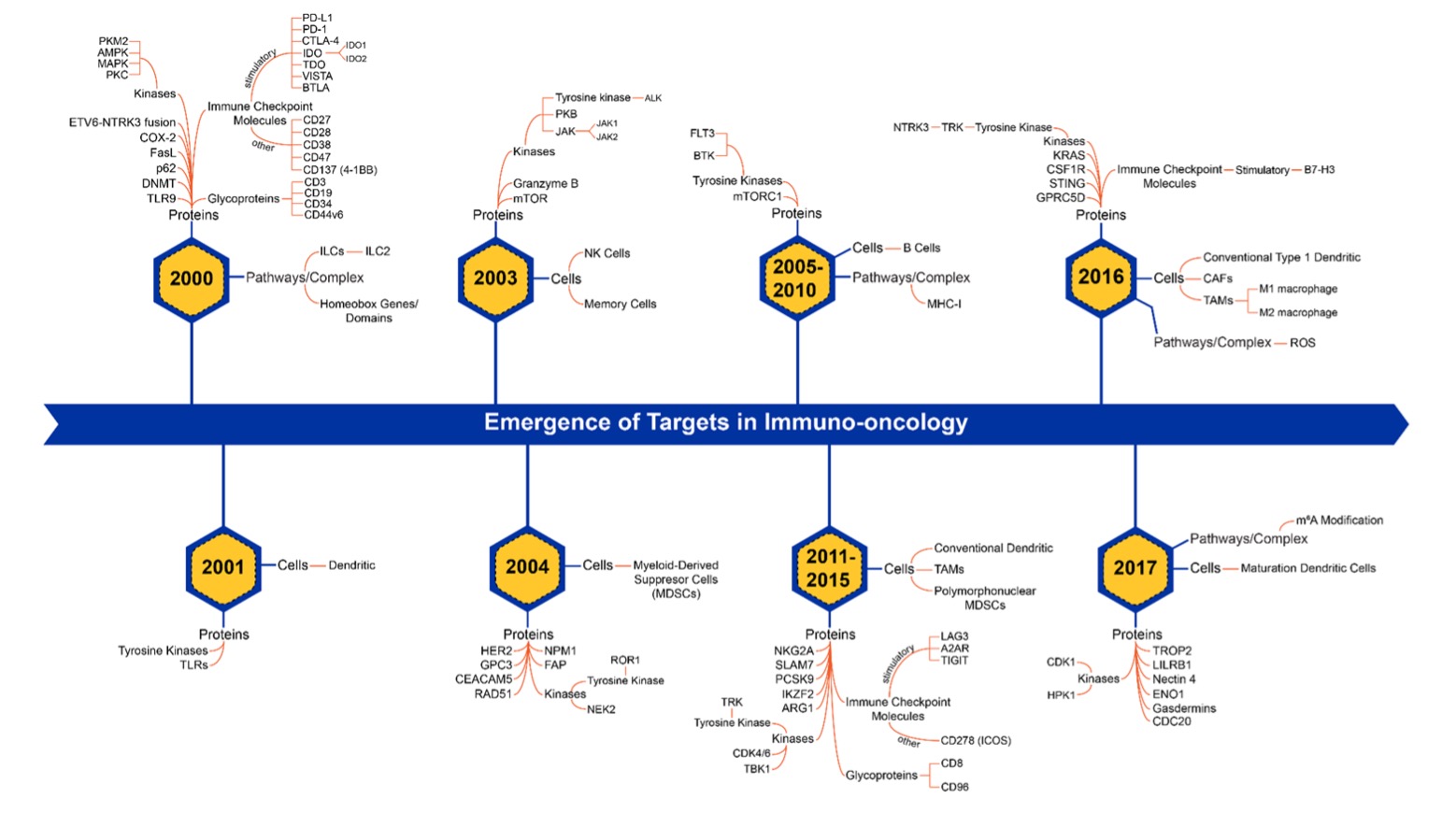
癌症免疫学在过去 20 年中发展迅速,新兴靶点也随时间的推移而发生变化(图 3)。 随着人们深入了解免疫系统在癌症中的作用,除检查点抑制剂外,其他主要的免疫疗法治疗模式也在不断发展,包括嵌合抗原受体 (CAR) T 细胞疗法、抗体药物偶联物 (ADC) 和癌症疫苗等。
CAR-T 细胞疗法是指对患者的 T 细胞进行基因改造,使其能够识别并攻击带有特定表面抗原的癌细胞。 近年来,关于 CAR-T 细胞疗法的出版物迅速增加,反映了研究突破的速度有所加快,目前已有六种经 FDA 批准的 CAR-T 细胞疗法投入使用(表 1)。
| 名称 | 靶抗原 | 批准年份 | 公司 | 目标疾病 | CAS RN 编号 |
| Kymriah (Tisagenlecleucel) | CD19 | 2017 | Novartis | B 细胞急性淋巴细胞白血病 (ALL) 和 B 细胞非霍奇金淋巴瘤 (NHL) | 1823078-37-0 |
| Yescarta (Axicabtagene ciloleucel) | CD19 | 2017 | Kite Pharma/Gilead | B 细胞 NHL 和滤泡性淋巴瘤 | 2086142-87-0 |
| Tecartus (Brexucabtagene autoleucel) | CD19 | 2020 | Kite Pharma/Gilead | B 细胞 ALL 和套细胞淋巴瘤 (MCL) | 2691112-12-4 |
| Breyanzi (Lisocabtagene maraleucel) | CD19 | 2021 | Juno Therapeutics, Bristol-Myers Squibb | B 细胞 NHL | 2099722-39-9 |
| Abecma (Idecabtagene vicleucel) | B 细胞成熟抗原 (BCMA) | 2021 | Celgene Corporation, Bristol-Myers Squibb | 多发性骨髓瘤 | 2306267-75-2 |
| Carvykti (Ciltacabtagene autoleucel) | BCMA | 2022 | Janssen Biotech | 多发性骨髓瘤 | 2641066-71-7 |
表 1. FDA 批准的 CAR-T 细胞疗法。
ADC 现已成为抗癌武器库中的另一股强大力量。 在这种疗法中,精确制导型方法占据中心位置,单克隆抗体与细胞毒性药物相结合,专门向癌细胞输送有效药物。 ADC 的形势与 CAR-T 细胞疗法的飞速发展如出一辙,除了 14 种已获 FDA 批准使用的 ADC 外,目前还有 150 多种独特的候选药物正在进行临床试验。
癌症疫苗的工作原理是让免疫系统攻击“外来”癌细胞。 我们的趋势格局分析重点介绍了 ADC 和 CAR-T 细胞疗法的持续增长,并将癌症疫苗确定为一种新兴趋势,其出版物近年来迅速增长。 这证明了该创新方法的发展势头,有望在全球范围内彻底改变人们使用免疫疗法抗癌的方式。
癌症免疫疗法结合纳米医学: 范式的转变
新兴癌症免疫疗法的有效性取决于其精确到达肿瘤部位的能力。 这种精确性通过药物或细胞递送系统来实现,而药物或细胞递送系统也是最大限度地提高治疗效果和尽量减少脱靶效应的关键因素。 此外,药物递送系统还能促进多种治疗药物的同时输送。 如果与化疗、放疗或其他 IO 疗法等其他癌症治疗方法结合使用,便可以为产生协同效应打开大门。
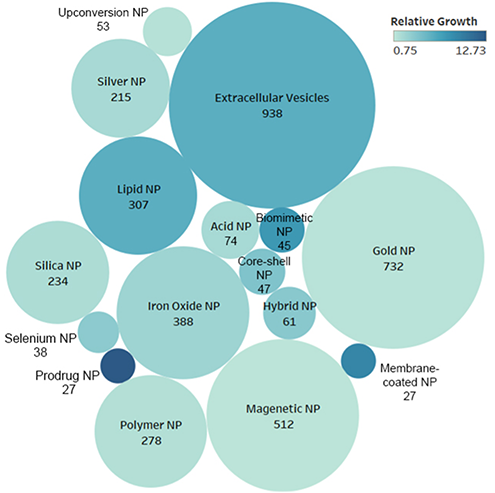
近年来,材料科学和纳米技术的进步催生了各种纳米材料。 虽然脂质纳米颗粒一直是免疫疗法给药的主力军,但我们的趋势格局分析表明其具有广阔的发展前景。 前体药物递送系统、仿生设计和细胞膜包覆纳米颗粒正日益成为值得关注的纳米技术(图 4)。
癌症免疫疗法的未来: 揭开充满希望的前景
在不断发展的免疫肿瘤学领域,征程远未结束,每一步都蓄势待发。 每一项新进展都促使人们不断发现新兴靶点和生物标志物,它们是前景广阔的 IO 疗法创新的关键所在。 这些发现不仅令人振奋,也证明了癌症免疫疗法的巨大潜力。
如需了解有关不断发展的免疫肿瘤学领域的更多信息,请参阅我们的同行评审出版物。



