Mis à jour : 22 décembre 2020
De récentes informations prometteuses au sujet de l'efficacité et de l'innocuité des vaccins contre la COVID-19 laissent entrevoir la lumière au bout du tunnel de la pandémie qui a interrompu la vie normale dans le monde entier tout au long de l'année 2020. Deux vaccins à ARN messager, l'un produit par Pfizer/BioNTech et l'autre par Moderna, viennent de recevoir une autorisation d'utilisation d'urgence (EUA) aux États-Unis et ont également été autorisés au Royaume-Uni et au Canada. De nombreux autres candidats vaccins les suivent de près.Toutefois, alors que de multiples vaccins devraient être mis à la disposition du public au cours des prochains mois, pour de nombreuses personnes, cet espoir s'accompagne d'une multitude de questions. Je vais tenter ici de répondre aux questions scientifiques les plus courantes au sujet des candidats vaccins actuels contre la COVID-19 et de vous indiquer des ressources importantes pour obtenir plus d'informations. J'encourage chacun à partager des sources d'informations précises et validées scientifiquement comme celles-ci avec d'autres afin que nous puissions tous prendre des décisions bien informées au sujet de la vaccination.
Quels sont les types de vaccins majeurs en cours de développement contre la COVID-19 ?
Plus de 200 vaccins contre la COVID-19 en cours de développement à travers le monde sont basés sur de multiples approches différentes. Tous les vaccins fonctionnent en administrant au corps humain un pathogène plus faible ou ne provoquant pas la maladie (ou antigène) similaire en termes de structure au pathogène qui provoque la maladie, de sorte que le système immunitaire humain puisse apprendre à reconnaître ce pathogène spécifique et à réagir efficacement lorsqu'il se trouve confronté au véritable pathogène. Toutefois, les plateformes vaccinales varient en ce qui concerne les antigènes utilisés et la manière dont ils introduisent cet antigène pour déclencher la réponse immunitaire de notre organisme.
Les vaccins à ARNm sont relativement récents dans le domaine de la recherche de vaccins. Toutefois, cette technologie a déjà présenté de grandes promesses dans les vaccins contre le virus Zika et le cytomégalovirus. Les candidats vaccins Pfizer/BioNTech (BNT162b2) et Moderna (mRNA-1273), qui devraient être les premiers largement disponibles, utilisent tous deux cette approche et plus de 20 autres candidats vaccins à ARN messager en sont actuellement à différents stades de développement.
Au lieu d'administrer directement un antigène déclenchant le système immunitaire dans le corps humain, les vaccins ARNm administrent un élément d'ARNm contenant le code génétique que nos cellules peuvent utiliser pour fabriquer l'antigène. L'ARNm est une biomolécule fragile qui se dégrade facilement à haute température ou sous l'effet des enzymes de l'organisme humain. Ces vaccins doivent donc être stockés à très basse température. L'ARNm présent dans ces formulations de vaccins est également enfermé dans des nanoparticules lipidiques qui préservent leur stabilité et facilitent son administration dans les cellules humaines.
Malgré une expérience limitée des vaccins à ARNm, ceux-ci sont généralement considérés comme plus sûrs que les vaccins traditionnels qui utilisent du matériel viral, car ils minimisent le risque d'introduire des pathogènes ou de provoquer des mutations génomiques. La fabrication de vaccins à ARNm est également plus rapide, moins coûteuse et plus évolutive que celle des autres types de vaccin, ce qui est particulièrement important compte tenu de l'urgence de la situation actuelle face à la COVID-19.
Pour des informations plus détaillées au sujet des vaccins à ARNm, lisez ce récent article de blog et regardez la vidéo ci-dessous qui présente le fonctionnement de ces vaccins au niveau des cellules.
Les vaccins à vecteur viral non répliquant utilisent un virus qui ne provoque pas la maladie comme vecteur pour transporter les instructions génétiques afin d'exprimer la protéine antigène du virus provoquant la maladie, mais ce virus transporteur a été génétiquement modifié, de sorte qu'il ne peut pas se répliquer dans notre corps. Un bon exemple de cette technologie de vaccination en cours d'utilisation est celui du vaccin contre le virus Ebola, qui a récemment obtenu une licence d'utilisation d'urgence dans l'Union Européenne. Environ 30 candidats vaccins contre la COVID-19 basés sur cette plateforme de vaccination sont en cours de développement, dont les candidats les plus à la pointe sont ceux d'AstraZeneca/Oxford (AZD1222) et de Janssen (Ad26COVS1). Cette approche de vaccination présente plusieurs avantages, notamment une capacité de production en gros volumes, un coût faible et des exigences moins strictes en termes de température de stockage et de transport.
Les vaccins à sous-unités protéiques diffèrent des vaccins à ARNm et des vaccins à vecteur viral non répliquant, car ils introduisent des protéines antigènes qui déclenchent une réponse immunitaire directement dans l'organisme, au lieu d'introduire des informations génétiques que nos cellules utilisent ensuite pour fabriquer ces antigènes in vivo. Le vaccin FluBlok contre la grippe est un exemple de vaccin actuellement licencié qui utilise cette approche. Environ 70 candidats vaccins contre la COVID-19 en cours de développement utilisent la technologie des sous-unités protéiques, dont plus de 10 sont en phase d'essai clinique.
Les vaccins à virus inactivé sont produits en développant le virus pathogène par culture cellulaire, laquelle est ensuite inactivée et introduite dans l'organisme. La plupart des vaccins courants contre la grippe utilisent cette approche. Actuellement, environ 20 candidats vaccins contre la COVID-19 en cours de développement utilisent l'approche du vaccin à virus inactivé. Comme le virus entier est introduit dans le corps, cette approche s'applique à un large éventail de protéines antigéniques et reproduit souvent la véritable infection en termes de réponse immunitaire. Toutefois, la capacité de production est limitée, car elle nécessite une installation disposant d'un niveau de biosécurité élevé pour gérer le virus vivant.
Vous trouverez d'autres comparaisons entre les différents types de vaccin et plus d'informations sur leur fonctionnement dans cet article.
Comment a-t-on pu développer si rapidement un vaccin contre la COVID-19 ?
Traditionnellement, il faut souvent 15 ans, voire plus, pour passer du laboratoire à la mise sur le marché, en passant par les phases de conception, de développement, de tests précliniques, d'essais cliniques et de révision réglementaire. Par conséquent, le fait de disposer de plusieurs vaccins hautement efficaces contre la COVID-19 approuvés ou pratiquement approuvés dans un délai de moins d'un an est remarquable. Cette vitesse record ne reflète pas un manque de diligence dans le développement ou les tests. Aucune étape n'a été ignorée et aucune norme réglementaire n'a été assouplie lors du développement de ces vaccins. En fait, le processus de développement a pu être accéléré comme suit : (1) Les chercheurs ont collaboré et partagé l'information à un degré sans précédent, à commencer par les scientifiques chinois qui ont publié la séquence génomique du virus SARS-CoV-2 à destination de la communauté mondiale des chercheurs début janvier. (2) Même si le vaccin à ARNm est considéré comme une nouvelle technologie, l'idée de base est en fait apparue dans les années 1990 et les recherches sur la technologie des vaccins à ARNm qui ont été entreprises depuis 2003 pour l'épidémie de SARS ont été largement exploitées pour la COVID-19. (3) Le développement d'un vaccin contre la COVID-19 a été activement soutenu du point de vue financier et réglementaire par les gouvernements du monde entier, avec des travaux comme l'Opération Warp Speed aux États-Unis, qui ont donné la priorité à ces vaccins pour les faire passer par le processus réglementaire aussi rapidement que possible et planifier à l'avance leur distribution. (4) La nature mondiale de la pandémie et l'intérêt public considérable ont garanti un pool de participants adéquat pour soutenir plusieurs essais cliniques simultanés au dernier stade.
Quels sont les vaccins contre la COVID-19 qui seront prochainement disponibles et quel est le meilleur ?
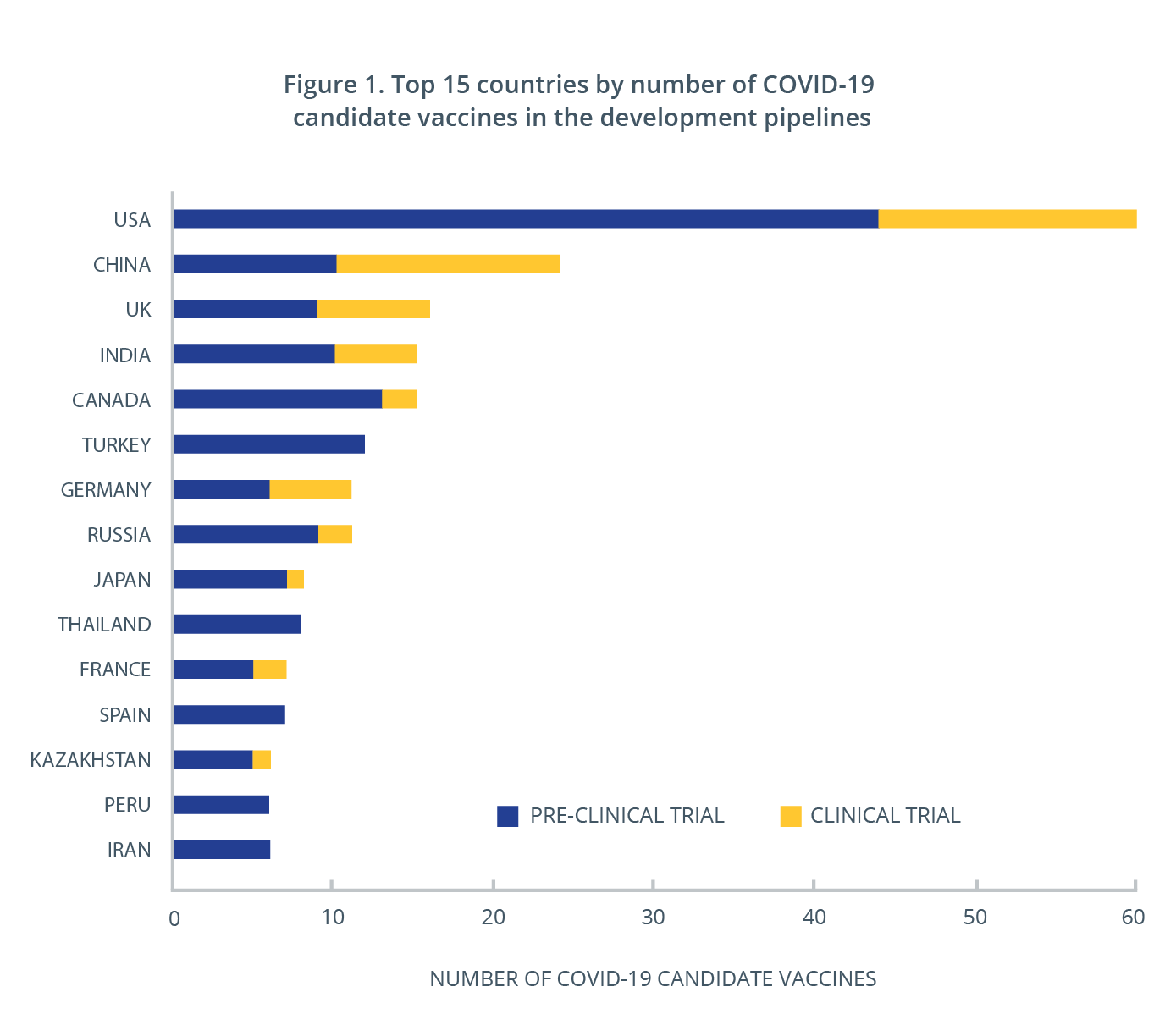
En tout, on dénombre plus de 50 candidats vaccins qui sont actuellement en cours d'étude clinique et près de 170 qui sont en phase d'évaluation préclinique à travers le monde. Plus de 30 pays ont travaillé au développement de vaccins contre la COVID-19 et au moins la moitié d'entre eux disposent d'un, voire de plusieurs vaccins en phase d'essais cliniques (figure 1). Les vaccins qui devraient être disponibles les premiers sont les vaccins à ARN messager de Pfizer/BioNTech et Moderna, dont la distribution a été récemment approuvée aux États-Unis, au Royaume-Uni et au Canada.La Chine et la Russie ont aussi commencé à distribuer des vaccins développés dans ces pays après avoir choisi d'accorder l'autorisation avant l'achèvement des essais cliniques.
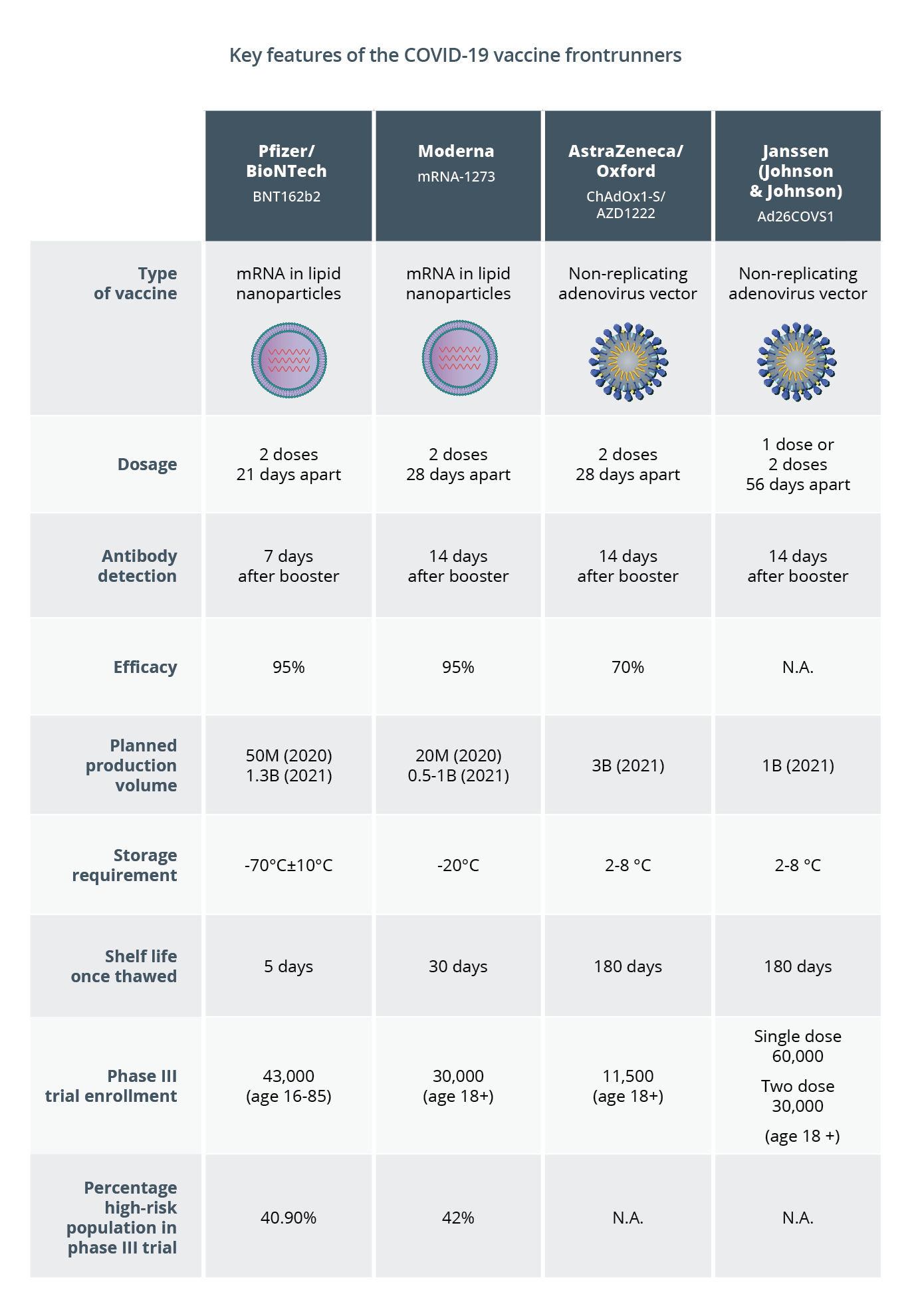
Le tableau ci-dessous présente les principales caractéristiques des quatre principaux vaccins pour lesquels les données d'efficacité préliminaires issues des dernières phases des essais cliniques ont été publiées. Selon les données initiales, les deux vaccins à ARNm présentent une efficacité supérieure à celle du candidat vaccin à vecteur viral non répliquant d'AstraZeneca/Oxford. Toutefois, ce dernier présente certains avantages en termes de coût et d'exigences de stockage. Un autre vaccin à vecteur viral non répliquant à base d'adénovirus développé par Janssen devrait bénéficier d'un très grand nombre d'inscriptions aux essais cliniques et pourrait nécessiter une seule dose, mais ses données d'efficacité ne sont pas encore disponibles.
N'oubliez pas cependant que le premier vaccin mis sur le marché ne constituera pas nécessairement la meilleure solution à long terme pour tout le monde. Outre les candidats majeurs mentionnés ci-dessus, de nombreux autres candidats vaccins prometteurs sont encore en cours d'essai clinique. Certains de ces candidats pourraient offrir des alternatives permettant de surmonter les défis logistiques majeurs liés aux premiers vaccins, dont la nécessité d'injecter plusieurs doses, les exigences extrêmes en termes de température de stockage, la faible durée de conservation et une éventuelle défiance du public envers de nouvelles technologies de vaccination.
Ces candidats supplémentaires en phase avancée, s'ils sont approuvés, seront particulièrement importants pour prendre en charge les programmes de vaccination dans des lieux où les infrastructures sanitaires physiques, cliniques et publiques sont plus limitées. Par exemple, le NVX-CoV2373, développé par Novavax et qui est actuellement en phase III d'essais cliniques, est un vaccin à sous-unités protéiques basé sur la même technologie que le vaccin existant contre l'hépatite B. Ce candidat vaccin semble provoquer des effets secondaires plus légers et déclencher une réponse immunitaire plus forte que les vaccins à ARNm, peut être stocké à des températures de réfrigération normales et pourrait être accepté avec plus de confiance par le public compte tenu de la familiarité avec la technologie utilisée. Autre exemple, le vaccin ARCT-021 d'Arcturus Therapeutics, actuellement en phase II d'étude clinique, est un autre candidat vaccin à ARN messager. Il envoie une charge d'ARN auto-amplificatrice directement dans les cellules, ce qui ne nécessite qu'une injection à une dose nettement moindre. Grâce à la lyophilisation, le vaccin ARCT-021 peut aussi être stocké à des températures de réfrigération normales.
Comment avoir la certitude que les vaccins contre la COVID-19 sont sûrs ?
La vaccination est considérée comme l'un des progrès médicaux les plus importants de la civilisation moderne. Elle nous a libérés d'un grand nombre de maladies infectieuses mortelles qui décimaient les populations dans le passé. Depuis les travaux pionniers du Dr Edward Jenner sur un vaccin contre la variole il y a plus de 200 ans, les vaccins contre de nombreuses maladies infectieuses mortelles comme la rougeole, les oreillons, la rubéole, la polio, les hépatites A et B, le papillomavirus humain (HPV) et la grippe font partie des traitements médicaux de base. Le processus de développement du vaccin contre la COVID-19 n'est pas différent de celui qui est utilisé pour l'élaboration de ces autres vaccins largement acceptés par le public, si ce n'est qu'il a bénéficié d'une recherche accélérée et d'une approbation rapide.
L'ensemble du processus de développement, d'évaluation et de réglementation qu'un vaccin doit subir avant d'être mis à la disposition du grand public a été soigneusement conçu dans une optique privilégiant la sécurité. Les essais cliniques des vaccins sont des entreprises de grande envergure qui font appel à un grand nombre de volontaires variés afin d'établir l'innocuité des vaccins et d'éliminer les problèmes de sécurité rares à court et à long terme. De nombreuses données relatives au développement de vaccins antérieurs indiquent que les réactions et les effets secondaires les plus sévères surviennent dans les 6 semaines suivant la vaccination. C'est la raison pour laquelle la FDA insiste pour disposer d'au moins deux mois de données de sécurité provenant d'un essai clinique en phase III avant même d'envisager d'accorder une autorisation d'utilisation d'urgence, mais les données des participants sont suivies pendant de nombreuses années pour s'assurer qu'aucun problème n'apparaît à long terme.
La taille des populations participant aux essais cliniques pour les principaux vaccins contre la COVID-19 correspondait à celle des essais cliniques antérieurs. Les données des essais cliniques de Pfizer indiquent que sur les 44 000 participants, 170 ont été confirmés comme atteints de la COVID-19 à ce jour. Sur ces cas, 162 étaient issus du groupe placebo, alors que huit seulement provenaient du groupe vacciné. Les données de l'essai clinique de Moderna portant sur 30 000 personnes indiquent que seules cinq personnes du groupe vacciné ont développé la COVID-19, alors que 90 personnes ayant reçu une injection de placebo sont tombées malades. Même si la plupart des participants ont ressenti certains effets secondaires, ces derniers étaient majoritairement légers et comprenaient une fatigue, des maux de tête, une douleur au site d'injection et une douleur musculaire. Chez de nombreux participants, ces effets étaient plus significatifs après la deuxième dose.
Combien de temps le vaccin me protégera-t-il contre la COVID-19 ?
La durée totale d'immunisation des personnes ayant été atteintes de la COVID-19 ou immunisées par vaccination n'est pas encore connue avec précision. Les chercheurs indiquent que les niveaux d'anticorps présents dans le sang des patients atteints de COVID-19 baisse rapidement au cours des semaines suivant leur rétablissement. Toutefois, on sait que les lymphocytes B à mémoire et les lymphocytes T, tous deux capables d'une réponse immunitaire rapide en cas de réinfection possible, durent beaucoup plus longtemps. L'idée selon laquelle ces cellules pourraient offrir une immunité plus durable est étayée par l'observation des patients rétablis de la COVID-19, qui sont très peu susceptibles de contracter à nouveau la maladie pendant au moins six mois. En outre, les scientifiques prévoient aussi que l'immunité induite par le vaccin contre la COVID-19 pourrait être plus forte que l'immunité résultant d'une infection virale naturelle. Cette conviction est étayée par des tests d'anticorps précoces réalisés chez des personnes ayant reçu le vaccin ARNm de Moderna, chez qui la production d'anticorps était plus élevée que celle des patients rétablis de la COVID-19, ainsi que par les données à plus long terme portant sur de nombreux vaccins largement utilisés, notamment ceux contre le papillomavirus humain et le tétanos. En outre, d'après les observations réalisées à ce jour, ce coronavirus ne mute pas aussi vite que le virus de la grippe, de sorte qu'il est très peu probable que les chercheurs aient à concevoir un autre vaccin contre la COVID-19 chaque année.
Il est cependant important de comprendre que la plupart des essais cliniques portant sur les vaccins contre la COVID-19 sont conçus pour prouver que chaque vaccin est sûr et établir son niveau d'efficacité dans la prévention de la maladie. Ils n'établissent pas nécessairement que les vaccins préviennent complètement l'infection. En conséquence, jusqu'à la réalisation d'autres tests l'année prochaine, on ignore encore si ces vaccins empêchent les personnes de propager le virus, même si elles ne tombent pas malades. C'est pourquoi le port du masque et la distanciation sociale pourraient rester recommandés jusqu'à ce qu'une grande partie de la population ait été vaccinée.
Pour des informations plus détaillées sur les vaccins et les thérapeutiques contre la COVID-19, y compris les commentaires des scientifiques, les jeux de données en accès libre et les rapports spéciaux, consultez les ressources CAS sur la COVID-19.