Présentation des colles moléculaires
Les colles moléculaires sont de petites entités chimiques qui utilisent une stratégie révolutionnaire appelée dégradation ciblée des protéines (TPD) par proximité induite dans laquelle des protéines pathogènes d'intérêt (POI) sont liées à des enzymes digestives naturelles et détruites (figure 1). Cette approche a pour résultat de « coller » littéralement les POI aux ubiquitines ligases E3 du système ubiquitine-protéasome, lequel fonctionne normalement comme un système de traitement des déchets cellulaires. Cette approche a créé de nouvelles catégories d'agents thérapeutiques aux modes de fonctionnement complètement nouveaux, produisant une nouvelle activité potentielle intéressante contre plusieurs maladies graves comme le cancer, les maladies inflammatoires et immunitaires et les infections, dont un bon nombre sont provoquées par l'expression aberrante d'une protéine pathogène. Plus de 600 ubiquitines ligases E3 sont encodées dans le génome humain et, jusqu'à présent, seules quelques-unes ont été exploitées à l'aide de l'approche TPD, de sorte qu'il existe un potentiel considérable d'en développer bien d'autres.
Posez des questions aux experts de Dana-Faber, au PDG de Neomorph et à CAS tandis qu'ils explorent les nouvelles tendances dans le domaine des colles moléculaires, de la dégradation ciblée des protéines et de la proximité induite lors d'un webinaire ACS en direct le 5 octobre 2022 à 14 h, heure de l'Est des États-Unis. Inscrivez-vous ici.
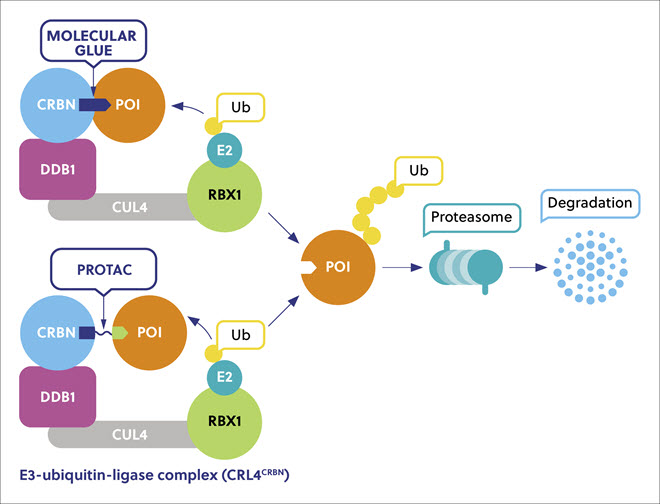
Les dégradeurs de protéines présentent des avantages, car ils agissent par le biais d'une liaison transitoire au lieu d'une occupation compétitive et se dissocient après avoir promu la polyubiquitination de la POI. Un seul dégradeur peut par conséquent détruire de nombreuses copies d'une protéine pathogène, offrant une haute efficacité contre des protéines jusqu'alors « intraitables » à faible dose. Les médicaments inhibiteurs de protéines bloquent le site actif d'une protéine pathogène, alors que les dégradeurs suppriment toutes ses fonctions, offrant une sensibilité supérieure aux POI et une plus grande chance d'affecter les interactions entre protéines non enzymatiques.
Le développement de composés de TPD qui utilisent la dégradation naturelle des protéines induite par l'ubiquitine à des fins thérapeutiques a considérablement progressé au cours des deux dernières décennies. Le premier brevet d'un dégradeur chimérique thérapeutique pour lier une POI à la ligase E3 a été déposé par Proteinix en 1999. Ce premier brevet a été suivi d'une étude de validation de concept au cours de laquelle une protéine associée au cancer a été dégradée par une chimère ciblant la protéolyse (PROTAC). Les premières PROTAC étaient de grosses structures moléculaires ; le premier rapport concernant un dégradeur récepteur androgénique (AR) à petite molécule utilisant de la nutline-3 pour se fixer sur le MDM2 a été publié en 2008. La découverte ultérieure de mimétiques à petites molécules de la peptide HIF1α a accéléré la conception rationnelle de PROTAC à petites molécules. Jusqu'à présent, peu de TPD induites par proximité ont atteint le stade des essais cliniques, mais deux PROTAC (ARV-110 et ARV-471 qui ciblent le récepteur des androgènes et des œstrogènes) sont parvenues au stade des essais de phase II, tandis que bien d'autres sont en cours de développement.
Les colles moléculaires et les PROTAC présentent des propriétés différentes. Les colles moléculaires sont de petites molécules qui interagissent avec un certain nombre de protéines cibles qui sont difficiles à prédire, présentant des activités biologiques distinctes en induisant et en renforçant l'interaction de deux protéines qui, par ailleurs, ne présentent pas d'affinité intrinsèque entre elles. Les PROTAC sont des molécules bivalentes composées de deux fractions, l'une se liant à la POI et l'autre à la ligase E3, jointes par un lieur. Les colles moléculaires sont plus petites, et on s'attend à ce qu'elles présentent de meilleures propriétés pharmacologiques, une perméabilité membranaire plus importante, une meilleure absorption cellulaire et une pénétration de la barrière sang-cerveau supérieure à celle des PROTAC. L'identification des colles moléculaires a principalement relevé du hasard, mais des approches de conception rationnelle pour cibler des protéines intraitables apparaissent. Suite à la découverte initiale, le parcours se poursuit vers la définition, l'optimisation et la validation de l'échafaudage (tableau 1).
Tableau 1. Parcours de découverte d'un dégradeur de colles moléculaires et de conception de médicament gérée par la structure.
| Découverte initiale | Définition de l'échafaudage |
| Optimisation | Validation |
On a découvert différents types de colles moléculaires ; la plus connue est sans doute la thalidomide et ses analogues, mais on peut également citer le lénalidomide et le pomalidomide, qui ciblent la ligase E3 céréblon. Les colles moléculaires ont été identifiées avec différents autres mécanismes d'action, notamment la dégradation des protéines médiée par l'autophagie, la stabilisation des sous-complexes de la MEK, l'inhibition de la mutation du KRAS, la stabilisation de la polymérisation de la tubuline α et la dégradation de la protéine 12 de liaison du FK506 (FKBP12).
Le paysage de la recherche sur les colles moléculaires tel qu'identifié dans CAS Collection de contenus™
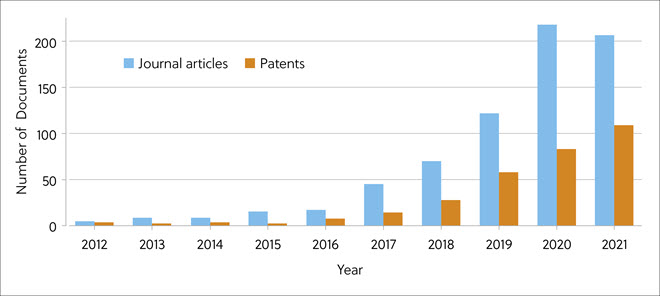
CAS Collection de contenus™ est la plus grande collection de connaissances scientifiques publiées, organisée par des humains et adaptée à l'analyse quantitative des publications scientifiques mondiales par rapport à des variables comme le temps, le domaine de recherche, la formulation, l'application et la composition chimique. Pour évaluer les progrès récents de la recherche sur les colles moléculaires, en particulier dans la chimie médicinale et la découverte de médicaments, un nouveau rapport CAS Insights s'est penché sur les données des publications pertinentes au cours de la période 2012 à 2021 figurant dans CAS Collection de contenus. Durant cette période, on a assisté à une croissance exponentielle des publications d'articles et de brevets concernant les dégradeurs de protéines (figure 2).
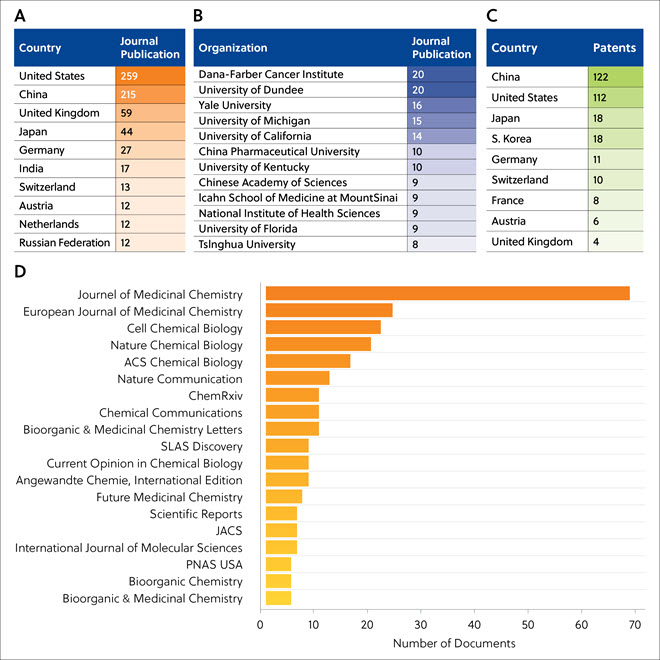
Les publications sur les dégradeurs de protéines provenaient principalement des États-Unis, de Chine, du Royaume-Uni, du Japon, d'Allemagne et d'autres pays (tableau 2A). Le Dana-Farber Cancer Institute et l'université de Dundee ont publié le plus grand nombre d'articles liés aux TPD (tableau 2B). Le plus grand nombre de demandes de brevet liées aux dégradeurs de protéines a été enregistré en Chine et aux États-Unis (tableau 2C). Les revues qui publient fréquemment des articles au sujet des TPD sont présentées dans le tableau 2D, qui met en évidence l'importance des TPD dans la recherche médicale ; le Journal of Medicinal Chemistry et l'European Journal of Medicinal Chemistry sont ceux qui ont enregistré le plus grand nombre d'articles au sujet des TPD.
Tableau 2. Principaux pays (A), entreprises (B) et revues scientifiques (D) ayant publié des articles au sujet des TPD, et principaux pays d'enregistrement de brevets liés aux TPD (C).
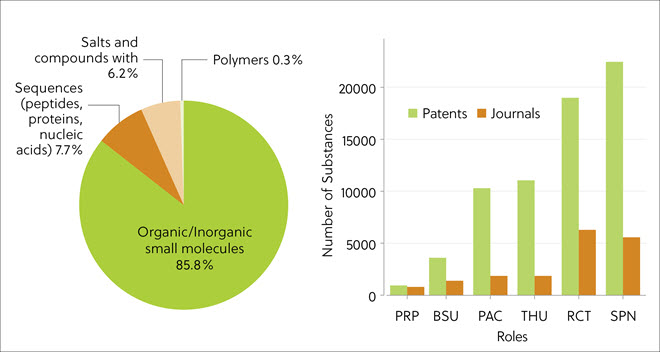
Le type de TPD le plus fréquent dans les publications était les petites molécules (85,8 %), suivies des bioséquences (7,7 %), y compris les peptides, les protéines, les acides nucléiques et les sels (figure 3, panneau de gauche). Cela indique un changement par rapport aux premières molécules chimériques ciblant les protéines, lesquelles étaient basées sur des peptides. Les dégradeurs de protéines sont synthétisées via des réactions chimiques à étapes multiples, ce qui explique la domination des rôles de la SPN (préparation synthétique) et des RCT (réactifs) liés à la synthèse dans les résultats de l'analyse de la littérature (figure 3, panneau de droite). Bien d'autres composés indexés dans CAS Collection de contenus provenaient de brevets.
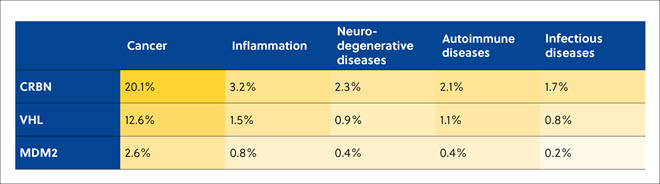
Dans l'analyse de la littérature, les CRBN, VHL et MDM2 se sont avérés les types les plus populaires de ligases E3 utilisées pour se fixer aux TPD, afin d'induire l'ubiquitination et la dégradation protéasomale ultérieure des protéines cibles dans le cancer et les maladies inflammatoires, neurodégénératives, auto-immunes et infectieuses (tableau 3).
Tableau 3. Corrélation du nombre de publications liées aux dégradeurs de protéines dans CAS Collection de contenus pour les trois ligases E3 les plus largement utilisées avec les maladies ciblées. Les pourcentages concernent le nombre total de publications liées aux dégradeurs de protéines.
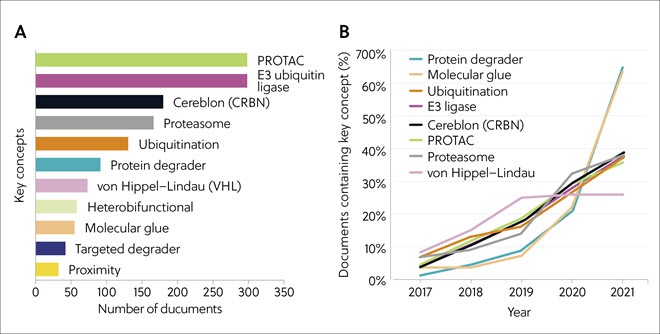
Le plus grand nombre de publications au cours de la période 2017-2021 concernait les PROTAC et les ubiquitines ligases E3, suivies du céréblon, du protéasome et de l'ubiquitination (figure 4A). Les documents portant sur les colles moléculaires et les dégradeurs de protéines étaient moins nombreux, mais ont enregistré une croissance et un intérêt de plus en plus marqués à partir de 2019. D'autres concepts, comme l'ubiquitination, la ligase E3, le céréblon, les PROTAC et le protéasome, ont également affiché une croissance continue tout au long de la période 2017-2021 (figure 4B).
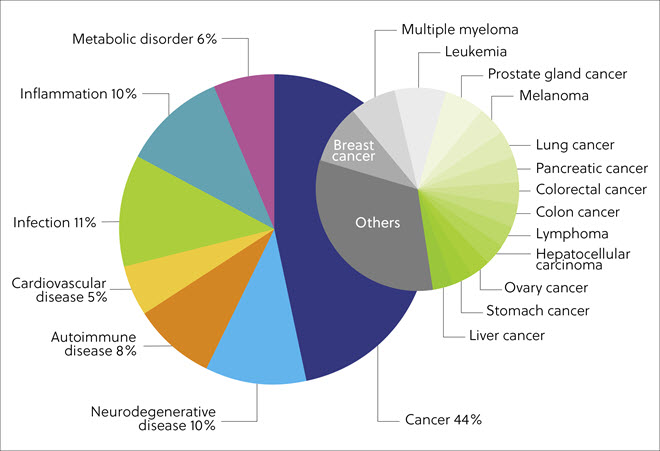
Une analyse des maladies ciblées par les dégradeurs de protéines figurant dans CAS Collection de contenus a révélé que la plus grande partie (44 %) des publications étaient associées à différents cancers (par ex. le cancer du sein et de la prostate, le myélome multiple et la leucémie). En outre, les maladies infectieuses (11 %), neurodégénératives (10 %), inflammatoires (10 %), auto-immunes (8 %), métaboliques (6 %) et cardiovasculaires (5 %) étaient également fortement représentées (figure 5).
Colles moléculaires découvertes et en cours de développement
Le nombre de types et de structures de colles moléculaires connus est déjà considérable et en augmentation constante. Les colles moléculaires les plus étudiées sont les petites molécules qui lient le CRBN de la ligase E3 et les sulfonamides aryles qui engagent le DCAF15. D'autres colles moléculaires qui induisent la dégradation des protéines par différents mécanismes d'action non-ligase E3 comprennent la dégradation des protéines médiée par autophagie, la stabilisation des interactions protéine-protéine, l'inhibition des KRAS mutants, la stabilisation de la polymérisation des microtubules et l'inhibition de la cible de la rapamycine chez les mammifères (mTOR). À cela s'ajoutent des composés naturels comme la cyclosporine A et la sangliféhrine A, qui ont fait la preuve de leur efficacité en tant que colles moléculaires. Ces développements indiquent un élargissement important des approches par colle moléculaire et un champ d'action potentiellement plus divers.
Même si de nombreuses colles moléculaires potentielles ont été identifiées, jusqu'à présent, peu d'entre elles ont été évaluées en termes d'efficacité thérapeutique en clinique et celles qui ont obtenu une approbation réglementaire sont encore moins nombreuses. Différentes entreprises à travers le monde disposent d'une série de colles moléculaires à l'état de développement préclinique pour une utilisation contre différents cancers et diverses maladies neurodégénératives et inflammatoires. Parmi ces entreprises figurent :
- Ranok (Hangzhou, Chine) : candidat médicament RNK05047 entrant en phase d'essai clinique au cours du premier semestre 2022 pour le traitement des tumeurs solides et des lymphomes.
- Monte Rosa Therapeutics (Boston, Massachusetts, États-Unis) : activités d'activation de l'IND pour son programme principal ciblant le GSPT1 pour le traitement oncologique et au-delà. Application de l'IND à soumettre à la FDA à la mi-2022. Phase de découverte pour d'autres colles moléculaires ciblant les tumeurs solides/liquides, les maladies auto-immunes et les maladies du sang.
- Plexum/en partenariat avec Amgen (San Diego, Californie, États-Unis) : phase d'optimisation de pointe pour une colle moléculaire de type céréblon ciblant l'IKZF2 pour le traitement des maladies immunitaires et du cancer.
- Frontier Medicines/en partenariat avec AbbVie (San Francisco, Californie, États-Unis) : phase de découverte de médicament pour développer des médicaments covalents à petites molécules contre des cibles immunologiques et oncologiques intraitables.
- f5 Therapeutics (San Diego, Californie, États-Unis) : candidats moléculaires pour le traitement de nombreux cancers, de la sclérose en plaques, de la polyarthrite rhumatoïde, de la stéatohépatite non alcoolique et de la fibrose du foie.
- Ambagon Therapeutics/en partenariat avec BMS et Merck (San Carlos, Californie, États-Unis) : phase de découverte de médicament avec cinq composés de traitement oncologique en début de découverte.
- Amphista Therapeutics (Londres, Royaume-Uni) : traitements de cancers avec mode d'action non ligase E3.
- Proxygen/en partenariat avec Boehringer Ingelheim (Vienne, Autriche) : phase de découverte de médicament pour le traitement des cancers bronchiques et gastro-intestinaux.
- Neomorph/en partenariat avec le Dana Farber Cancer Institute (San Diego, Californie, États-Unis) : phase de découverte de médicament pour faire progresser le pipeline du développement de sa colle moléculaire contre des cibles intraitables.
- Seed Therapeutics/en partenariat avec Lilly (New York, État de New York, États-Unis) : phase de découverte de médicament avec des candidats au pipeline de colles moléculaires pour le traitement des cancers et des maladies neurodégénératives et infectieuses. Leur composé majeur cible l'oncogène KRAS.
- Pin Therapeutics (Séoul, Corée du Sud) : phase de découverte de médicament.
- Venquis Therapeutics (San Diego, Californie, États-Unis) : phase de découverte de médicament contre le cancer et les maladies dégénératives.
- IRB Barcelona/en partenariat avec Almirall (Barcelone, Espagne) : phase de découverte de médicament pour le traitement des maladies cutanées.
- Shanghai Dage Biomedical Technology Co., Ltd. (Shanghai, Chine) : pipeline de colles moléculaires traitant des cibles contre les cancers et les maladies inflammatoires et métaboliques. Phase d'optimisation de pointe pour les candidates colles moléculaires d'oncologie.
- Triana Biomedicines (Waltham, Massachusetts, États-Unis) : lancé récemment en avril 2022 pour établir un pipeline de colles moléculaires conçues rationnellement en vue de traiter des maladies gérées de manière inadéquate.
- Evotec/en partenariat avec BMS (Hambourg, Allemagne) : phase de découverte de médicament pour développer un pipeline de dégradeurs de colles moléculaires
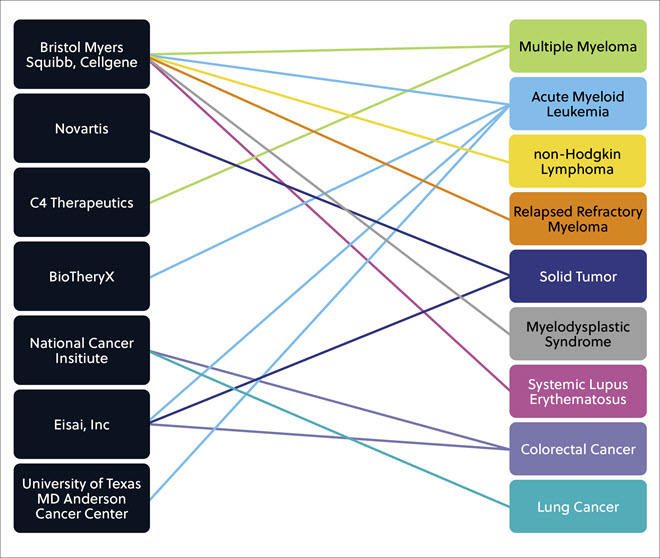
Plusieurs autres entreprises/institutions disposent d'une gamme prometteuse de composés de colles moléculaires à différents stades de développement clinique, qui visent à traiter de nombreuses tumeurs solides et liquides différentes, ainsi que des affections inflammatoires et des maladies auto-immunes comme le lupus érythémateux systémique (figure 6).
Perspectives des colles moléculaires en tant qu'agents thérapeutiques - peuvent-elles répondre à des besoins médicaux non pris en charge ?
L'induction de la proximité de protéines cibles avec les enzymes dégénératives qui n'entreraient pas normalement en contact proche au moyen de colles moléculaires est une approche fascinante qui possède le potentiel de créer de grands nombres d'agents thérapeutiques très nouveaux contre une grande diversité de maladies graves. Le défi consiste maintenant à développer l'approche TPD en identifiant des composés candidats avec une activité utile et en les faisant progresser jusqu'au stade de produits cliniquement utiles.
Le mécanisme d'action des colles moléculaires et leurs principes de conception sont insuffisamment compris et des recherches supplémentaires sont nécessaires pour créer de nouveaux composés et les exploiter pleinement. Les méthodes de découverte de nouvelles colles moléculaires se sont largement appuyées sur le criblage à haut débit, suivi d'une validation systématique. Il existe un besoin de stratégies de conception efficaces et rationnelles pour améliorer le développement de composés nouveaux et plus efficaces et pour évaluer leur activité dans différentes indications. Des outils informatiques permettant de modéliser et de prédire la liaison des colles moléculaires et les progrès de la cristallisation pour améliorer la compréhension de l'arrimage des protéines sont nécessaires pour passer du stade de la découverte par hasard à celui de la conception rationnelle.
Les recherches dans CAS Collection de contenus révèlent que l'induction de la dégradation des protéines au moyen de colles moléculaires suscitent un grand intérêt et connaissent une croissance fulgurante à la fois en termes d'articles de recherche et de brevets. Même si les composés ciblant la ligase E3 restent dominants, il existe aussi un fort intérêt pour les composés non-ligase E3 et certains dégradeurs naturels de colles moléculaires, ce qui indique une grande diversité d'agents potentiels. Les perspectives pour les colles moléculaires semblent donc prometteuses avec l'apparition probable de nombreux autres agents thérapeutiques utilisant cette approche dans un avenir immédiat, qui possèdent le potentiel fascinant d'être en mesure de répondre à un large éventail de besoins médicaux non traités.
Téléchargez notre rapport d'informations pour découvrir la croissance fulgurante des dégradeurs de colles moléculaires, leurs applications thérapeutiques et la manière dont l'intérêt pour la recherche a évolué au cours des dix dernières années.