Gain new perspectives for faster progress directly to your inbox.
Dans le paysage en évolution constante des traitements contre le cancer, les conjugués anticorps-médicaments (CAM) sont apparus comme une catégorie de traitements prometteuse. Les CAM combinent la puissance des médicaments cytotoxiques et la sélectivité des anticorps monoclonaux, offrant une nouvelle approche de la thérapie ciblée. Les conjugués anticorps-médicaments ont démontré des promesses considérables dans la lutte contre le cancer et pourraient révolutionner le traitement ciblé de toute une série d'indications non oncologiques.
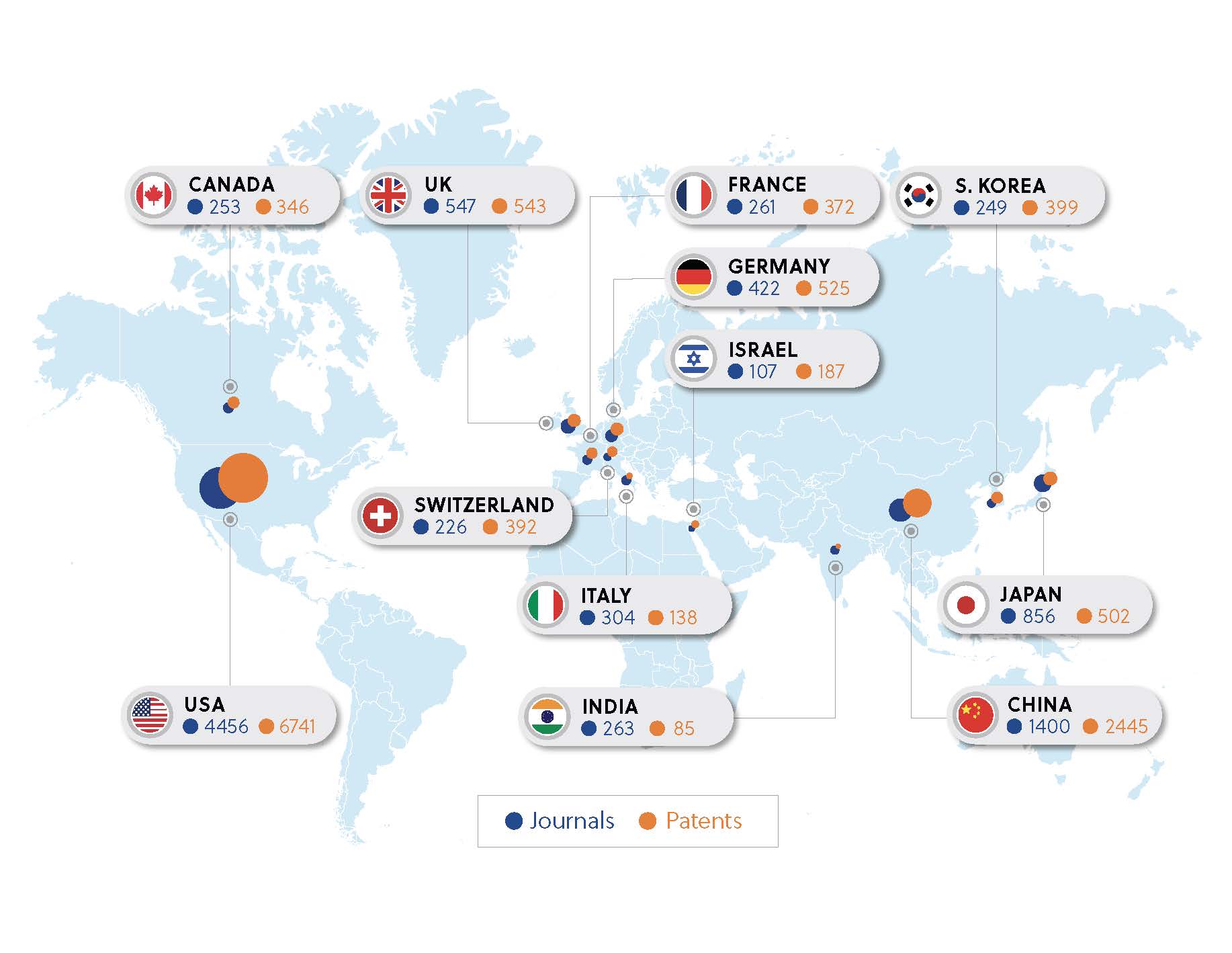
Une analyse des données de CAS Collection de contenus™ liées à la recherche et au développement sur les conjugués anticorps-médicaments démontre une forte croissance avec une augmentation de 30 % du nombre des publications (principalement des articles de revues et des brevets) au cours des trois dernières années. Les États-Unis, la Chine et le Japon sont en tête en termes de nombre de publications d'articles de revues et de brevets (figure 1). Il est intéressant de noter que les brevets sont désormais plus nombreux que les publications dans les revues, ce qui indique que les connaissances scientifiques accumulées se sont transformées en applications brevetables. L'éventail des brevets pour des conjugués anticorps-médicaments dans CAS Collection de contenus ne cesse de se diversifier, les chercheurs explorant de nouvelles technologies de liens, des techniques de conjugaison et des fragments d'antigènes cibles.
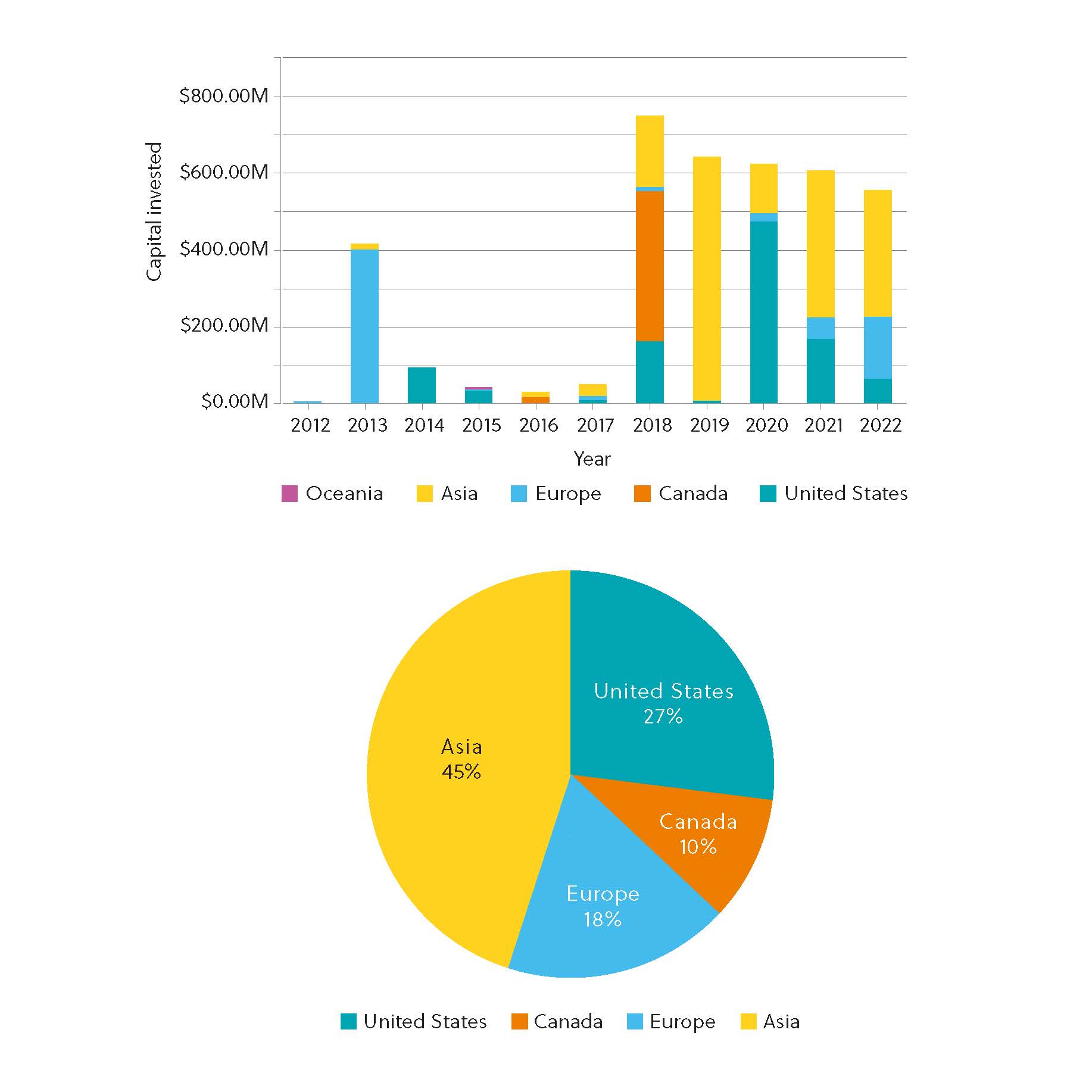
Avec une pléthore de conjugués anticorps-médicaments en cours de développement préclinique et clinique, ces remarquables composés ont attiré l'attention des chercheurs et des laboratoires pharmaceutiques. Selon PitchBook, on assiste à une augmentation spectaculaire de l'investissement privé depuis 2018 (figure 2), ce qui témoigne d'un intérêt significatif pour les conjugués anticorps-médicaments en raison de leur potentiel thérapeutique et commercial. Le marché mondial des conjugués anticorps-médicaments était estimé à 8,6 milliards de dollars en 2022 et pourrait atteindre 23,9 milliards de dollars d'ici à 2032, soit un TCAC de 10,7 % au cours de cette période. Les conjugués anticorps-médicaments attirent l'attention de tous les marchés mondiaux et World ADC Asia a organisé des conférences dédiées pour rassembler les responsables de ce secteur.
À l'intérieur du cheval de Troie : comprendre les conjugués anticorps-médicaments
Pour saisir l'importance des conjugués anticorps-médicaments, il est nécessaire de comprendre comment ils fonctionnent. Ce traitement dynamique comprend trois composants principaux : un anticorps monoclonal, une charge de médicament cytotoxique et une molécule de liaison (figure 3). L'anticorps monoclonal est conçu pour identifier spécifiquement les antigènes surexprimés à la surface des cellules cancéreuses, ce qui permet un ciblage sélectif. La charge cytotoxique est souvent un puissant médicament de chimiothérapie hautement efficace pour tuer les cellules cancéreuses. Enfin, l'agent de liaison sert de passerelle entre les deux autres composants, préservant la stabilité au cours de la circulation tout en libérant la charge au moment de l'internalisation.
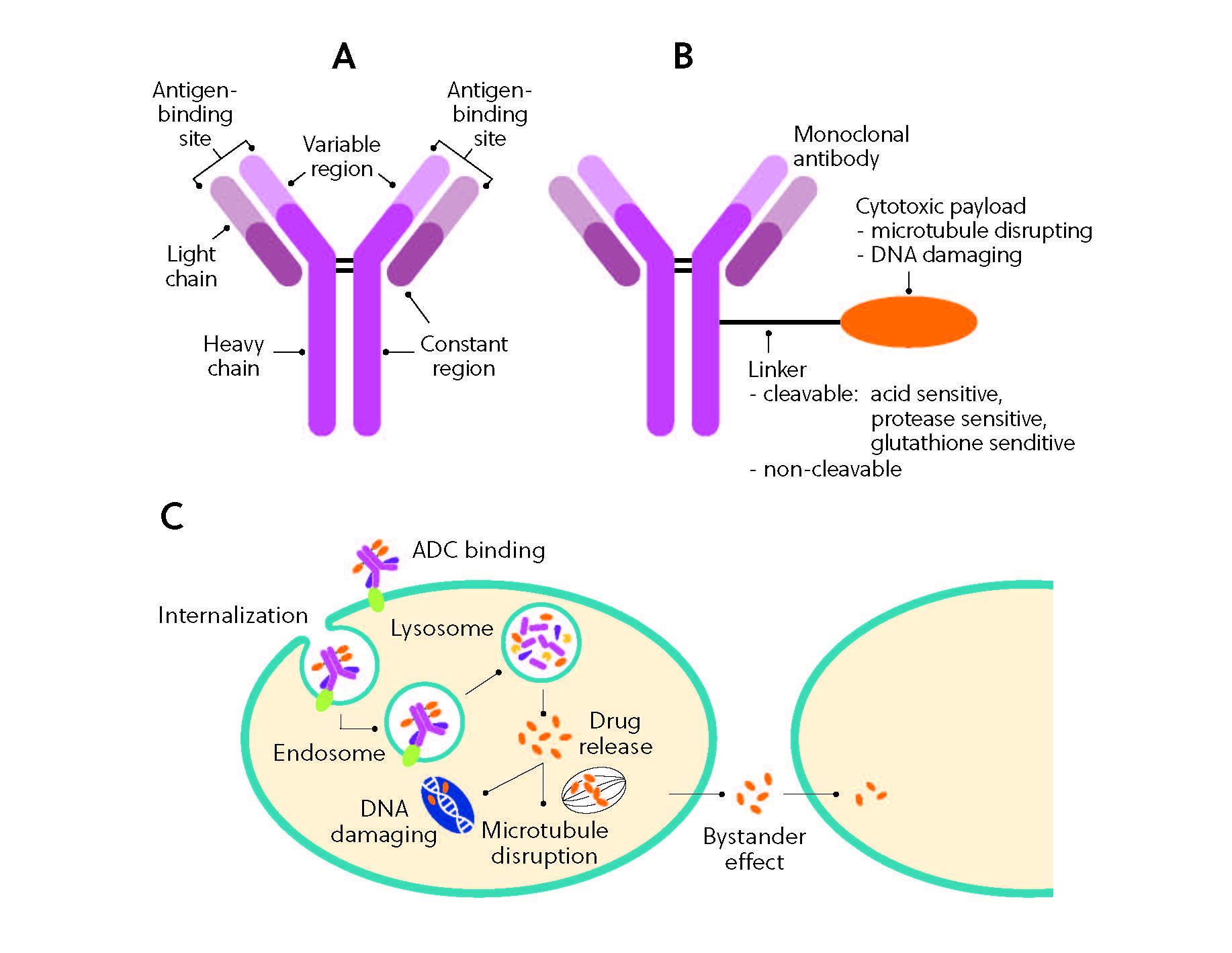
À l'instar des immunothérapies comme les inhibiteurs des points de contrôle immunitaires, les conjugués anticorps-médicaments promettent de révolutionner les traitements contre le cancer. Toutefois, ces deux catégories de composés fonctionnent à l'aide de mécanismes distincts. Alors que les immunothérapies renforcent la réponse immunitaire du patient contre les cellules cancéreuses, le conjugué anticorps-médicament fonctionne comme un « cheval de Troie », portant une frappe létale directement contre les cellules cancéreuses.
Récits de succès dans le traitement par conjugués anticorps-médicaments
Il a fallu plus d'un siècle pour produire les conjugués anticorps-médicaments qui sont en cours de développement clinique. Depuis que le scientifique allemand Paul Ehrlich a proposé le concept de « balle magique » au début du XXe siècle, les chercheurs se sont efforcés de mettre au point des traitements capables de cibler les pathogènes ou les cellules malades de manière sélective sans nuire au reste de l'organisme. Depuis lors, des découvertes majeures de la recherche et du développement de conjugués anticorps-médicaments ont abouti à l'approbation de médicaments révolutionnaires telles que l'agent anti-lymphome Adcetris® (brentuximab vedotin) de Takeda et le Kadcyla® (trastuzumab emtansine) de Genentech, approuvé pour le traitement du cancer du sein à récepteur 2 du facteur de croissance épidermique humain en 2013. Depuis 2020, huit autres conjugués anticorps-médicaments ont été approuvés pour le traitement d'un certain nombre de tumeurs solides et d'hémopathies malignes. Il existe actuellement dans le monde 15 conjugués anticorps-médicaments qui ont reçu une approbation réglementaire (figure 4).

Grâce aux conjugués anticorps-médicaments, la fameuse balle magique autrefois inaccessible est désormais à notre portée. La nature ciblée de ces composés permet l'administration sélective d'une charge cytotoxique dans les cellules malades et minimise l'exposition des cellules saines au médicament. Cette approche ciblée renforce l'efficacité du traitement, mais réduit également le risque d'effets hors cible et de toxicité systémique. En épargnant les cellules saines, les conjugués anticorps-médicaments ouvrent la voie à des schémas thérapeutiques plus tolérables avec une réduction des effets secondaires.
Défis et limites des conjugués anticorps-médicaments
Même si le potentiel des conjugués anticorps-médicaments est indéniable, plusieurs défis et limites doivent être surmontés au cours de leur développement. Tout d'abord, la fabrication de conjugués anticorps-médicaments comprend de nombreuses étapes, dont la production d'anticorps, la synthèse des médicaments et la conjugaison des deux. Cette complexité peut entraîner des coûts de fabrication élevés, rendant ces thérapies moins accessibles aux patients dans certaines régions ou certains systèmes de santé.
La sélection d'antigènes adéquats est un autre obstacle, car le ciblage efficace dépend de la spécificité de l'antigène pour les cellules cancéreuses. Cette sélectivité est essentielle pour garantir la précision du traitement et minimiser les effets hors cible. Toutefois, tous les cancers n'ont pas d'antigènes cibles bien définis et l'hétérogénéité de l'expression des antigènes dans les tumeurs peut encore compliquer la sélection de la cible.
En outre, le choix de la charge cytotoxique est essentiel à la réussite d'un conjugué anticorps-médicament. Le médicament cytotoxique doit posséder une forte létalité contre les cellules cancéreuses tout en préservant sa stabilité pendant la conjugaison et la circulation. Parvenir à cet équilibre entre puissance, stabilité et cinétique de libération représente un défi majeur dans le développement de conjugués anticorps-médicaments.
Les chercheurs sont confrontés à un autre défi : le développement d'une résistance du médicament aux conjugués anticorps-médicaments. Les cellules cancéreuses peuvent développer différents mécanismes pour échapper aux effets des conjugués anticorps-médicaments, comme la dérégulation de l'antigène cible ou l'augmentation de l'efflux du médicament. Ces mécanismes de résistance peuvent limiter l'efficience de ces traitements et réduire leur efficacité au fil du temps.
L'avenir prometteur des conjugués anticorps-médicaments en oncologie et au-delà
L'avenir des conjugués anticorps-médicaments est brillant et plusieurs progrès fascinants se profilent à l'horizon. Les chercheurs explorent des stratégies innovantes pour optimiser la conception de conjugués anticorps-médicaments, notamment l'utilisation de médicaments cytotoxiques alternatifs ou de nouveaux liens et l'amélioration des techniques d'ingénierie des anticorps.
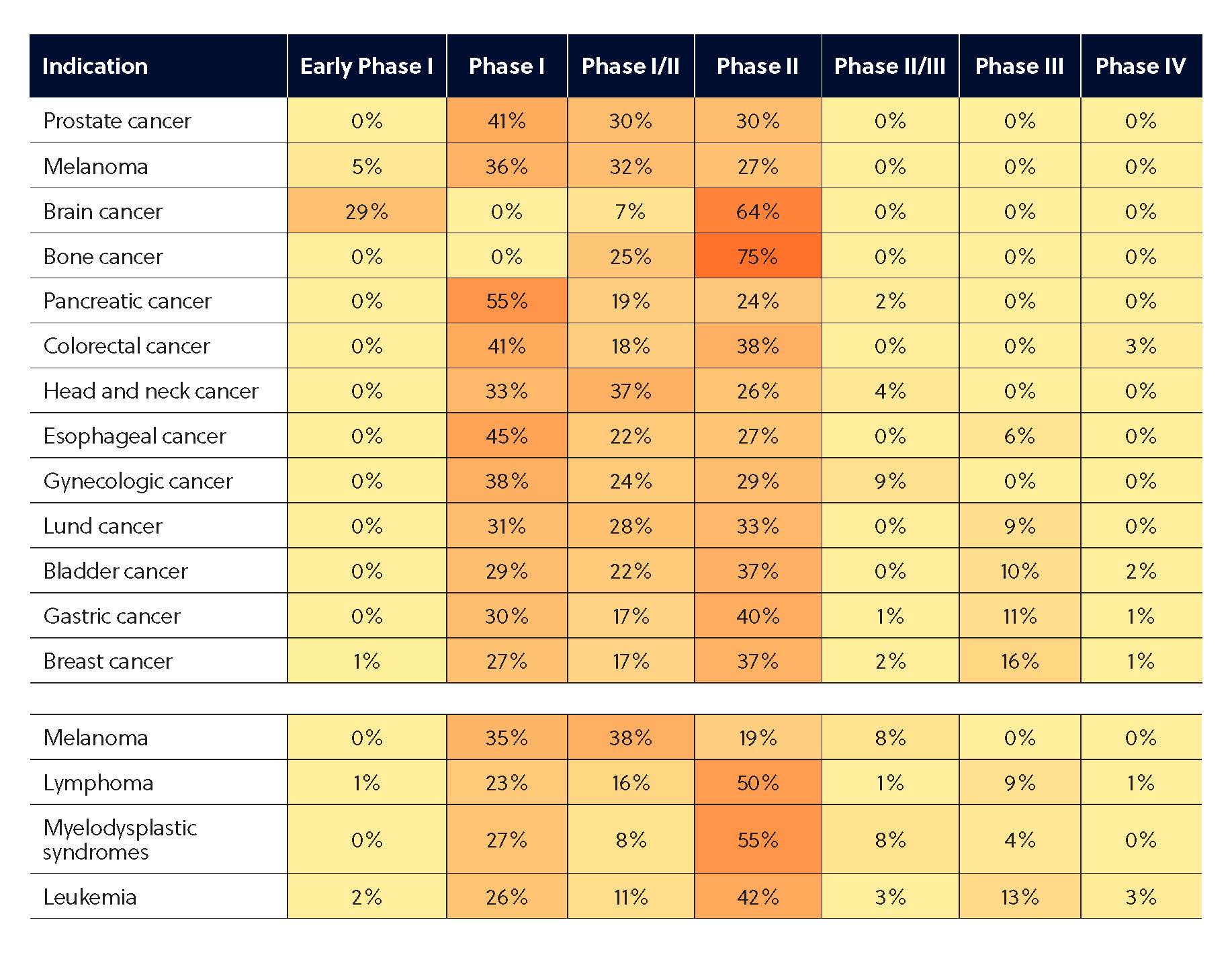
Les traitements combinés intégrant des conjugués anticorps-médicaments et des immunothérapies ou d'autres agents ciblés pourraient présenter des effets de synergie susceptibles d'amplifier leur impact clinique. Les chercheurs pensent que le CAM brentuximab vedotin et la chimiothérapie gemcitabine - une combinaison à l'étude contre différents types de cancer - fonctionnent bien ensemble, car ils ciblent chacun différents types de cellules cancéreuses, administrant une frappe à deux niveaux contre les maladies comme le lymphome de Hodgkin. Les conjugués anticorps-médicaments ont également montré des promesses lorsqu'ils sont combinés avec des inhibiteurs de points de contrôle comme les inhibiteurs PD-1, le pembrolizumab et le nivolumab, ces combinaisons étant actuellement à différents stades d'essais cliniques. De telles combinaisons constituent une option de traitement attrayante pour les patients fragiles ou âgés qui présentent un risque plus élevé de toxicité sévère liée à la chimiothérapie. Même si la plupart des essais d'oncologie en sont à un stade précoce de développement (figure 5), l'extraordinaire diversité de candidats médicaments et de types de cancer étudiés met en évidence le potentiel considérable des conjugués anticorps-médicaments.
Au-delà de l'oncologie, l'expansion des conjugués anticorps-médicament dans de nouveaux domaines thérapeutiques se profile à l'horizon. Cette technologie est actuellement à l'étude dans la lutte contre les maladies infectieuses. La résistance aux antibiotiques a compromis l'efficacité du traitement des infections bactériennes et entraîné le développement de conjugués anticorps-antibiotiques (CAA) pour résoudre ce problème. À l'instar des conjugués anticorps-médicaments, les CAA utilisent des anticorps pour administrer des antibiotiques à des bactéries ciblées, combinant la spécificité des anticorps et la puissance des antibiotiques par le biais d'un lien spécialisé. Même si la recherche sur les CAA est limitée, ces nouveaux composés fascinants pourraient traiter efficacement les biofilms bactériens, ce qui constitue un défi mondial majeur en matière de santé.
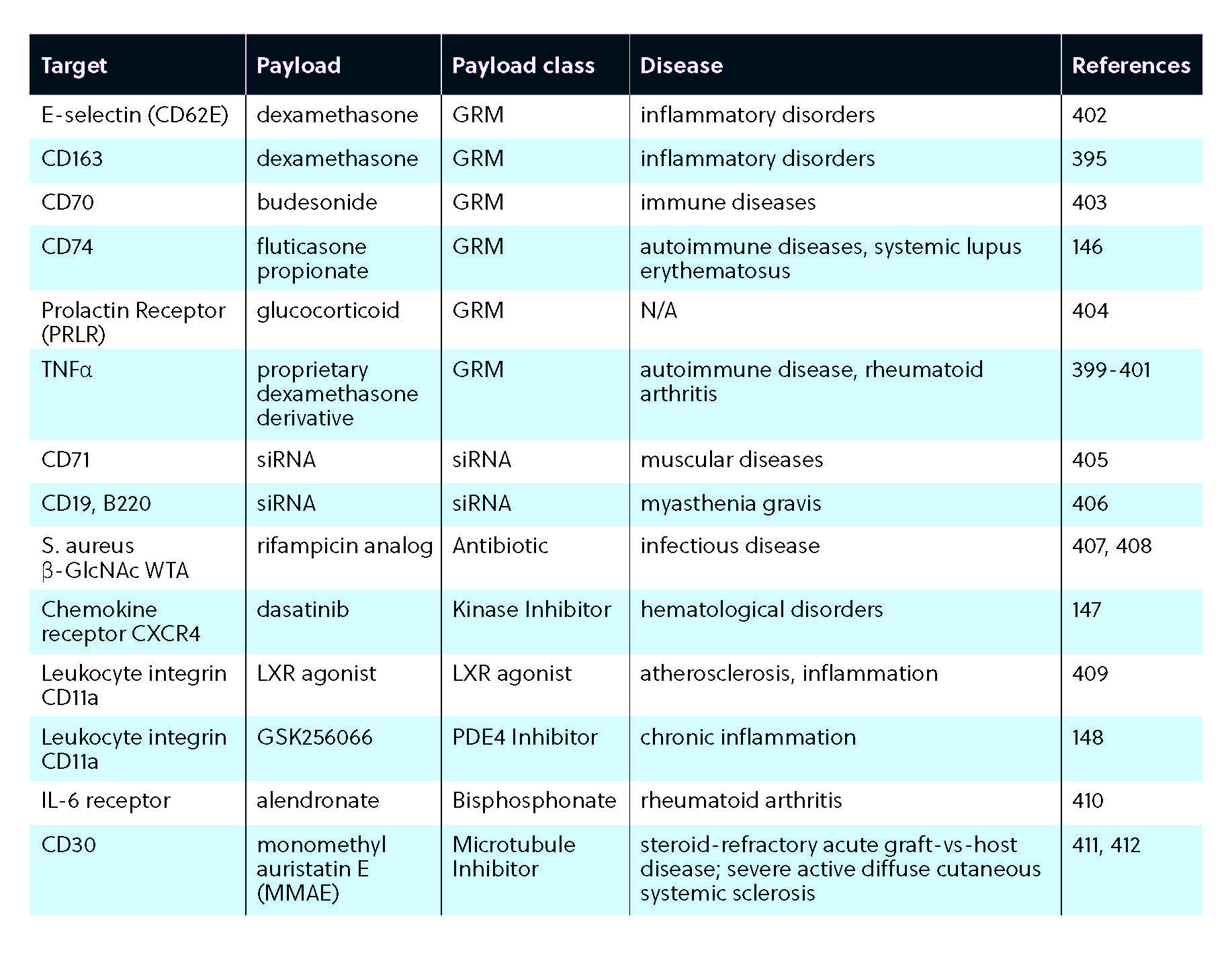
Les conjugués anticorps-médicaments sont également à l'étude en tant qu'agents immunomodulateurs, permettant l'administration ciblée de médicaments anti-inflammatoires comme les glucocorticoïdes tout en minimisant les effets indésirables systémiques habituellement associés à ces agents. Plusieurs stratégies de conjugués anticorps-médicaments sont à l'essai contre un certain nombre d'affections, de la polyarthrite rhumatoïde à la myasthénie grave (tableau 1).
Alors que l'évolution de la technologie des conjugués anticorps-médicaments se poursuit, ces composés constituent une modalité thérapeutique prometteuse offrant un vaste potentiel au-delà de l'oncologie. Même si leur développement se heurte fréquemment à des défis et des limites, le succès des médicaments déjà approuvés et le pipeline croissant de CAM à l'étude témoigne de leur potentiel de transformation pour répondre aux besoins cliniques et améliorer les résultats des patients.
Pour en savoir plus sur le paysage fascinant et en évolution constante des conjugués anticorps-médicaments, consultez notre publication révisée par des pairs dans Bioconjugate Chemistry.



