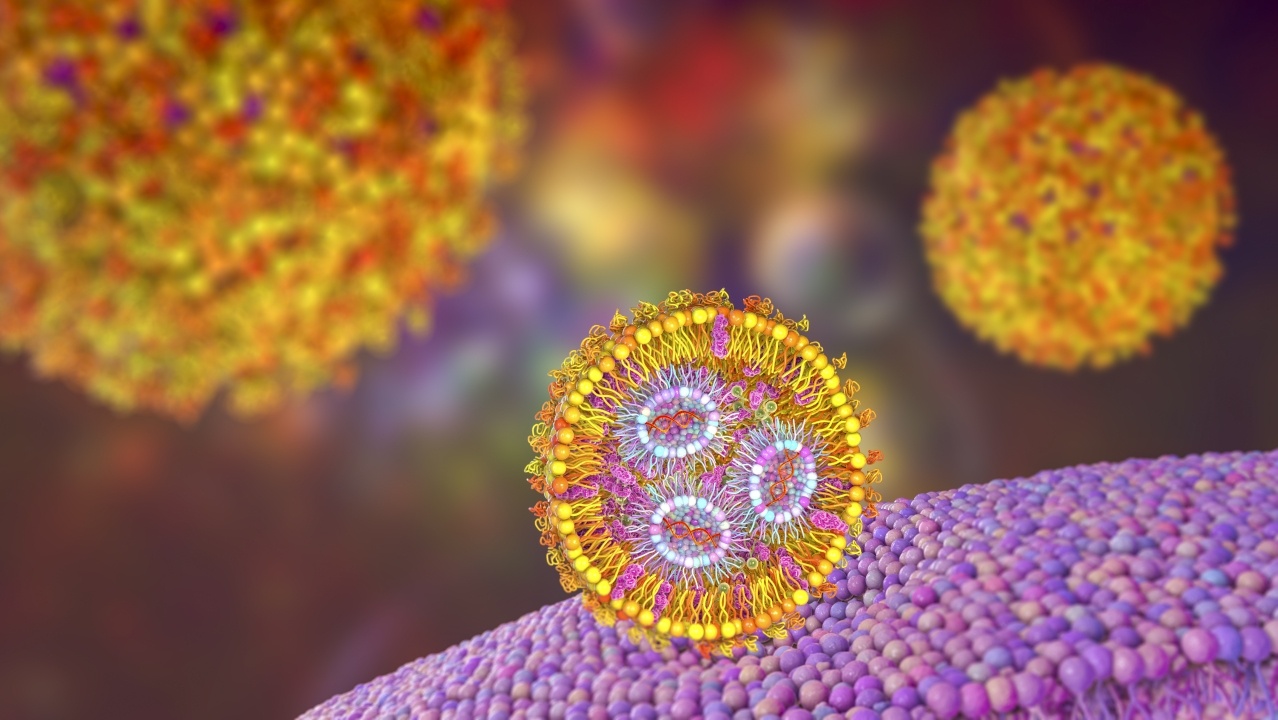
世界的な疾患の大流行がこの分野の研究とイノベーションを加速させた結果、有望視されていたメッセンジャー(m)RNAワクチンが長い年月を経てようやく実現しました。 しかし、mRNAワクチンの成功は、mRNAを保護し細胞内に送り込む、もうひとつの重要な技術である脂質ナノ粒子(LNP)なくしてはあり得ませんでした。 本記事では、脂質ナノ粒子研究の展望と、COVID-19以外にも広がるナノテクノロジーの未来の可能性について説明します。
リポソームから脂質ナノ粒子に至る道のりについては、ナノテクノロジーの概要、薬物送達への応用、RNA革命を実現する上で果たした役割、化粧品、農業など将来的な可能性に関するCAS Insights Reportで詳しくご覧ください。
ナノテクノロジーとmRNAワクチン:サクセスストーリー
SARS-CoV-2との闘いにおいて複数のワクチンが採用されました。中でも、モデルナ製とファイザー/ビオンテック製の2つの脂質ナノ粒子ベースのmRNAワクチンが最も幅広く使用されたことは、COVID-19大流行への対応でナノテクノロジーが果たした重要な役割を物語っています。 これらのワクチンが2021年大規模に接種されたことでパンデミックの流れが変わり、COVID-19の症例数が顕著に減少しました。
しかしながら、ウィルスの急速な拡散により、 SARS-CoV-2の複数の新しい変異株が発生し、今後も変異株の発生が予測されています。これは公衆衛生上の大きな課題となっています。 デルタ株やオミクロン株といった懸念される変異株は、中和抗体の機能を弱めることで、ワクチンの有効性に影響を与えています。 このようなSARS-CoV-2変異株の課題に取り組む鍵を握っているのが、ナノテクノロジーです。 科学者たちは現在、この目的でナノ粒子、ワクチン誘導、中和抗体、人工中和抗体、「ナノデコイ」(おとり)など、さまざまなナノテクノロジーの利用方法を模索しています。 後者は、細胞に発現するアンジオテンシン変換酵素2(ACE2)受容体と相互作用する、デコイとなるナノタンパク質を作り、ウイルスとACE2の結合を阻害し、宿主細胞を感染から防ぐ方法です。 新型コロナウイルスの大流行の終息を早めるために、これらのナノテクノロジーが展開されていますが、この集中的な研究努力から得られた知見を、その他の世界規模の感染症など、アンメットニーズのある分野にどのように適用できるでしょうか。
脂質ナノ粒子技術の開発
将来の展望に目を向ける前に、脂質ナノ粒子技術のこれまでの歴史を振り返ってみましょう。 すべての始まりは1965年のリポソームの発見です。これは水中で自発的に集合して脂肪莢膜を形成する、閉鎖した脂質二重構造を持つ小胞です。 低分子の薬剤をカプセル化し、その水溶性を高められるため、研究者たちは直ちに薬物送達に応用できる可能性に気が付きました(40%以上の低分子薬は低い水溶性を示すことがわかっています)。 初めてリポソームを発見して以来、この技術は継続的に修正・改良され、脂質ナノ粒子の機能を最適化して非常に汎用性に優れた薬物送達プラットフォームとリポソーム医薬品を生み出してきました。
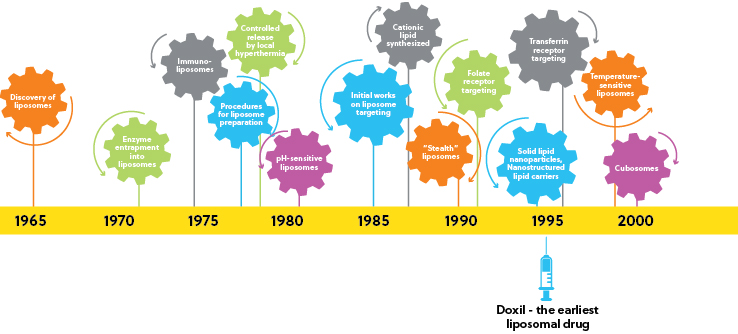
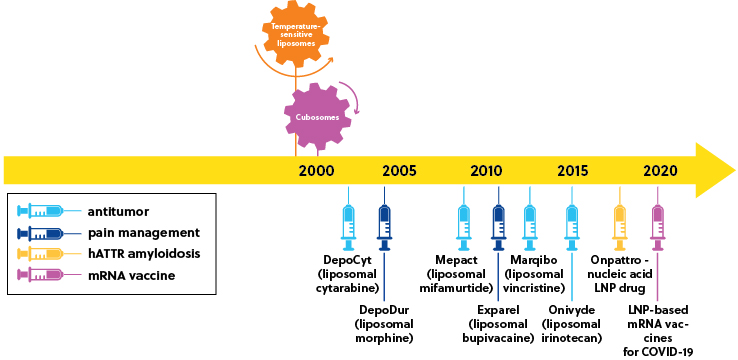
現在、COVID-19のmRNAワクチンの重要な構成要素として脚光を浴びていますが、脂質ナノ粒子は既に数10年にわたり医薬品として利用されてきました。 1995年には、抗癌剤ドキソルビシンのLNP製剤であるドキシルがリポソーム医薬品として初めて承認されました。 別のリポソーム医薬品であるEpaxalは、肝炎ワクチンとして使用されるタンパク抗原のLNP製剤です。 この進展に続いて、2018年にはアメリカ食品医薬品局がトランスサイレチン型遺伝性アミロイドーシスによる多発性神経障害の治療薬としてLNPベースの低分子干渉RNA薬Onpattro(パチシラン)を承認しました。 この重要なマイルストーンにより、ナノ粒子の送達を可能にする多くの核酸ベースの治療法について臨床開発の道が開かれました(脂質ナノ粒子の主要な進歩の年表については図1を、詳細についてはCAS Insights Reportを参照してください)。
ポストコロナの世界におけるナノテクノロジー
CAS コンテンツコレクション™の最近の分析では、脂質ナノ粒子に関連する研究の独特な状勢について調査しています。 この分析により、CAS コンテンツコレクション™に収録されている24万件以上のLNP関連の科学文献のうち、19万件以上が2000年から2021年のものであり、ナノテクノロジーへの関心が高まっていることが明らかになっています。 COVID-19での対応を踏まえて感染症対策にナノテクノロジーを応用することにより、ナノテクノロジーへの関心はさらに高まると予測されています。また、ナノ治療薬市場は2027年までに1640億ドル以上に達すると推測されます。
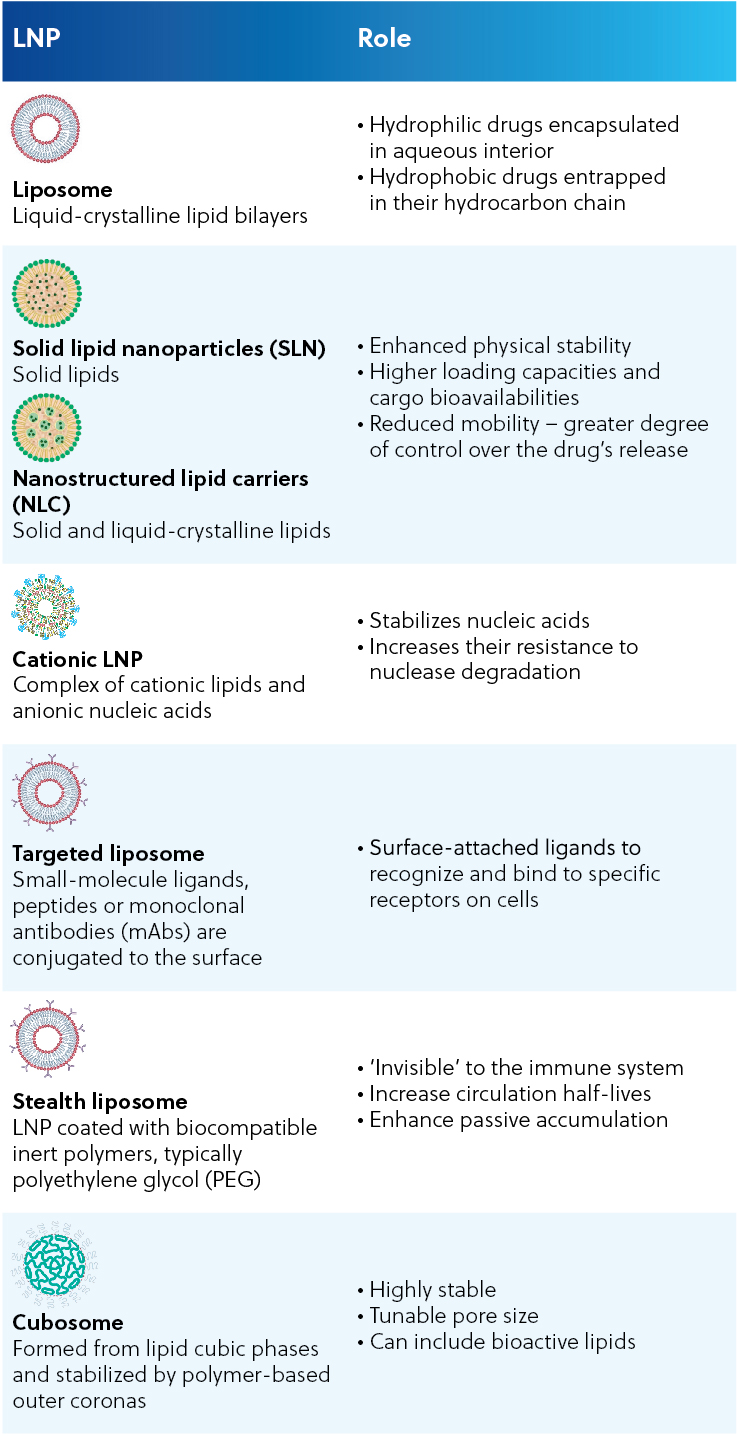
脂質ナノ粒子は長期間にわたり薬物送達システムの主流として認識されてきましたが、この技術にも制限があります。 LNPの第一世代とされるリポソームは、有機溶媒を用いた複雑な製造方法が必要なほか、封入薬では低効率を示し、大規模での実施は困難です。 固体脂質ナノ粒子とナノ構造脂質キャリアの開発など、主要なナノテクノロジーの進歩が一部の問題の克服に役立っている一方で(図 1を参照)、課題は残っています。 製造コスト、膨張性、安全性、ナノシステムの複雑さをすべて評価し、潜在的なメリットとのバランスを考慮する必要があります。 この技術の現在の制約を克服できるように、研究者は現在、次世代の脂質ナノ粒子に注目しています。より高機能で洗練された送達システムを見つけるためです。
表1:脂質ナノ粒子の種類:構造と役割
COVID-19のmRNAワクチンに対するナノテクノロジーの応用が成功したことで、マラリア、結核(TB)、ヒト免疫不全ウイルス(HIV)などの感染症の治療に対するこの技術の応用に、再び関心が高まっています。 ナノテクノロジーは、このような疾患の検出と治療のいずれも変革できる可能性を秘めています。 技術に汎用性があるため、リポソーム、ポリマーナノ粒子、ナノ薬物結晶に封入した治療薬を局所または全身に送達し、徐放または速放できることになります。 無限の可能性を秘めたテクノロジーです。
ただし、HIVなど一部の感染症は集中的な研究の的となっている一方で、マラリアや結核などの感染症はあまり熱心に研究されていません。 このようなアンメットニーズが存在する分野におけるナノテクノロジーの進歩は、資金調達(または資金不足)が歴史的に制約要因となっています。 しかし、この状況は変わりつつあります。 ジョンズ・ホプキンズ大学の研究チームは、遺伝子治療薬の送達に用いる脂質ナノ粒子の設計を迅速化し、そのプロセスを従来より安価に実現するプラットフォームを開発しています。 この研究チームは現在、この技術を利用し、肝臓に寄生するマラリア発症の原因となる寄生虫を標的としたマラリアワクチンを開発しています。
ナノテクノロジーの明るい未来
ナノテクノロジーは、科学、特に医学の分野で新たな地平を切り開きました。 COVID-19のmRNAワクチンの送達ベクターとしての脂質ナノ粒子の使用は、今後さらに研究の幅を広げることでしょう。 より高度で多機能なナノキャリア設計の薬が、現在または将来のアンメットニーズに対応することになります。
脂質ナノ粒子技術の過去、現在、未来の機会に関する、より詳細な状勢の分析については、CAS Insights Reportをご覧ください。



