COVID-19の感染者が世界中で再び増加する中、米国で現在主流の株はオミクロン亜系統のBA.5となっています。 COVID BA.5変異株は、変異を繰り返しながら拡散を拡大し、免疫を回避し続けています。最近の査読前の研究によると、再感染には大きな健康リスクがあり、そして新しい変異株は治療用モノクローナル抗体(mAb)の影響を受けにくい可能性があることが示されています。そこで本ブログでは、感染を増加させ、防御抗体を回避し、(再)感染率を高める主な変異について探ります。
変異は感染率を上昇させる
人体への侵入の際、鍵となるタンパク質はスパイクタンパク質です。そこで、多くのCOVIDワクチンがこれを標的とし、中和しています。しかし、オミクロンの変異株(BA2.12.1、BA.4、BA.5)のスパイクタンパク質による最近の変異は、感染を強化するような重大な変化が起きていることを示唆しています。

図1に見られるように、これら3つの変異株は、受容体結合ドメイン(RBD)の一部を改変する、重要な変異を共有しています。 これは細胞と結合して感染を可能にするスパイクタンパク質の部分であり、また防御抗体の重要な標的でもあります。
BA.4とBA.5に見られるF486V変異は、スパイクがウイルス受容体と結合する能力に支障をきたします。 それに対して、R493Q復帰変異は受容体結合を回復させるため、適応性も回復されます。
変異は治療に対する耐性を高める
変異には、ウイルスの拡散が早くなるものがある一方、現行の治療の効果が薄まる変異もあります。L452の変異では、ウイルスは細胞により密接に結合するため、ウイルスを遮断しようとする抗体に見つかりにくくなる場合があります。 研究者によればこのL452変異は、今年初めの大規模なオミクロン感染急増に対するCOVID-19ウイルスの反応だと考えています。BA.4とBA.5も、抗体結合部位を無効にし、結合親和性に変化をもたらしてきたN末端ドメイン(NTD)の変異(Del69-70)を有しています。 F486VとR493Qの変異も、抗体との結合による免疫を回避することに寄与し、その結果mAbの効果を低下させ、最終的に治療抵抗性を高めている可能性があります。
ベブテロビマブ(CAS登録番号 2578319-11-4)は、BA.2.12.1、BA.4、またはBA.5感染症に対して臨床的に承認された唯一のmAbで、これらの新しい亜系統に対しても有効性は保たれています。ベブテロビマブは、ヒト免疫グロブリンG-1(バリアント)モノクローナル抗体です。
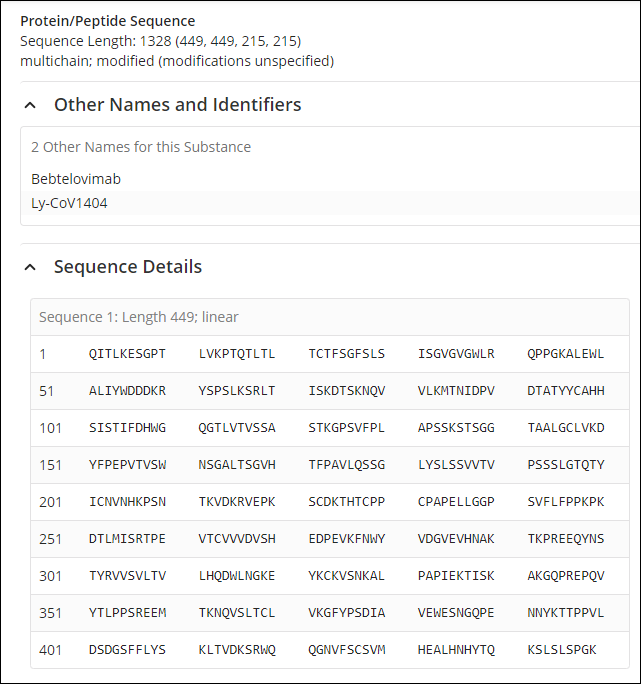
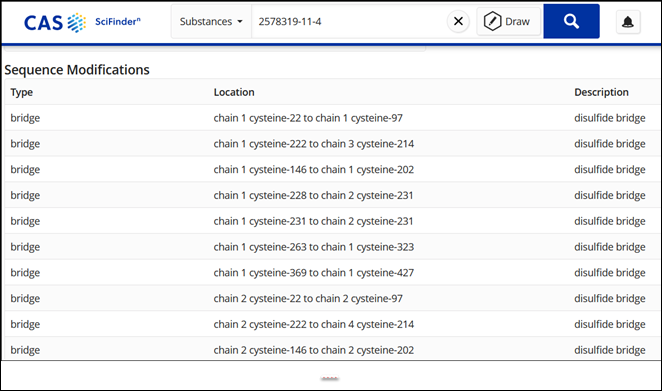
CAS SciFindernによる物質検索では、この治療薬には4つのタンパク質配列、449のアミノ酸からなる2つの同一の重鎖ポリペプチドと、215のアミノ酸からなる2つの同一の軽鎖ポリペプチドが含まれていることが分かります。 図2と図3に示すように、CAS SciFindernでその配列と変更箇所を確認することができます。
New England Journal of Medicineに最近発表された論文では、ワクチン接種と感染の両方により誘発される中和抗体を、BA.2.12.1、BA.4、BA.5の亜系統がいかに回避しているかが解明されています。 つまり、BA.4またはBA.5亜系統に対する中和抗体価は、また(より少ない度合いで)BA.2.12.1亜系統に対する抗体価も、以前のBA.1およびBA.2亜系統に対する抗体価より低くなっていることが示されているのです。この調査結果は、高頻度のワクチン接種や感染歴のある対象集団において、現在なぜBA.2.12.1、BA.4、BA.5変異株が急増しているのか、その背景を提供しています。
スパイクタンパク質の変異以外での特徴
BA.4とBA.5はスパイクの変異という点では同じですが、スパイクタンパク質外の変異については共通点と相違点があります。 これらの変異は、ウイルスの複製、感染率、治療抵抗性に影響を及ぼします。 BA.4とBA.5は、いずれも変異が2回分戻り、Orf6 D61とNSP4 L438という元のウイルスになっています。研究者は、これらの変異が複製に影響を及ぼしていると考えています。 Orf6 D61内在のタンパク質Orf6は、タンパク質や酵素、そしてさまざまなシグナルのダウンレギュレーションをすることで、ウイルスの複製を促進します。 NSP4 L438常駐タンパク質NSP4は、二重膜小胞の形成に関与しているため、これもウイルスの複製を促進している可能性があります。
BA.4には、Orf7BのL11Fとヌクレオカプシド(N)タンパク質のP151Sという2つの変異がありますが、その影響は、Nタンパク質を検出する抗原検査ではまだ確定できていません。 Orf7BとNタンパク質の変異は、いずれも免疫回避に寄与していると考えられます。 また、Nタンパク質の変異も、ウイルスの安定性に影響し、その結果適応性が高まることが考えられます。 BA.5では膜(M)タンパク質でD3N変異が見られます。これは比較的珍しい変異です。 膜タンパク質は免疫抑制の役割を果たすとともに、ウイルスを取り囲むため、細胞への侵入や感染性を高めることに寄与していることが考えられます。
ワクチンは入院の予防に効果的であることが証明される
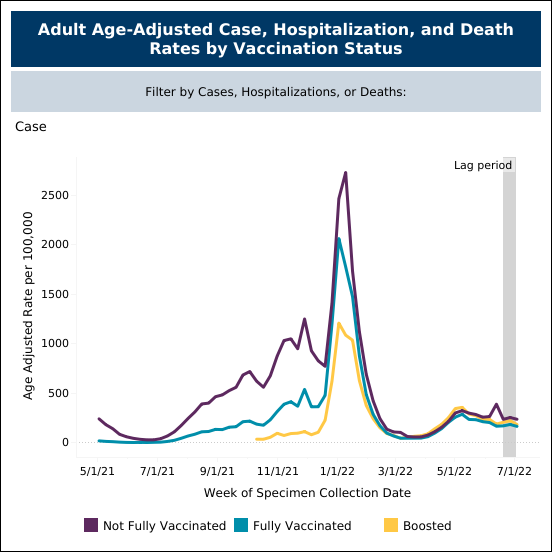
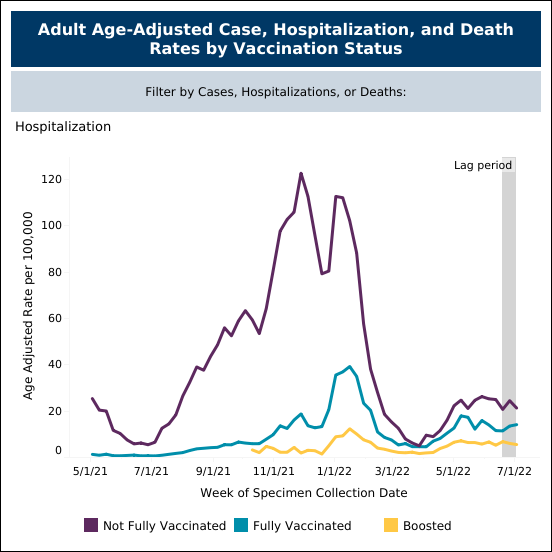
現在のCOVID-19ワクチンは、症候性感染に対しては最小限の予防効果しかありません。これは、BA.5変異株が猛威を振るった6月と7月に、接種完了者と未接種者がほぼ同じ確率で感染したことを示すミネソタ州保健局のデータでも明らかになっています(図4)。 ところが、入院率を調べると、ワクチン未接種者の方が入院数が大幅に多く、その差は歴然です(図5)。
現在のワクチンは、重篤な症状や入院、死亡に対しては十分な予防効果があります。 これらのワクチンで獲得した免疫は、患者の免疫系がウイルスと戦うのを助けるため、結果的に重症化や入院の可能性が低くなります。
New England Journal of Medicineに掲載された論文によると、現行のCOVIDワクチンは、BA.1およびBA.2変異株に対しても有効であることが述べられています。 この交差免疫は、パンデミック当初から認識されていました。 インフルエンザ、はしか、肺炎、小児まひのワクチンは、すべてSARS-CoV-2感染に対して、ある程度の予防効果を有していることを示唆する証拠があります。 メイヨー・クリニックによると、前の年に肺炎ワクチンを接種した人はCOVID-19の感染リスクが28%低下した一方、小児まひワクチンの接種を受けた人はCOVID-19感染リスクが43%低減したことが確認されています。
次のステップ - 今後の研究の方向性
ウイルスが世界中で変異し、進化し続けていく中、COVID-19のパンデミックが衰える兆しはありません。 しかし上記で示されるように、現在のワクチンは重症化、入院、そして死亡に対して依然として高い有効性を持っています。 ところが、COVID疲れにより、推奨されるブースター接種を受けない人が多くいます。 対象者であってもまだブースター接種を受けていない方は、できるだけ早く受けるようにするべきです。 また、密閉空間や人混みでは、引き続き高品質なマスクを着用することで、症候性感染症の抑制につながります。
ファイザーとモデルナの両社は、新しいBA.1変異体をベースにしたワクチンを開発しており、2022年の秋季には米国で接種可能になる予定です。ただし、以前BA.1に感染したことがあっても、より新しい変異株に対する防御力は限られていることから、この種の第2世代ワクチンがどの程度有効なのかを疑問視する声もあります。 将来的には、ウイルスの蔓延を食い止めるためには、より幅広い抗原を標的とした抗ウイルス療法と、より新しいワクチン技術を組み合わせることが必要になるでしょう。
