Gain new perspectives for faster progress directly to your inbox.

現在、RAS遺伝子および関連がん遺伝子は、すい臓がん、肺がん、大腸がんなど、世界のがんの30%以上に影響を及ぼしています。 以前これらは、結合部位が浅く、困難な位置にあり、また酵素活性が低いことから、アンドラッガブルな標的とされていました。 共有結合阻害剤の有名な例としては、最近FDAから承認されたソトラシブ(ルマケラス®)があります。これは、2024年には10億ドルを超える売上が予測されているほど成長中のRAS阻害剤クラスのひとつです。
標的共有結合阻害剤は、誘導システムと弾頭(図1)を活用するもので、この方式は、結合しやすく、標的性が高く、有害な副作用も少ないことが証明されています。 2000年までは、標的と共有結合を形成する薬剤の多くは、非選択的であったため、望ましくない副作用を引き起こしていました。 その結果、共有結合阻害剤は理想的な薬剤候補ではないと考えられるようになり、製薬業界による開発は限定的なものに留まっていました。 ところがここ数年の間に、共有結合阻害剤は目覚ましい復活を遂げています。これは、過去10年間でリンパ腫、肺がん、乳がんの治療薬が8つ承認されているなど、米国FDAの承認件数が増加していることからも明らかです。
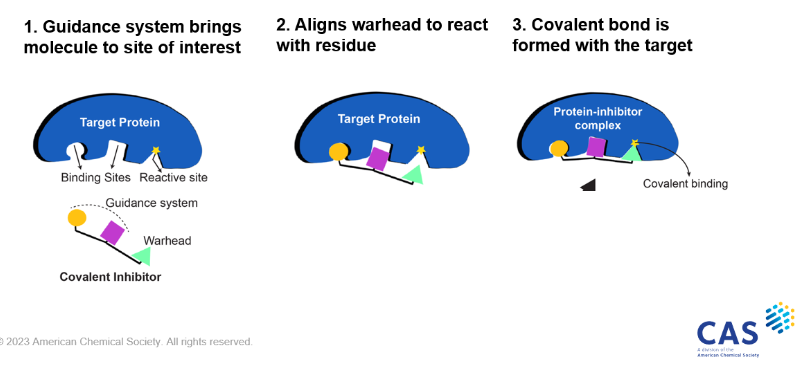
現在、この「弾頭」は、目的の標的に配置されたときに初めて共有結合を形成するなど、細かく調整された反応性を示す、卓越した機能性を持つものが設計されるようになってきています。 そうした中、Totus Medicines社とCASの専門家により、2023年10月19日に共同でウェビナーが開催されました。
そこでは、標的共有結合阻害剤に関する最新の開発動向や、今までアンドラッガブルだった標的に対してそれがいかに適用されているかなどが紹介されています。 なお、共有結合阻害剤における活動状況など、さらなる有益な洞察については、ChemRxivに最近掲載された論文に基づくCASの記事もご覧ください。
ウェビナーの主なハイライト

今回のディスカッションの導入として、まずGary Gustafson博士により、この新しい科学分野の現状説明がありました。 出版物や知的財産から標的共有結合阻害剤の研究で進展があることが示唆される中、その真の可能性についての理解が深まってきています。 共有結合阻害剤の状勢を深く掘り下げることで、最も頻繁に使用されている弾頭や、そこで標的とされているタンパク質、また対応しようとしている適応症などに関する洞察や傾向が明らかになっています。

Neil Dhawan博士からは、共有結合阻害剤がいかに精密な結合を形成し、広範囲にわたる疾患の治療選択肢を提供しているかの説明がありました。 博士は、PI3Kαの生物活性に関するTotusの最新の研究に加え、高度に特異的な方法でPI3Kαを完全に阻害できるTOS-358という分子についても紹介しました。 そして結論として、複数のPI3Kα変異腫瘍の治療薬としてTOS-358を早期承認に進めるため、どんな臨床的アプローチがあるかなどの話をしました。
締めくくりに、参加者から幅広い質問が寄せられました。その中には、何が共有結合の創薬復活のきっかけになったのかといったものから、共有結合による創薬にはどのような画期的な新技術が活用されているか、などの質問もありました。 この日は、標的共有結合阻害剤の有望な可能性や、それがどのようにがんを治療するのかの仕組みなど、非常に興味あるパネルディスカッションになりました。
ウェビナーの動画や関連スライドは、こちらでご覧ください。