La enzima convertidora de angiotensina 2 (ECA2) es una proteína que ha captado una atención considerable en los últimos años por su papel como receptora del virus SARS-CoV-2, pero la oleada de investigación sobre la ECA2 también ha revelado posibilidades interesantes para su uso como diana terapéutica en otras enfermedades.
¿Qué es la ECA2?
La ECA2 es una proteína de membrana con un dominio enzimático que se localiza en la superficie externa de las células humanas. Su nombre se debe a que esta proteína se identificó inicialmente como un homólogo (o una variante) de la enzima convertidora de angiotensina (ECA), una enzima que interviene en la formación de la hormona peptídica angiotensina II a partir de la angiotensina I. La ECA ha sido objeto de numerosos estudios y es un conocido vasoconstrictor (es decir, causa la contracción de los músculos de la pared de los vasos sanguíneos y el estrechamiento de la luz de estos).
La ECA2 —de la que hoy se sabe que es un receptor vírico— también actúa como vasodilatador, de forma que contrarresta la acción de la ECA y provoca la relajación de las paredes de los vasos sanguíneos. Tanto la ECA como la ECA2 son elementos esenciales en el sistema renina-angiotensina (SRA) que regula la presión arterial y el flujo sanguíneo a diversos órganos, como los pulmones, el corazón y los riñones.
Funciones de la enzima convertidora de angiotensina 2
El sistema renina-angiotensina abarca una compleja red de enzimas, hormonas peptídicas y receptores, como se muestra en la figura 1. El precursor de la angiotensina (Ang) es el angiotensinógeno; lo secreta el hígado y lo escinde una enzima renal, la renina, para producir angiotensina I (Ang I). A continuación, la ECA convierte la Ang I en angiotensina II (Ang II). La Ang II, un péptido hormonal de ocho aminoácidos, se une a los receptores de angiotensina tipo 1 (AT1R) en la superficie de las células musculares de los vasos sanguíneos pequeños para ejercer un efecto vasoconstrictor. También estimula la reabsorción de sodio por parte de los riñones. Juntas, la vasoconstricción y la reabsorción de sodio favorecen el aumento de la presión arterial. Por consiguiente, una actividad de ECA anormalmente elevada supone un aumento del nivel de Ang II, que a su vez desemboca en hipertensión.
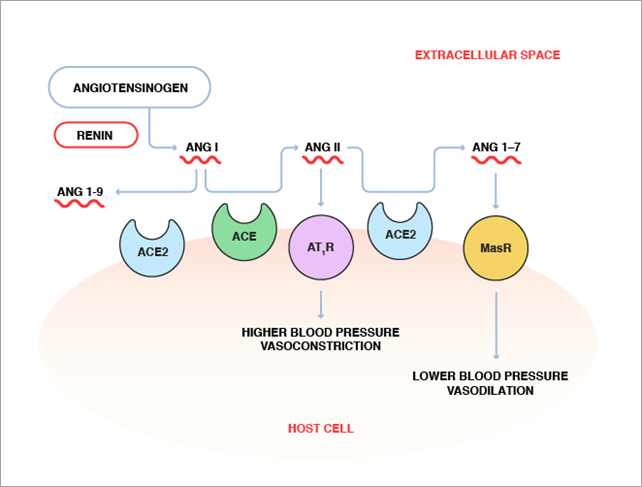
Por el contrario, la ECA2 cataliza la conversión del péptido de ocho aminoácidos, Ang II, en un péptido de siete aminoácidos (Ang 1-7), que parece tener el efecto contrario al de la Ang II al actuar sobre un receptor diferente, llamado receptor Mas (MasR). Si bien el papel exacto de la Ang 1-7 en la regulación de la presión arterial todavía no se ha caracterizado por completo, hay datos que indican que reduce la presión arterial e induce la vasodilatación. Además, la ECA2 escinde la Ang I en Ang 1-9, por lo que puede contrarrestar todavía más el efecto de la ECA al eliminar el sustrato de esta. Al provocar la conversión de Ang II en Ang 1-7 y de Ang I en Ang 1-9, la ECA2 puede contribuir a mantener el equilibrio entre vasoconstricción y vasodilatación necesario para el control de la presión arterial.
Papel de la ECA2 en la infección por el virus SARS-CoV-2
Desde el inicio de la pandemia de COVID-19, los científicos se han esforzado por conocer en profundidad el virus SARS-CoV-2, dilucidar el mecanismo de evolución de la enfermedad e identificar opciones de tratamiento. Se han realizado extensas investigaciones para identificar genes y proteínas viables como dianas para los agentes terapéuticos. Ya en las primeras etapas de la pandemia se descubrió el importante papel que la ECA2 podía desempeñar como receptor del virus SARS-CoV-2.
La proteína de la espícula (proteína S) que se encuentra en la superficie de los virus SARS-CoV-2 y SARS-CoV puede reconocer la ECA2. La ECA2 y la proteína S se unen de forma similar a como lo hacen una llave y una cerradura, lo que permite que el virus se introduzca en las células humanas (figura 2).
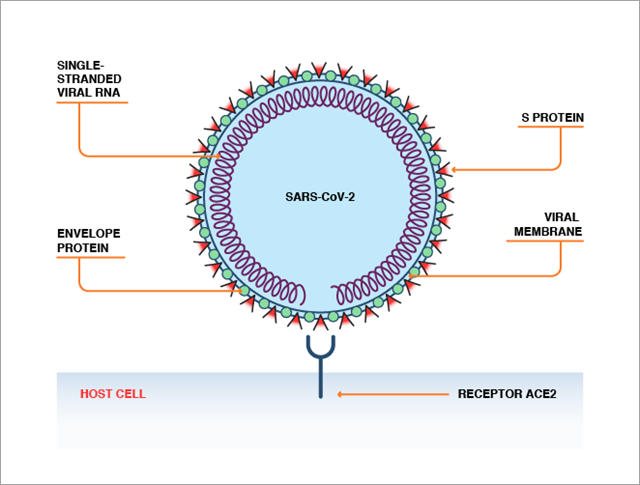
Aunque el SARS-CoV-2 es muy similar al SARS-CoV —el virus que causó el síndrome respiratorio agudo grave (SARS)—, algunas mutaciones en el dominio de unión al receptor de la proteína S han aumentado considerablemente la afinidad de unión del virus SARS-CoV-2 a la ECA2. Es posible que estas diferencias expliquen la mayor transmisibilidad de la COVID-19. Se ha constatado que la ECA2 se expresa en los pulmones, el sistema digestivo, el corazón, las arterias y los riñones. Además, se sabe que la expresión de ECA2 aumenta con la edad y que es más alta en las personas que padecen enfermedades cardiovasculares, lo que podría explicar por qué la COVID-19 es más grave en estas subpoblaciones.
Interacciones de la proteína ECA2 con los tratamientos de la COVID-19
Aunque actúe como sitio de anclaje para el SARS-CoV-2 y facilite la entrada del virus en las células del anfitrión, la ECA2 no está sola en este proceso. Hay otras enzimas del organismo anfitrión que también intervienen para facilitar la entrada del virus. Las enzimas denominadas proteasas se encargan de eliminar fragmentos tanto de ECA2 como de proteína S para favorecer el proceso de interacción. Otras enzimas modifican el complejo ECA2-proteína S empaquetado en vesículas unidas a la membrana para facilitar la entrada del virus en la célula del anfitrión. Así pues, no solo la ECA2 y su interacción con el SARS-CoV-2, sino también todas las demás proteínas que intervienen en este proceso, podrían ser dianas válidas para los agentes contra la COVID-19.
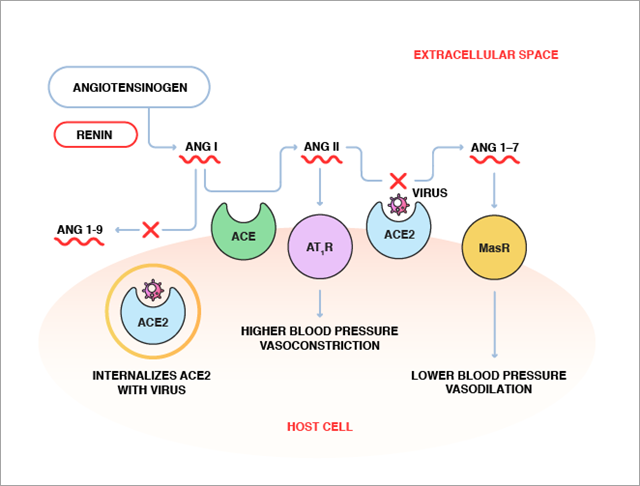
Se ha sugerido que, en el momento de la unión vírica, es posible que el virus bloquee el dominio catalítico de la ECA2, lo que limitaría el acceso al sustrato, la Ang II, y provocaría la acumulación de Ang II. Además, con la entrada del virus, es posible que la ECA2 que se encuentra en la superficie celular se introduzca en la célula junto al virus, lo que disminuiría la función enzimática de la ECA2 (figura 3). Como resultado de la disminución de la actividad de la ECA2, el nivel de Ang II circulante puede aumentar, como se ha observado en pacientes con COVID-19. El nivel de Ang II presenta una correlación lineal positiva con la carga vírica y la lesión pulmonar, lo que indica una relación directa de la disminución de la concentración tisular de ECA2 con el desequilibrio del SRA y el desarrollo de daño orgánico en pacientes con COVID-19. No obstante, es necesario realizar más estudios para confirmar esta conclusión.
Posible papel de la ECA2 como diana de los tratamientos contra la COVID-19
En vista de la función primordial que desempeña la ECA2 en la invasión de las células del anfitrión por el virus SARS-CoV-2, algunas iniciativas se están dirigiendo hacia el desarrollo de medicamentos que puedan bloquear esta función. Hasta la fecha, para esta aplicación todavía no se ha aprobado ningún medicamento de moléculas pequeñas por la vía del reposicionamiento de fármacos. Sin embargo, hace poco ha concluido el desarrollo de un medicamento biológico que puede lograr este objetivo. Este medicamento de grado clínico, la ECA2 humana recombinante (ECA2hr) soluble, se concibió inicialmente para combatir el síndrome de dificultad respiratoria aguda (SDRA).
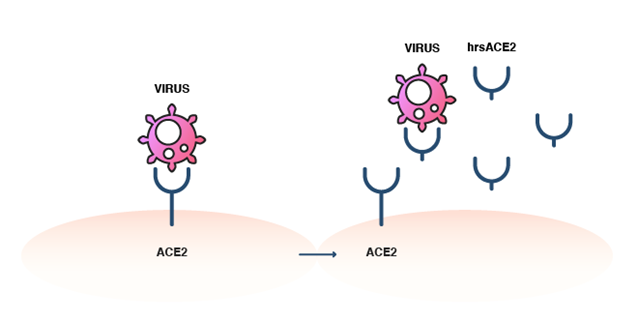
La ECA2hr soluble no incluye el segmento de unión a la membrana y, por tanto, no se puede adherir a las células humanas. Sin embargo, sí se puede unir al virus SARS-CoV-2 actuando como receptor señuelo. Al unirse de forma competitiva al coronavirus, impide la unión de este a la ECA2 natural, unida a la membrana, y bloquea así la entrada del virus en las células del anfitrión (figura 4). Diversos estudios realizados en cultivos celulares y varios organoides han revelado que la ECA2hr inhibe la infección de las células del anfitrión por el virus. Asimismo, según reveló un ensayo clínico realizado en 2017, parece que se tolera bien y que provoca una rápida disminución del nivel sérico de Ang II en los pacientes con SDRA. Cabe esperar que la ECAhr soluble será el primer medicamento dirigido a la ECA2 y que abrirá la puerta a otros tratamientos específicos para luchar contra la COVID-19. La ECA2hr ha mostrado potencial como tratamiento de combinación y ha mejorado el efecto de remdesivir en la infección por SARS-CoV-2.
Aplicaciones terapéuticas futuras de la ECA2
Más allá de la COVID-19, la vía de la ECA2 ofrece una ruta potencial para tratar otras enfermedades respiratorias, como la nueva gripe de 2009 (H1N1) y la gripe aviar (H5N1), probablemente mediante el desarrollo de ECA2 recombinante para el uso con un inhibidor de AT1R o de ECA. Las enfermedades cardiovasculares son otra área en la que ECA2 despierta un interés creciente, y nuevas dianas como la ECA2 podrían ayudar a encontrar formas más eficaces de controlar la hiperactividad de RAS, que desempeña un papel muy importante en problemas como la hipertensión. Es probable que la ECA2 también sea una diana importante en la lucha contra la diabetes de tipo 2, por ejemplo, mediante el uso de vías mediadas por ECA2 para contrarrestar los efectos del exceso de actividad de Ang II en el riñón de los diabéticos.
El papel creciente del ARN en el desarrollo de nuevos tratamientos está transformando el panorama del descubrimiento de fármacos. Manténgase al día con CAS. Explore el informe de CAS Insights sobre las novedades del panorama de los tratamientos derivados del ARN.



