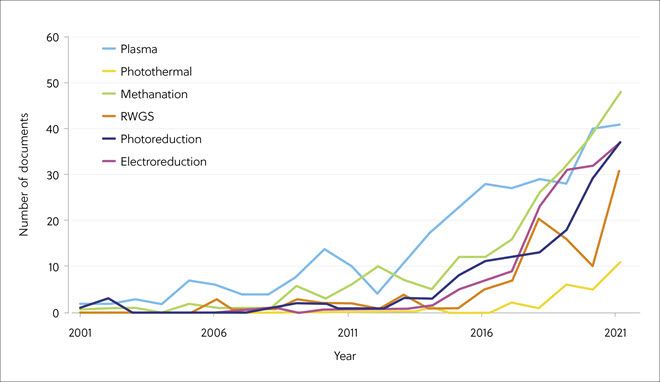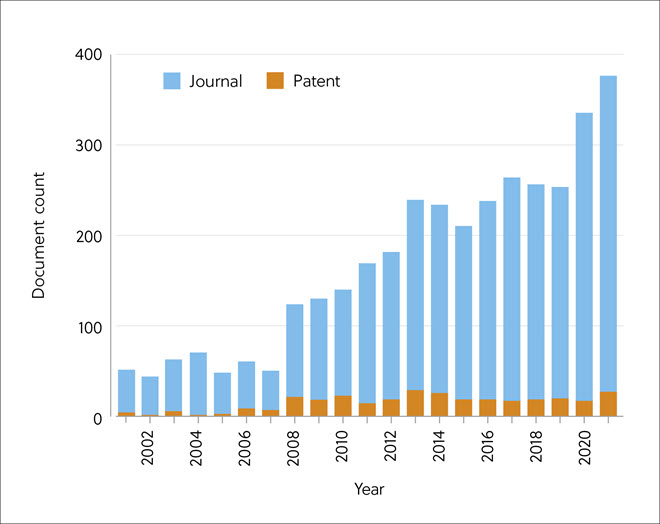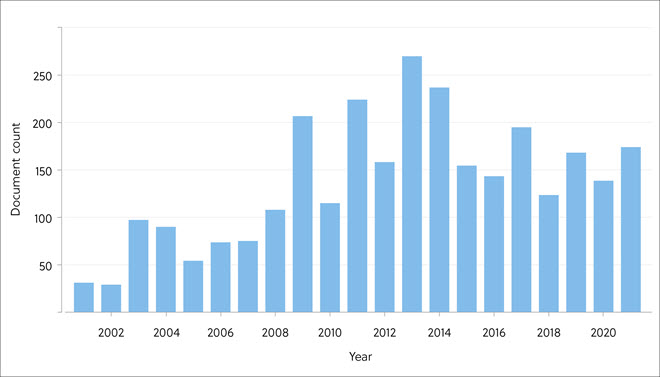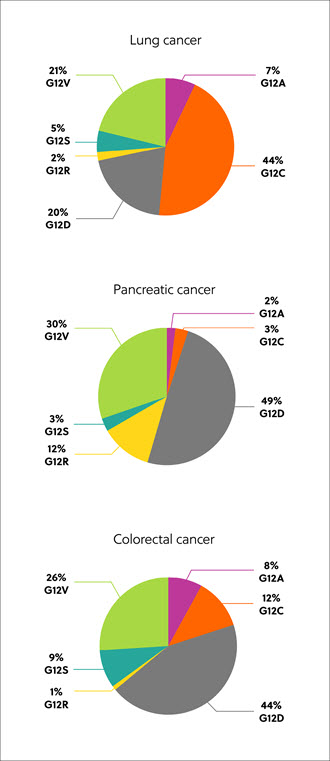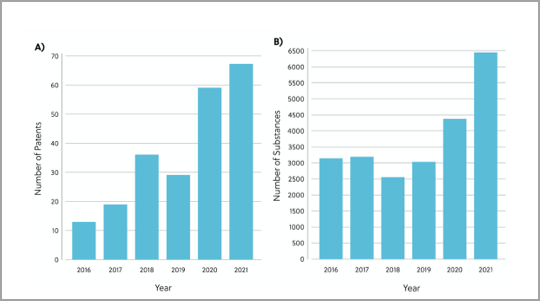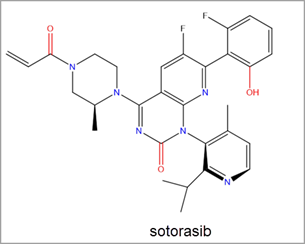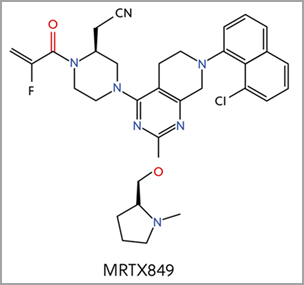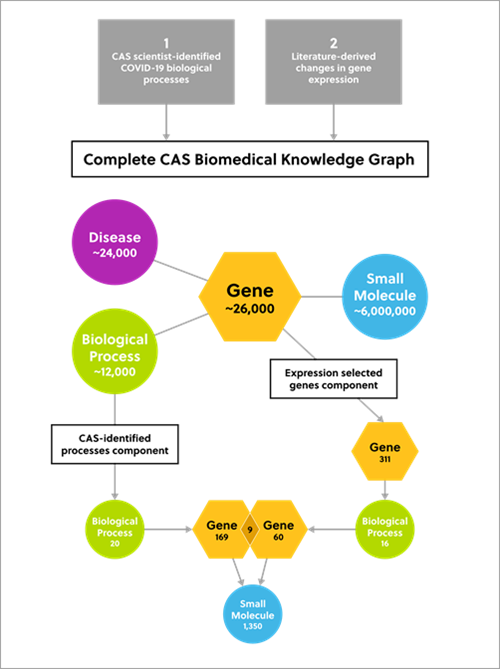
过去十年间,研究、临床开发和商业活动都发生了极大转变,RNA 逐渐应用于医学领域。 随着用于 COVID-19 mRNA 疫苗的脂质 RNA 纳米颗粒的开发迅速成功,以及数种相关药物获批,RNA 已一跃成为药物研究的前沿。 这篇经同行评审的文章(刊载于《化学信息与建模杂志》 (Journal of Chemical Information and Modeling))借助 CAS 内容合集来研究 RNA 在药物开发中的多方面益处。 这包括研究其作为新疗法(药物或靶标)的潜力。 其中还研究了医学领域中 RNA 的当前研究布局和趋势。