最近,世界卫生组织 (WHO) 对一种备受关注的新 SARS-CoV-2 变体进行了分类。 这种名为 Omicron (B.11.539) 的新变体最初是南非一个强大的基因测序网络发现的,并报告给了世界卫生组织。 这种特殊的变体是迄今为止最严重的突变,包括 50 多个已确定的突变,其中 30 多个位于刺突蛋白上。
为什么 Omicron 变体如此令人担忧?
对 Omicron 变体的初步研究表明,与 2019 年在中国首次发现的原始病毒相比,它已显著进化。这意味着它重新感染那些已经感染过 COVID-19 的人或逃避目前接种第一代疫苗所产生的免疫的可能性会加大。 这一变体可能会严重阻碍全球疫情后的复苏,对社会和经济造成巨大的影响。
Omicron 变体的结构是其引发对免疫逃避和传播(即使是接种过疫苗的人群)更大担忧的主要因素。 它的多重受体结合域 (RBD) 和 N 末端域 (NTD) 突变与中和性抗体的抗性有关,而蛋白酶裂解突变预期会使病毒更容易进入细胞或增加传播。 事实上,多项研究表明,这些突变会影响免疫系统中和突变的 SARS-CoV-2 病毒的能力,甚至可能将免疫中和能力降低 10 倍。
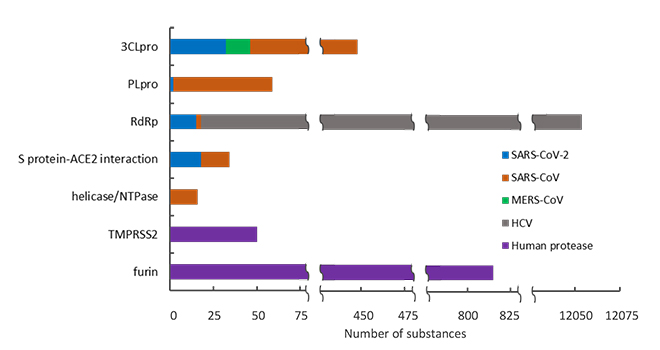
这种新变体最初在南非发现,目前在澳大利亚、欧洲、加拿大、亚洲以及最近在美国也有发现。 然而,许多专家认为,根据之前对 Delta 变体传播的经验,Omicron 已经遍布全球大部分地区。 尽管已经有小分子药物(例如萘莫司他、甲磺酸卡莫司他)可靶向 SARS-CoV-2 的非突刺蛋白,并且可能对 Omicron 仍然有效,但对于结束这场疫情,为当前和未来的变体开发一种可持续的疫苗至关重要。
刺突蛋白的作用
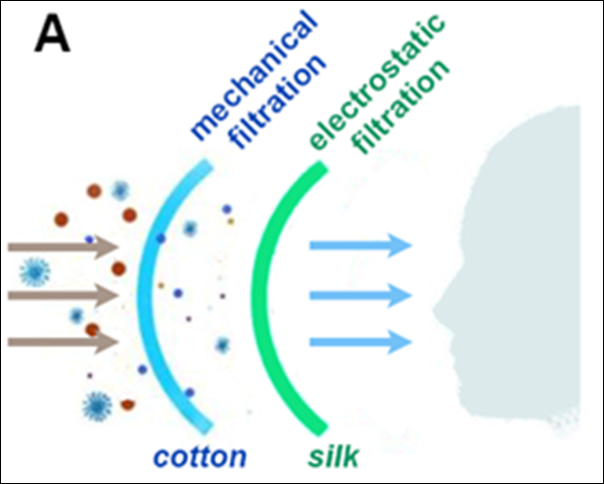
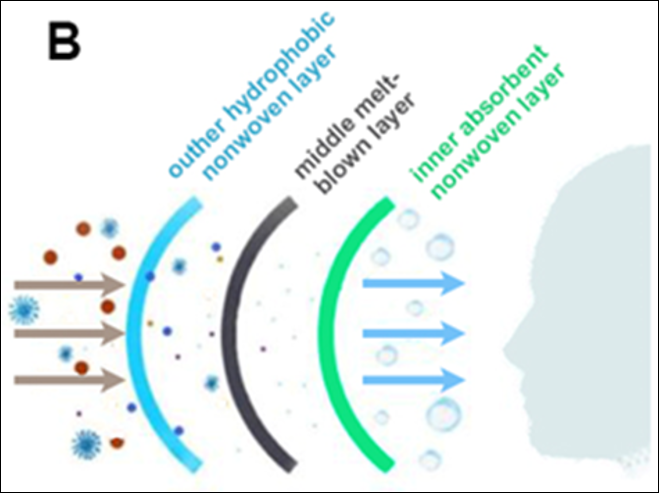
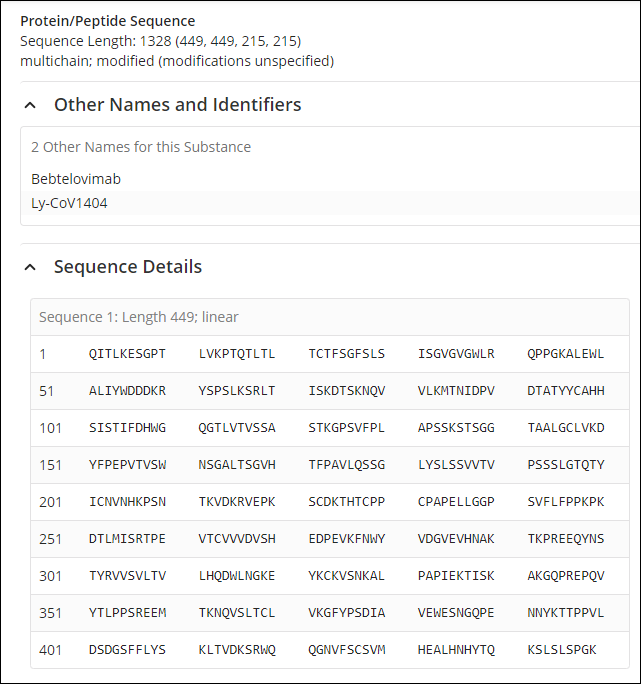
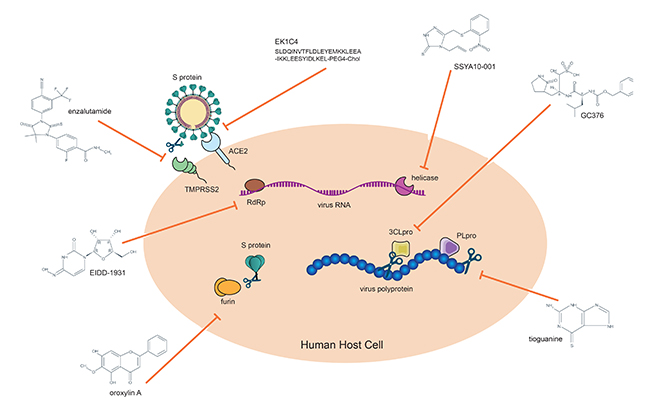
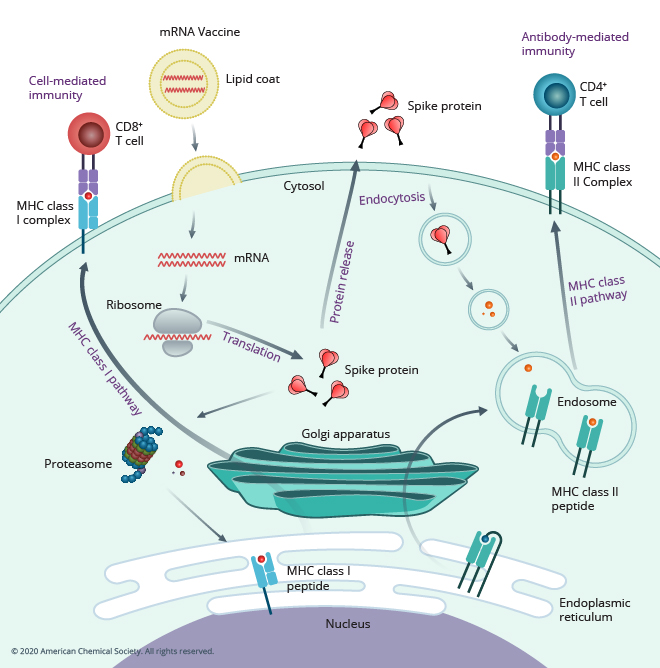
综上所述,如下图所示的 SARS-CoV-2 病毒刺突蛋白是第一代 COVID-19 疫苗靶向的关键抗原,因为它能使 SARS-CoV-2 病毒进入人体细胞。 目前的 mRNA 疫苗通过将 S 蛋白编码为抗原来中和它。
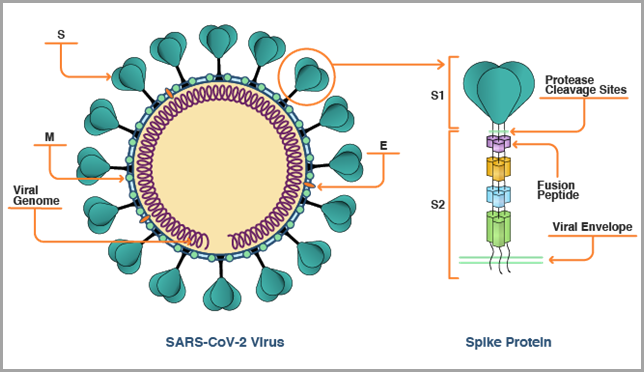
SARS-CoV-2 病毒的快速进化迫使研究人员评估 S 蛋白本身是否足以作为疫苗设计的抗原。 随着最初的疫苗和治疗剂组合正在被部署以遏制疫情,科学家们现在必须考虑过去两年中我们对 SARS-CoV-2 病毒的免疫反应所了解的所有信息,哪些反应与保护性免疫相关,以及这些研究对构建第二代疫苗的潜在意义,第二代疫苗可能需要扩展或放弃不断突变的 S 蛋白。
获得持续免疫的途径
许多因素决定了人类如何研发“保护性免疫”,特别是针对 SARS-CoV-2 等不断进化和变异的病毒。 理想情况下,我们希望实现一种免疫反应,能够识别并阻止入侵的病毒和细菌。 保护性免疫包括体液免疫和细胞免疫。 最近发表的一些对 SARS-CoV-2 的免疫反应的研究报告如下表所示。 感染幸存者对 COVID-19 蛋白的抗体和T细胞反应似乎很广泛,但并不完全。 这些反应主要针对病毒结构蛋白(如 S 蛋白、核蛋白、膜蛋白)。 这些反应的子集可能负责保护性免疫。
| 体液免疫 | 细胞免疫 | ||||
| 蛋白抗原 | IgG* | IgA* | CD4 T 细胞 | CD8 T 细胞 | 记忆 T 细胞 |
| 3C 样蛋白酶 | + | + | |||
| S 蛋白 | + | + | + | + | + |
| 核蛋白 | + | + | + | + | + |
| 小包膜蛋白 | + | ||||
| 膜蛋白 | + | + | + | + | |
| Orf3 蛋白 | + | + | |||
| Orf6 蛋白 | |||||
| Orf7a 蛋白 | + | ||||
| 辅助蛋白 7b | + | ||||
| Orf8 蛋白 | + | + | + | ||
| Orf10 蛋白 | |||||
*包括针对 S 蛋白的中和抗体
S 蛋白抗原覆盖在病毒表面,免疫系统很容易发现它,是保护性免疫的理想靶点。 但是,上表中显示的一些体液免疫反应和细胞免疫反应针对的是刺突蛋白以外的 SARS-Cov-2 抗原。 这些观察结果以及病毒变异体和突破性感染的出现表明,专注于针对单一抗原(即 S 蛋白)的免疫反应的疫苗可能无法提供有效疫苗所需的广泛免疫。 这些类型的中和抗体通常是保护性免疫反应的必要部分,但不足以建立持久免疫。 针对其他 SARS-CoV-2 抗原的体液反应和细胞反应是否提供广泛的保护性免疫需要进一步研究。
我们可以从流感疫苗中获得哪些持续免疫力的经验教训?
尽管我们并不完全了解 SARS-CoV-2 感染中的保护性免疫,但最近对流感病毒 (IAV) 疫苗的研究提供了一些有用的见解。 用 IAV 基质蛋白 (M2e) 或核蛋白 (NP) 进行免疫均会产生保护性免疫。 COVID-19 疫苗研究人员可以尝试同时针对高度可变的 SARS-CoV-2 S 蛋白和独特保守的 SARS-CoV-2 蛋白(如 ORF8)。 虽然 ORF8 蛋白目前尚未定性,但它可能是第二代 SARS-CoV-2 疫苗的一个新保守抗原靶点。
目前少量的临床疫苗和临床前疫苗使用全灭活病毒 (IV) 或减毒活病毒 (LAV),它们应向免疫系统提供多种抗原。 数量更少的多表位/多抗原疫苗正在开发中,并且缺乏临床数据。 虽然初步表明可以达到可接受的保护水平,但中和抗体减少的原因尚不清楚,需要进一步研究以更好地了解保护性免疫。
需要新的治疗方法应对不断进化的病毒
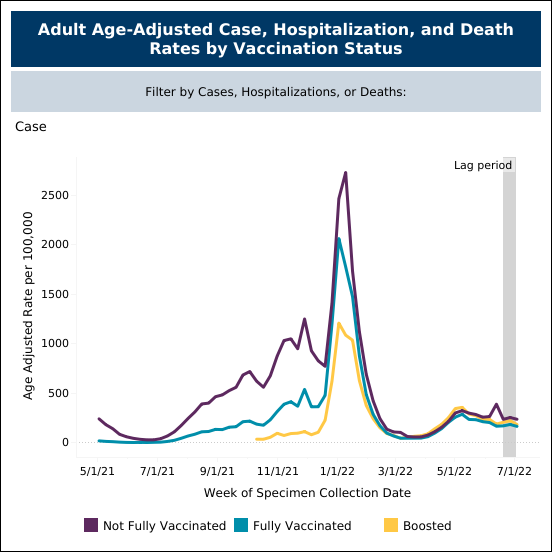
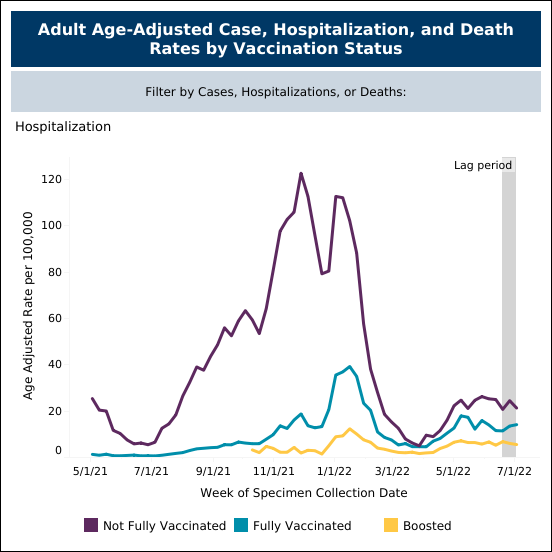
目前仅靶向于 S 蛋白的 SARS-CoV-2 疫苗是开始研发抗病毒疗法和下一代疫苗的重要一步。 这些研发的速度和效率是前所未有的。 即使是针对像 Delta 这样的新变体,数据显示疫苗也显著减少了住院人数和死亡人数。 然而,随着病毒的不断变异和进化,仅靶向于 S 蛋白可能不足以获得保护性免疫。 我们期待一种更全面的方法,可能包括多种类型的疫苗与抗病毒疗法相结合,这些疗法针对更广泛的抗原,可真正阻止病毒传播。
想了解最新的 COVID-19 信息和资源吗? 访问我们的 COVID-19 资源页面,获取独特的见解、同行评审的出版物和数据,以促进您的 COVID-19 研究。 此外,请务必订阅 CAS 博客以获取持续更新和见解。