O Prêmio Nobel de Química de 2022 ficou com Carolyn R. Bertozzi, Morten Meldal e K. Barry Sharpless pelo desenvolvimento da química de cliques e da química bio-ortogonal. O trabalho descreve reações que podem ser usadas para conectar rapidamente moléculas em condições ambientais ou biológicas. Essa pesquisa tem ampla aplicação, sendo utilizada desde polímeros e produtos farmacêuticos até o estudo de mecanismos biológicos e o desenvolvimento de novos bioterapêuticos.
Recursos do CAS sobre química bio-ortogonal: relatório de insights, publicação de revistas sobre química bioconjugada, artigo sobre o papel dos açúcares na química bio-ortogonal
O que é a química de cliques?
A química de cliques é um conjunto de reações rápidas e específicas para o arranjo de fragmentos em estruturas mais complexas. O termo "química de cliques" foi criado pelo professor K. Barry Sharpless, que imaginou a formação de inibidores enzimáticos acoplando moléculas menores no sítio ativo de uma enzima. O laboratório dele e de Morten Meldal desenvolveu versões regiosseletivas catalisadas por cobre da cicloadição Huisgen de azidas e alcinos terminais para formar 1,2,3-triazóis. Devido à sua facilidade e confiabilidade, este método tem sido usado para a preparação de polímeros, anticorpos e produtos farmacêuticos. Outras reações de clique, como tiol-eno e SuFEx, também foram desenvolvidas, principalmente para uso com polímeros.
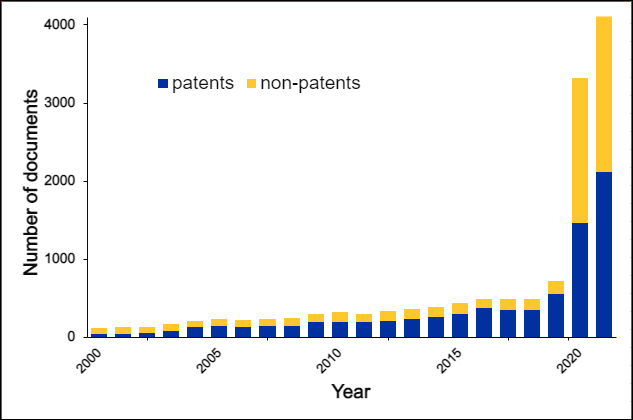
Aproximadamente 30 mil documentos nos bancos de dados do CAS usaram o conceito de “química de cliques”. A referência mais antiga à “química do clique” nos bancos de dados do CAS foi em 1999 (“Click chemistry: a concept for merging process and discovery chemistry” (com H. C. Kolb), Book of Abstracts, 217º ACS National Meeting, Anaheim, Califórnia, 21-25 de março (1999), ORGN-105 Editora: American Chemical Society, Washington, D.C.), enquanto a referência mais antiga do grupo sobre a reação de cicloadição de azida-alcino data de 2002. O documento mais citado pelo grupo Sharpless sobre a química de cliques, “Click chemistry: diverse chemical function from a few good reactions” foi citado mais de 11.000 vezes.
O que é a química bio-ortogonal?
A química bio-ortogonal (um termo usado pela primeira vez por Carolyn Bertozzi no final da década de 1990) descreve reações que ocorrem rapidamente sob condições biológicas (à temperatura ambiente ou próximo à temperatura ambiente, em soluções aquosas, na presença de moléculas biológicas e em baixas concentrações). Muitas moléculas com diferentes grupos funcionais estão presentes nas células, e reações que reagem seletivamente com um único grupo funcional seriam úteis para entender o comportamento de sistemas biológicos.
Carolyn Bertozzi e seu grupo de pesquisa primeiro desenvolveram as reações de Staudinger de azidas com triarilfosfinas substituídas por éster para uso no estudo de carboidratos em sistemas biológicos. Os catalisadores de cobre necessários para acelerar as cicloadições de azida-alcino sob condições biológicas à temperatura ambiente são tóxicos para as células. O laboratório Bertozzi desenvolveu alcinos cíclicos tensos com base no trabalho realizado por Wittig e Krebs no início dos anos 1960. Os alcinos cíclicos sofrem cicloadições de azida-alcino promovidas por tensão (SPAAC) sem um catalisador e à temperatura ambiente e, portanto, podem ser usados em células vivas. O SPAAC tem sido importante para visualizar e compreender os processos biológicos nas células vivas. Uma variedade de outras reações bio-ortogonais foram desenvolvidas.
Aproximadamente 3 mil documentos nos bancos de dados do CAS usaram o termo “química bio-ortogonal”, dos quais a referência mais antiga foi à tese de doutorado de G. A. Lemieux, um estudante de doutorado no laboratório do professor Bertozzi. O desenvolvimento de reações bio-ortogonais pelo laboratório do professor Bertozzi é discutido em “From Mechanism to Mouse: A Tale of Two Bioorthogonal Reactions”. Uma visão geral das reações bio-ortogonais é fornecida em uma revisão separada, que também é o artigo mais citado pelo grupo Bertozzi discutindo a química bio-ortogonal, com mais de 2.400 citações.
Como é a jornada para o Prêmio Nobel?
A química bio-ortogonal cresceu notavelmente nas últimas duas décadas, encontrando um uso mais difundido nos últimos anos. Desenvolvimentos e aplicações notáveis no campo são resumidos nesta linha do tempo.
Além disso, o CAS Content Collection foi analisado para comparar o aumento nas publicações de termos bio-ortogonais e o aumento nas aplicações da química bio-ortogonal.
Isso demonstra que a imagiologia correspondeu ao uso mais frequente da química bio-ortogonal de 2010 a 2020, seguida por aplicações farmacêuticas. O uso da química bio-ortogonal para rotulagem foi relatado em quase tantos documentos quanto seu uso em produtos farmacêuticos, embora a rotulagem provavelmente represente uma variedade de usos não caracterizados de outra forma. Números semelhantes de documentos usaram a química bio-ortogonal em hidrogeis ou agentes de diagnóstico para estudos mecanísticos ou de espectrometria de massa.
Que oportunidades futuras aguardam a química bio-ortogonal?
Os campos de imagem, diagnóstico e administração de medicamentos foram transformados por essas abordagens, mas ainda mais oportunidades surgiram nestas áreas:
- Exploração do desenvolvimento de parceiros reativos com estabilidades biológicas aprimoradas ou simplificação de métodos para eliminar a necessidade de catalisadores (reduzindo toxicidades);
- A rotulagem múltipla levaria a uma exploração simplificada de mecanismos biológicos e agentes de diagnóstico mais confiáveis;
- Químicas melhoradas ativadas por luz poderiam minimizar os danos aos organismos e permitir imagens ainda mais profundas dentro de organismos vivos
Esses métodos permitiram uma síntese mais fácil e confiável, a melhor compreensão dos mecanismos biológicos e o desenvolvimento de tratamentos mais eficazes e seletivos. O trabalho levou a avanços em química, biologia e medicina, abrindo portas para trabalhos que, de outra forma, não seriam possíveis. Para ter uma visão panorâmica única deste campo, baixe nosso Relatório de insights que se baseia em tendências históricas para destacar as oportunidades futuras para a química bio-ortogonal ou confira as publicações revisadas por pares.