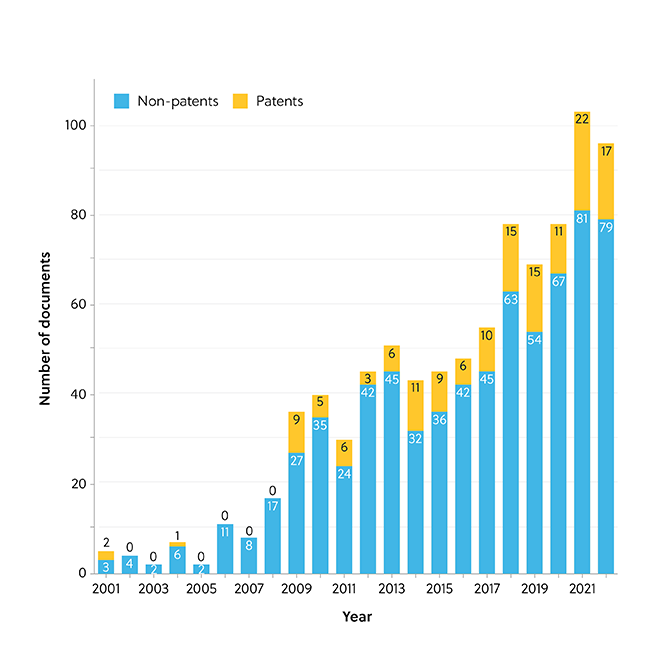
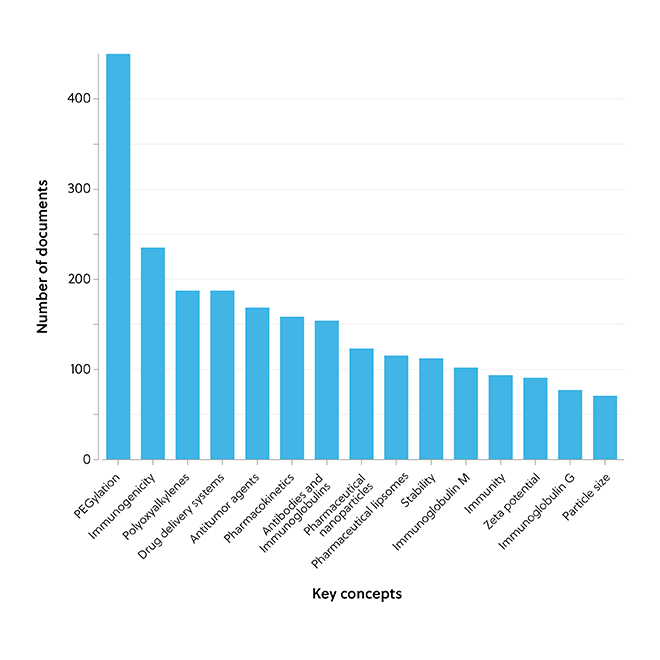
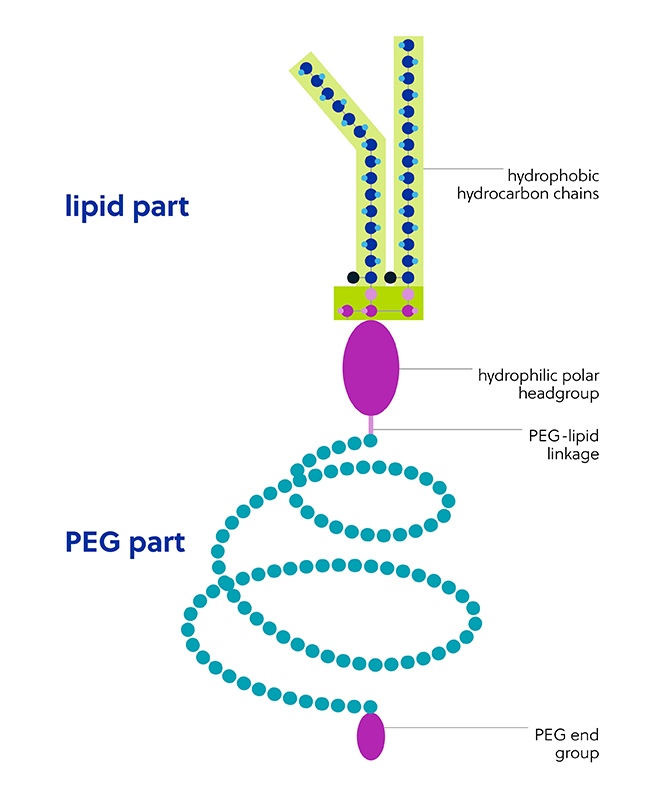
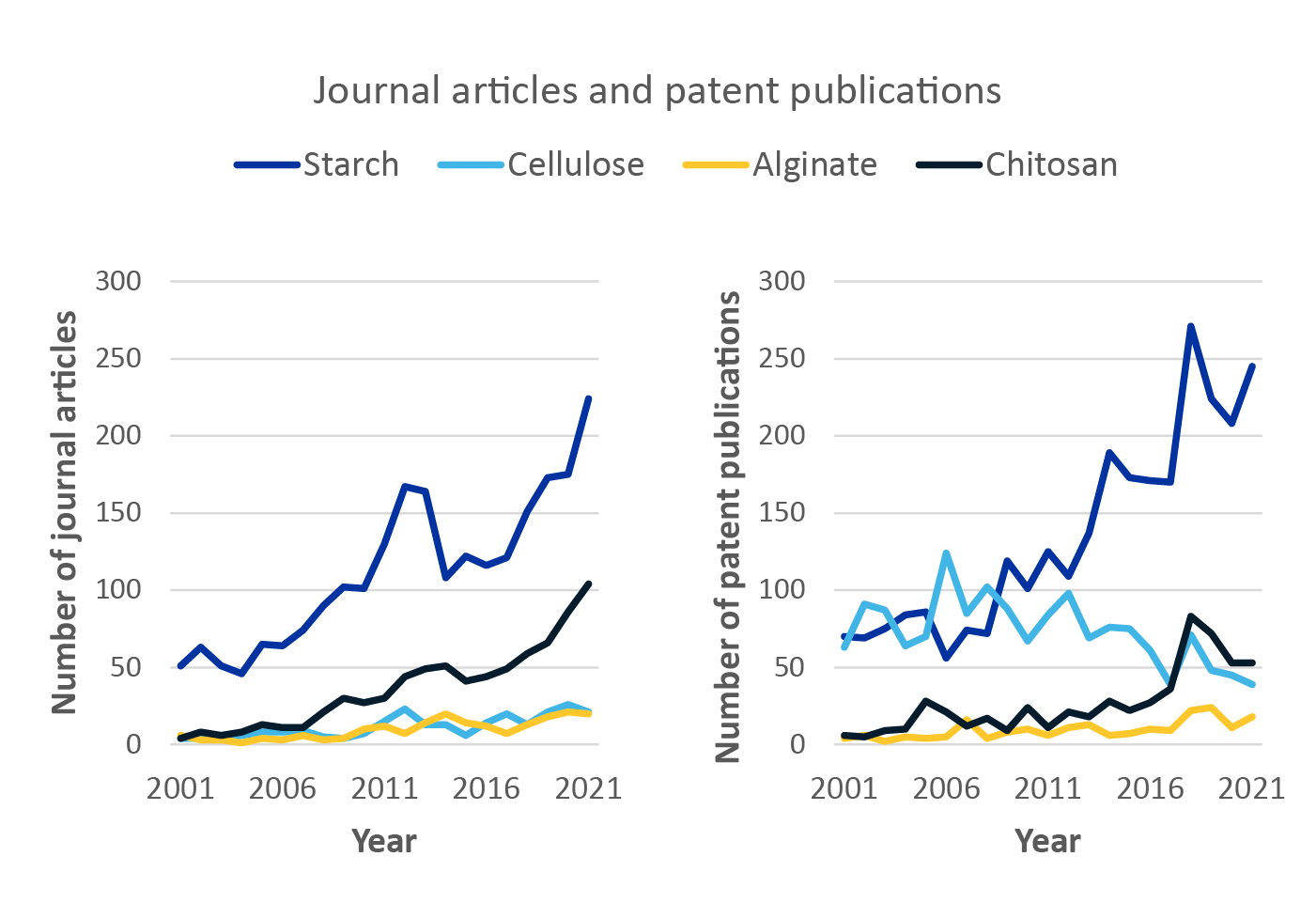
Gain new perspectives for faster progress directly to your inbox.

特許分析を通じていかに研究開発の機会を最大化するか
競争が激化している昨今の市場においては、研究開発のチームは、イノベーションを推進させそして時代を先取りする新しい機会を常に模索しています。 ただ、あまりにも情報量が膨大なため、非生産的な研究にリソースを浪費しないよう有望な開発分野を特定するのは困難です。 このような場合、特許の現状分析が大きく役立ちます。
特許の現状分析とは
このプロセスでは、特定の業界や分野における技術の状勢を深く掘り下げ、現在存在している特許等を包括的に理解することを行います。 特許の現状分析とは、特定の研究分野に関連する特許や科学文献の調査を行うことを指します。 過去数年間の開発を調査することによって、新たなトレンドに関する洞察が得られるとともに、新規の機能性材料を求めたり、既存薬をリパーパシングしたり、または新薬を開発したりなど、潜在的な機会を特定できるようになります。 これにより、学術組織や研究開発チームは、努力とリソースを集中すべき領域について、より多くの情報に基づいた決定ができるようになるのです。
特許の現状分析には、特許マッピング、特許引用分析、そして特許ポートフォリオ分析など、いくつかの手法が含まれます。 特許マッピングでは、ひとつの技術分野で出願されたすべての特許を確認できるため、トレンドやパターンを容易に把握することができます。 特許引用分析では、ひとつの特許内における引用を調査することで、アナリストはその技術分野で最も影響力のある特許と中心的存在を特定できるようになります。 そして特許ポートフォリオ分析では、ある企業が出願した特許を分析することにより、特定の技術分野におけるその企業の強みと弱みを把握できます。
つまり、特許の現状分析とは、特定技術を深くまで掘り下げ、隠れたトレンドを明らかにし、そして市場で優位に立つための方法なのです。 では、特許の現状分析の価値と機会を最大化させるためには、どうしたらよいのでしょうか。
それは適切なツールに早めに投資しておくことから始まる
特許の現状分析における課題は、2つあります。まずはその膨大な情報量。そして、類似した概念を指すのにたくさんの用語が使われていて一貫性がないことです。 これだけ多くの情報がある中、自分の研究に関連するものを絞り込むのには、時間がかかります。 体系化された方法もなく、ただ単独で取り組むとより困難になるだけで、意義ある洞察を導き出すことはほぼ不可能になってしまいます。
そこで、まず自分のアイデアがどれほど重要なのか、そして他者が同じ分野にはたして投資してくることが予想されるのかどうか、そういったことを考慮する必要があります。 その特許をグローバルな規模で出願をするつもりなら、その市場に自信を持って参入できるようにしてくれるような、目的に合致したツールが必要になります。 理想としては、有形無形のアセットに多額の投資を行う前に、特許の現状分析のための信頼できる効率的なツール群があることが望ましいでしょう。 最初からツールを使わないで成功することも可能ですが、それは一般的ではありません。またチャンスを逃したり、情報過多になったり、投資判断を誤ってしまうなどのリスクも発生します。
特許の現状分析に関する最近のWIPOの研究では、情報の質の高さと、その名称に関係なく物質を見つけられることがいかに重要かが指摘されています。 科学関連の研究開発組織の多くが早い段階からCASを利用しているのも、そのためです。初期段階のお客様の中には、社員の正式なオンボーディングの前から、CASのソリューションをご利用いただいているケースもあります。
特許の現状分析に大改革を。適切なツールがあれば、市場トレンドを把握し、そして市場ニーズを予測できる
世界的な状況を確認する際には、精査しなければならない情報はかなりの量に上ります。 市場ニーズを把握するには、最近の開発やイノベーション、そして過去数年間の特許関連の活動を評価する必要があります。 例えば仮に、過去3年間以内に発表された文献を見たところ、自社の研究開発の取り組みやイノベーションを取り巻く特許申請と科学文献の動向に、相当の変化があったことに気付いたとします。 その場合、市場が向かっている方向は明らかであり、どこにイノベーションのギャップがあるのかもわかります。
適切なツールを使用すれば、色々な質問に対する回答が得られるようになります。例えば、市場や研究開発の場では、今何が起きているのか。何が成功しているのか。最近の出来事によって特許の現状がどのように変化したのか。あるいは、具体的な例で言えば、すでに存在していて長い間使用されてきた医薬品で、他の疾患に再利用できるものは何なのか。 こういったことによって、意思決定のスピードが向上し、研究開発ポートフォリオ管理に自信を持てるようになるのです。
例えば、FDAが関節リウマチやアトピー性皮膚炎など複数の疾患の治療薬として承認しているキナーゼ阻害剤が、最近の論文でタウ異常症の調節因子を阻害することが示されたとします。その場合、そのキナーゼ阻害剤(または類似化合物)には、神経変性疾患へのリパーパシング(既存薬再開発)の可能性があるかもしれません。 特許の現状分析を行えば、リパーパシングできる物質を特定したり、誰がすでにそれを研究しているかを知ることができるのです。 包括的な知的財産検索ツールがあれば、より速く、より簡単に、そしてより信頼性をもってこれを行うことができます。
WIPOの最新の報告書では、グリーンテクノロジーの発展に関する洞察は、いつ市場に参入するべきか、そしてどこに隙間がありそうかなどを示していると述べています。 グリーンテクノロジーに関わる特許活動は、過去20年間で飛躍的に伸びています。 風力、水素エネルギー、低公害車両の技術のグローバルな特許出願件数は飛躍的に増加し、5年間は毎年平均して倍増してきています1。
CAS コンテンツコレクションTM について
-
CASの各ソリューションの根幹になっているのは、人の手で収集・精選された膨大な科学データと特許データです。 特許と文献の記録が詳細な索引で補強されているので、サーチャーは、結果をより明確に見つけだし、そしてそれを理解できるようになっています。
成功の秘訣 - 適切なツールがあれば、競合他社に差をつけ、研究開発の意思決定に役立つ先行指標を特定できる
特許の現状分析は、先行指標を特定し、競合相手の活動を追跡することにより、研究開発チームが一歩先を行くのに役立ちます。 STN IP Protection SuiteTM内のCAS Scientific Patent ExplorerTMなどのツールを使用することで、特許関連の活動を簡単に追跡し、競合する組織を特定できるようになります。 大手製薬企業など、既知の競合相手の結果が得られるだけでなく、小規模のスタートアップ企業や、他の業種または他の地域の市場、そして場合によっては貴組織のイノベーション領域における潜在的な協力相手すら、判明させることができるかもしれません。
競合相手の出願先などの特許関連活動を常に把握しておくことで、研究開発チームは、最新の開発動向について常に情報を得ることができ、また研究努力と投資を集中すべきところについて、戦略的な決定を下すことができます。 例えば、競合他社が英国で出願したことが確認できたとします。貴組織がその地域で出願する予定がなかったのなら、競合相手がなぜ英国で出願しているのか、そして貴組織も英国で出願を検討するべきかどうか、調査が必要であることが分かるわけです。
さらに、その際に適切なツールがあれば、特定の物質に関連する文献について、例えば製剤、特定の成分、そして適応症などの正確な情報を見つけることができます。 それが生物学的物質であろうと化学物質であろうと、特許内で登場しているのなら、CASならその物質の名前を特定し、識別子を提供することができるでしょう。 既知の物質であれば、その物質がどのように公開されたかに関係なく、例えば関連する臨床コード、ラボコード、商品名、一般名、CAS 登録番号®の記録が収載されているのです。
例として「Upadacitinib」を検索すると、たとえ化学構造にしか言及されていなくても、関連する文献がヒットします。 このレベルの精度と関連性は、他のツールでは得られません。 CASは、競合他社がどの物質を研究しているかを正確に特定することができます。たとえ最初に特許で開示されたのが、何百、何千もの物質を表すことのできるただのマルクーシュ構造であったとしても、です。 これは、他の方法では得られない情報です。つまり、CAS STNext® を含むCASソリューションは、医薬品の開発だけでなく、工学、材料、化学など、その他の科学分野の研究開発において、競合他社に先んじるためには欠かせないツールなのです。
まとめ
特許の現状分析は、科学組織や研究開発チームにとって、新たなトレンド、潜在的な機会、そして先行指標を特定できる価値あるツールです。これを活用することで、最終的に努力とリソースをどの領域に集中させるべきかについて、より多くの情報に基づいた意思決定につなげることができます。 早期に適切なツールに投資することは、きわめて重要です。 膨大な情報量と、広範囲で一貫性のない専門用語に圧倒されてしまうと、チャンスを逃し、情報過多になり、投資判断を誤ることになりかねません。
特許の現状分析のためのツールを評価する際は、以下の機能と特徴が決め手となります。
- 包括的なコンテンツの範囲。 CAS コンテンツコレクションのように、広範囲かつ信頼できる特許・科学情報にアクセスでき、複数の管轄区域の特許および公開科学情報を検索・分析できること。
- 高度な検索 ブール検索、近接演算子、検索フィルターなどの高度な検索機能により、結果を絞り込んで精度を上げられること。
- 競合情報分析 関心分野を的確に検索し、有効な特許を確認し、競合や協力関係の可能性がある領域を特定するのに役立つ関連情報を提供できること。
- 信頼性の高い検索結果 情報を収集し、それを分析または主要ステークホルダーと共有しやすくするためにデータとしてエクスポートできること。
研究開発の機会を最大化させるには、科学組織と研究開発チームは、信頼性が高くそして効率的な特許検索ツールに投資することを検討する必要があります。
CAS Scientific Patent Explorerを使えば、革新的な知的財産に関する洞察をいかに収集できるようになるか、その詳細はこちらをご覧ください。ウェビナーを見る
参考文献
Harrison, C. Analyzing the Green Tech IP Landscape. WIPO Green Webinar Series. 2022年3月。 アクセス日:3月15日